वायरल संक्रमण माइटोकॉन्ड्रियल फ़ंक्शन को नियंत्रित करता है
Sep 07, 2023
अमूर्त: माइटोकॉन्ड्रिया यूकेरियोटिक कोशिकाओं में चयापचय और क्रमादेशित कोशिका मृत्यु में शामिल महत्वपूर्ण अंग हैं। इसके अलावा, माइटोकॉन्ड्रिया वायरस के खिलाफ मेजबान कोशिकाओं की जन्मजात प्रतिरक्षा से भी निकटता से संबंधित है। माइटोकॉन्ड्रियल आकृति विज्ञान और कार्य की असामान्यता विभिन्न प्रकार की बीमारियों को जन्म दे सकती है। बड़ी संख्या में अध्ययनों में पाया गया है कि विभिन्न प्रकार के वायरल संक्रमण माइटोकॉन्ड्रियल गतिशीलता को बदल सकते हैं, माइटोकॉन्ड्रिया-प्रेरित कोशिका मृत्यु में मध्यस्थता कर सकते हैं, और इंट्रासेल्युलर अस्तित्व को बनाए रखने के लिए माइटोकॉन्ड्रियल चयापचय स्थिति और सेलुलर जन्मजात प्रतिरक्षा प्रतिक्रिया को बदल सकते हैं। इस बीच, माइटोकॉन्ड्रिया वायरल संक्रमण के दौरान एक एंटीवायरल भूमिका भी निभा सकता है, जिससे मेजबान की रक्षा होती है। इसलिए, माइटोकॉन्ड्रिया मेजबान और वायरस के बीच बातचीत में एक महत्वपूर्ण भूमिका निभाता है। इसमें, हम संक्षेप में बताते हैं कि कैसे वायरल संक्रमण माइटोकॉन्ड्रियल आकृति विज्ञान और कार्य को बदलकर माइक्रोबियल रोगजनन को प्रभावित करते हैं और कैसे वायरस मेजबान प्रतिरक्षा प्रतिक्रिया से बच जाते हैं।
कीवर्ड: माइटोकॉन्ड्रियल विखंडन और संलयन; वाइरस संक्रमण; एपोप्टोसिस; मेजबान जन्मजात प्रतिरक्षा

सिस्टैंच पौधा-बढ़ाने वाली प्रतिरक्षा प्रणाली
1. माइटोकॉन्ड्रिया की शारीरिक आकृति विज्ञान
माइटोकॉन्ड्रिया की उत्पत्ति एक प्राचीन जीवाणु एंडोसिम्बियोन्ट से हुई है, और यह लगभग सभी कोशिकाओं में पाए जाने वाले महत्वपूर्ण अंग हैं। माइटोकॉन्ड्रिया के पहली बार रिपोर्ट होने के बाद से लगभग 130 वर्षों में, नए कार्यों की खोज की गई है। माइटोकॉन्ड्रिया डायनामिन-संबंधित GTPases के एक समर्पित सेट द्वारा मध्यस्थता वाले विखंडन और संलयन के माध्यम से माइटोकॉन्ड्रियल नेटवर्क के गतिशील संतुलन को बनाए रखता है, कोशिकाओं के लिए ऊर्जा प्रदान करता है, और ऑटोफैगी, कैल्शियम होमोस्टैसिस, जन्मजात प्रतिरक्षा, सिग्नल ट्रांसडक्शन और एपोप्टोसिस जैसी प्रक्रियाओं को नियंत्रित करता है [1] ]. माइटोकॉन्ड्रिया कोशिका के भीतर अत्यधिक गतिशील प्रक्रिया में होते हैं, माइटोकॉन्ड्रिया की आकृति विज्ञान को नियंत्रित करने के लिए विखंडन और संलयन चक्र से गुजरते हैं। फ़ज़ी प्याज (Fzo) ड्रोसोफिला शुक्राणुजनन के दौरान माइटोकॉन्ड्रियल संलयन में मध्यस्थता करने वाला पहला प्रोटीन है, और Fzo जीन में उत्परिवर्तन माइटोकॉन्ड्रियल संलयन विकार और ड्रोसोफिला शुक्राणु कोशिकाओं में असामान्य संचय का कारण बन सकता है [2]। स्तनधारियों में, माइटोकॉन्ड्रियल संलयन में मध्यस्थता करने वाले प्रोटीन में मुख्य रूप से एमएफएन1 (मिटोफ्यूसिन1), एमएफएन2 (मिटोफ्यूसिन2), और ओपीए1 (ऑप्टिक एट्रोफी 1) [3-5] शामिल हैं। एमएफएनएस में हेप्टाड रिपीट क्षेत्र (एचआर2) होते हैं, और एमएफएन1 और एमएफएन2, बाहरी माइटोकॉन्ड्रियल झिल्ली (ओएमएम) पर स्थित होते हैं, एचआर2 संरचनाओं के ऑलिगोमेराइजेशन के माध्यम से एमएफएन1/एमएफएन2 होमोडीमर या एमएफएन1/एमएफएन2 हेटेरोडिमर बनाने के लिए बातचीत करते हैं, जिससे चरण ट्रांस-प्लगिंग को बढ़ावा मिलता है। आसन्न ओएमएम [6,7], और इसमें जीटीपी हाइड्रोलिसिस शामिल है, जो अंततः ओएमएम [8,9] के संलयन की ओर ले जाता है। OPA1, IMM से स्थानीयकृत एक गतिशील रूप से संबंधित GTPase, IMM फ़्यूज़न में भाग लेता है। ओपीए1 प्रोटीन को इंटरमेम्ब्रेन स्पेस में विभिन्न टुकड़ों में हाइड्रोलाइज किया गया था: एक माइटोकॉन्ड्रियल संलयन से जुड़ा लंबा उपप्रकार एल-ओपीए1 है, और दूसरा छोटा उपप्रकार एस-ओपीए1 [10,11] है। L-OPA1 अपने GTPase डोमेन और इसके आसन्न माइटोकॉन्ड्रियल झिल्ली कार्डियोलिपिड (CL) के बीच हेटेरोमोर्फिक इंटरैक्शन के माध्यम से चयनात्मक माइटोकॉन्ड्रियल संलयन प्राप्त करता है। संलयन-मध्यस्थ प्रोटीन (एमएफएन1, एमएफएन2, और ओपीए1) की हानि माइटोकॉन्ड्रियल आकृति विज्ञान में परिवर्तन का कारण बन सकती है, जिससे माइटोकॉन्ड्रियल विखंडन हो सकता है। माइटोकॉन्ड्रियल संलयन एक आवश्यक सेलुलर प्रक्रिया है जो माइटोकॉन्ड्रियल टुकड़ों के विलय की सुविधा प्रदान करती है और माइटोकॉन्ड्रियल डीएनए, प्रोटीन और मेटाबोलाइट्स के आदान-प्रदान में मध्यस्थता करती है। जीन नॉकआउट और आरएनए हस्तक्षेप तकनीकों द्वारा माइटोकॉन्ड्रियल व्यंजन प्रोटीन को हटा दिया गया, जिससे माइटोकॉन्ड्रियल विखंडन हुआ [3,5]। माइटोकॉन्ड्रिया "माइटोकॉन्ड्रियल विखंडन" के माध्यम से क्षतिग्रस्त माइटोकॉन्ड्रिया को भी छोटे टुकड़ों में तोड़ सकता है। स्तनधारी कोशिकाओं में, Drp1 एक महत्वपूर्ण प्रोटीन है जो माइटोकॉन्ड्रियल विखंडन में मध्यस्थता करता है। Drp1 सक्रिय होने के बाद, इसे साइटोसोल से OMM में भर्ती किया जाता है, जहां ऑलिगोमेराइजेशन होता है। Drp1 ओएमएम के व्यास के भीतर छल्ले और सर्पिल बनाता है और इसकी जीटीपी-एंजाइम गतिविधि के आधार पर जीटीपी को हाइड्रोलाइज करता है, जिसके परिणामस्वरूप झिल्ली संकुचन और विच्छेदन होता है [12,13]। Drp1 के परिवहन और कार्य को दो प्रमुख श्रृंखलाओं में फॉस्फोराइलेशन के विरोधी प्रभावों द्वारा तेजी से नियंत्रित किया जाता है। सामान्य तौर पर, सेरीन 616 का फॉस्फोराइलेशन Drp1 गतिविधि को बढ़ाता है और माइटोकॉन्ड्रियल एकत्रीकरण के लक्ष्य को बढ़ावा देता है, जबकि सेरीन 637 में फॉस्फोराइलेशन Drp1 की गतिविधि को कम करता है, इसे साइटोप्लाज्म में रखता है [14]। उदाहरण के लिए, RIP1 Drp1 के Ser616 अवशेषों को फॉस्फोराइलेट करता है, जिससे माइटोकॉन्ड्रियल विखंडन प्रेरित होता है और माइटोफैगी के माध्यम से क्षतिग्रस्त माइटोकॉन्ड्रिया को नष्ट कर देता है, जब कोशिकाएं ऊर्जा तनाव की स्थिति में होती हैं [15]। Drp1 के Ser637 पर फॉस्फोराइलेशन GED डोमेन के साथ GTP-बाध्यकारी/मध्य डोमेन की बातचीत को रोकता है, जिससे GTPase गतिविधि कम हो जाती है और Drp1 फ़ंक्शन और माइटोकॉन्ड्रियल आकारिकी में परिवर्तन होता है [16]। Drp1 को अपना कार्य करने के लिए विभिन्न सहायक प्रोटीनों की आवश्यकता होती है। वर्तमान में, माइटोकॉन्ड्रियल विखंडन कारक (माइटोकॉन्ड्रियल विखंडन कारक, एमएफएफ), माइटोकॉन्ड्रियल विखंडन प्रोटीन 1 (माइटोकॉन्ड्रियल विखंडन प्रोटीन 1, फिस1), माइटोकॉन्ड्रियल डायनेमिन 49 (49 केडीए के माइटोकॉन्ड्रियल डायनेमिक्स प्रोटीन, एमआई डी49), और माइटोकॉन्ड्रियल डायनेमिन 51 (माइटोकॉन्ड्रियल डायनेमिक्स प्रोटीन) माइटोकॉन्ड्रिया पर स्थित 51 kDa, MiD51) को Drp1 के लिए लिगैंड के रूप में कार्य करते हुए पाया गया है, जो Drp1 को माइटोकॉन्ड्रिया में भर्ती करता है और माइटोकॉन्ड्रियल विखंडन को नियंत्रित करता है [17]। Fis1, यीस्ट कोशिकाओं में एकमात्र Dnm1 रिसेप्टर, स्तनधारी कोशिकाओं में माइटोकॉन्ड्रिया में Drp1 की भर्ती के लिए विवादास्पद है। उदाहरण के लिए, Fis1 और Drp1 स्तनधारी कोशिकाओं में परस्पर क्रिया करते हैं, और Fis1 का स्तर बढ़ने से माइटोकॉन्ड्रियल विखंडन को बढ़ावा मिलेगा [18]। हालाँकि, कोलन कैंसर कोशिकाओं में Fis1 विलोपन से पता चलता है कि यह माइटोकॉन्ड्रियल विभाजन के लिए आवश्यक नहीं है [19]। एक हालिया अध्ययन में पाया गया कि मानव Fis1 Mfn1, Mfn2 और OPA1 से जुड़कर माइटोकॉन्ड्रियल संलयन तंत्र को अवरुद्ध करता है, यह सुझाव देता है कि Drp1 मानव Fis1 फ़ंक्शन के लिए डिस्पेंसेबल है [20]। एमएफएफ प्रोटीन भी Drp1 का एक रिसेप्टर अणु है, यह एमिनो-टर्मिनल साइटोप्लाज्मिक क्षेत्र के माध्यम से Drp1 के साथ संपर्क करता है और OMM पर सजातीय रूप से वितरित होता है, मुख्य रूप से Drp1 [19] के समान स्थानों पर। एमएफएफ की अधिक अभिव्यक्ति माइटोकॉन्ड्रिया में डीआरपी1 की भर्ती को बढ़ावा दे सकती है जबकि एमएफएफ अभिव्यक्ति को शांत करने से माइटोकॉन्ड्रियल संलयन को बढ़ावा मिल सकता है। इसके अलावा, माइटोकॉन्ड्रियल डायनेमिक्स प्रोटीन (MiDs) fifis1 और Drp1 की कमी वाली कोशिकाओं में माइटोकॉन्ड्रियल विखंडन में शामिल होते हैं। जब MiDs अत्यधिक अभिव्यक्त होते हैं, तो वे माइटोकॉन्ड्रियल बढ़ाव में मध्यस्थता करने के लिए बड़ी संख्या में निष्क्रिय S637 फॉस्फोराइलेटेड Drp1 को माइटोकॉन्ड्रिया में भर्ती करते हैं [21,22]। माइटोकॉन्ड्रिया कोशिका चयापचय, क्रमादेशित कोशिका मृत्यु और जन्मजात प्रतिरक्षा और वायरल संक्रमण के प्रति मेजबान प्रतिक्रिया जैसी सेलुलर गतिविधियों की एक श्रृंखला में शामिल हैं। इसके अलावा, दीर्घकालिक विकासवादी प्रक्रिया में, वायरस ने माइटोकॉन्ड्रिया को लक्षित करके अपने इंट्रासेल्युलर अस्तित्व को प्रभावित करने के लिए एक मार्ग विकसित किया है, और माइटोकॉन्ड्रिया-प्रेरित कोशिका मृत्यु की मध्यस्थता करके, वे मेजबान प्रतिरक्षा को फैला सकते हैं या उससे बच सकते हैं। इस समीक्षा में, हम पता लगाते हैं कि वायरस माइटोकॉन्ड्रिया में कैसे हेरफेर करते हैं और यह हेरफेर माइक्रोबियल रोगजनन को कैसे प्रभावित करता है।

सिस्टैंच जड़ी बूटी-एंटीट्यूमर के प्रभाव
2. वायरल संक्रमण माइटोकॉन्ड्रियल गतिशीलता को बाधित करता है
विभिन्न प्रकार के वायरल संक्रमण माइटोकॉन्ड्रिया के गतिशील संतुलन को नष्ट करके माइटोकॉन्ड्रियल ऑटोफैगी को प्रेरित कर सकते हैं, जो वायरल स्व-संक्रमण के लिए अनुकूल है। हेपेटाइटिस सी वायरस (एचसीवी) के रोगियों में माइटोकॉन्ड्रियल रूपात्मक परिवर्तनों की प्रारंभिक खोज के बाद से, अधिक से अधिक अध्ययनों ने एचसीवी संक्रमण के कारण माइटोकॉन्ड्रियल फ़ंक्शन में परिवर्तनों पर ध्यान केंद्रित किया है, जो एक सकारात्मक-स्ट्रैंड आरएनए वायरस है [23]। एचसीवी कोर प्रोटीन को लक्षित किया जा सकता है और ओएमएम पर स्थित किया जा सकता है, जिसके परिणामस्वरूप इलेक्ट्रॉन परिवहन कॉम्प्लेक्स I में कमी आती है, माइटोकॉन्ड्रियल इलेक्ट्रॉन परिवहन में बाधा आती है, और प्रतिक्रियाशील ऑक्सीजन प्रजातियों (आरओएस) के उत्पादन में वृद्धि होती है [24,25]। एचसीवी कोर, ई1 और एनएस3 प्रोटीन के माध्यम से आरओएस उत्पादन को भी प्रेरित करता है, जो माइटोकॉन्ड्रियल पारगम्यता संक्रमण को ट्रिगर करता है, जिससे डीएनए क्षति और एसटीएटी3 सक्रियण होता है [26]। Ca2+ और ROS द्वारा प्रेरित माइटोकॉन्ड्रियल पारगम्यता सीमा को कम करना हेपेटाइटिस सी वायरस संक्रमण की एक विशेषता है। यह माइटोकॉन्ड्रिया के साथ एचसीवी कोर प्रोटीन की बातचीत का प्रत्यक्ष परिणाम है [27]। एचसीवी संक्रमण वायरल दृढ़ता को बढ़ावा देने के लिए माइटोकॉन्ड्रियल विखंडन और माइटोफैगी को बढ़ावा देकर माइटोकॉन्ड्रियल गतिशीलता को भी बाधित करता है। HCV Drp1 (Ser616) के फॉस्फोराइलेशन को प्रेरित करता है और माइटोकॉन्ड्रियल विखंडन में मध्यस्थता करने के लिए इसे माइटोकॉन्ड्रिया तक पहुंचाता है, जिससे माइटोफैगी होती है [28]। एचसीवी-प्रेरित माइटोकॉन्ड्रियल विखंडन और माइटोफैगी का हस्तक्षेप ग्लाइकोलाइसिस और एटीपी उत्पादन को कम कर सकता है और साथ ही इंटरफेरॉन संश्लेषण को बढ़ा सकता है, जिससे वायरल स्राव बाधित हो सकता है [28]। एक अन्य अध्ययन से पता चला है कि एचसीवी-प्रेरित माइटोकॉन्ड्रियल विखंडन न केवल डीआरपी1 प्रोटीन पर निर्भर है, बल्कि एचसीवी एनएस5ए प्रोटीन फॉस्फेटिडिलिनोसिटोल 4-किनेज III के साथ भी बातचीत कर सकता है, जो माइटोकॉन्ड्रियल विखंडन को प्रेरित करता है [29]। एचसीवी पार्किन और पिंक1 की अभिव्यक्ति को प्रेरित करता है और माइटोफैगी को मध्यस्थ करने के लिए पार्किन के माइटोकॉन्ड्रिया में स्थानांतरण को ट्रिगर करता है। पार्किन और PINK1 को शांत करके माइटोफैगी का निषेध माइटोकॉन्ड्रियल कॉम्प्लेक्स I एंजाइम गतिविधि को आंशिक रूप से बचा सकता है और HCV प्रतिकृति को रोक सकता है [28]। दिलचस्प बात यह है कि एचसीवी कोर प्रोटीन पार्किन के साथ इंटरैक्ट करता है, पार्किन के माइटोकॉन्ड्रिया में स्थानांतरण को रोकता है, जिससे माइटोकॉन्ड्रियल ऑटोफैगोसोम का निर्माण होता है और ऑटोफैगी गिरावट की विफलता होती है [30]। क्लासिकल स्वाइन फीवर वायरस (सीएसएफवी) और डेंगू वायरस (डीईएनवी) एचसीवी के समान ही वायरस के परिवार से संबंधित हैं, और संक्रमण माइटोकॉन्ड्रिया के कार्य को प्रभावित करके स्व-प्रतिकृति की सुविधा भी प्रदान कर सकता है [31-35]। सीएसएफवी संक्रमण के कारण एमएनएफ2 सर्वव्यापी और क्षीण हो जाता है और पार्किन और पिंक1 की अभिव्यक्ति और माइटोकॉन्ड्रियल ट्रांसलोकेशन को उत्तेजित करता है, जिससे माइटोकॉन्ड्रियल विखंडन होता है और माइटोफैगी बढ़ जाती है। डीआरपी1 और पार्किन को शांत करने के परिणामस्वरूप सीएसएफवी प्रतिकृति में गिरावट आई [31]। DENV प्रोटीन NS4B और NS3 Drp ट्रिगर माइटोकॉन्ड्रियल विखंडन को रोककर माइटोकॉन्ड्रियल गतिशीलता में असंतुलन में मध्यस्थता करते हैं, जो DENV की प्रतिकृति के लिए अनुकूल है। इसके अलावा, DENV का NS4B प्रोटीन DRP1 को निष्क्रिय कर सकता है और माइटोकॉन्ड्रियल बढ़ाव में मध्यस्थता कर सकता है [34]। माइटोकॉन्ड्रियल विस्तार माइटोकॉन्ड्रिया को जटिल झिल्ली (सीएम) के संपर्क में लाता है और माइटोकॉन्ड्रियल-संबद्ध झिल्ली (एमएएम) पर माइटोकॉन्ड्रिया-एंडोप्लाज्मिक रेटिकुलम बाइंडिंग साइट की अखंडता को नष्ट कर देता है, जिसके परिणामस्वरूप आरएलआर सिग्नल ट्रांसडक्शन विफलता और इंटरफेरॉन उत्पादन कम हो जाता है। हालाँकि, एक अन्य अध्ययन में पाया गया कि DENV MFN1 और MFN2 के NS2B3 प्रोटीन क्लीवेज के माध्यम से माइटोकॉन्ड्रियल संलयन को भी रोक सकता है, RLR सिग्नल ट्रांसडक्शन को अवरुद्ध कर सकता है और माइटोकॉन्ड्रियल झिल्ली क्षमता को नष्ट कर सकता है, जिससे DENV संक्रमण बढ़ सकता है [35]। यह भी बताया गया है कि हेपेटाइटिस बी वायरस (एचबीवी), हेपेटोविरिडे परिवार से संबंधित आंशिक रूप से डबल-स्ट्रैंडेड डीएनए वायरस, माइटोकॉन्ड्रियल गतिशीलता को बदलकर यकृत कोशिकाओं में माइटोकॉन्ड्रियल क्षति में मध्यस्थता कर सकता है, जिससे यकृत रोग हो सकते हैं। कई अध्ययनों से पता चला है कि एचबीवी एचबीएक्स प्रोटीन माइटोकॉन्ड्रिया को लक्षित कर सकता है और ओएमएम, आईएमएम या मैट्रिक्स में स्थित हो सकता है। अध्ययनों से पता चला है कि MARCH 5, एक माइटोकॉन्ड्रियल E3 यूबिकिटिन लिगेज, पॉल्यूबीक्यूटिनेशन के माध्यम से माइटोकॉन्ड्रिया पर जमा हुए HBx को ख़राब कर सकता है और Drp1, Fis1 और Mfn1 के सर्वव्यापीकरण के माध्यम से माइटोकॉन्ड्रियल गतिशीलता को नियंत्रित कर सकता है, जिससे HBV को नकारात्मक रूप से नियंत्रित किया जा सकता है [36]। HBx PINK1 अभिव्यक्ति को विनियमित करके विध्रुवित/अक्रियाशील माइटोकॉन्ड्रिया को नष्ट करने के लिए पार्किन को भर्ती करता है [37]। अन्य अध्ययनों से पता चला है कि HBV और HBx प्रोटीन ने DRP1 की अभिव्यक्ति को बढ़ावा देकर माइटोकॉन्ड्रियल विखंडन को बढ़ावा दिया। एचबीवी और एचबीएक्स प्रोटीन पार्किन-मध्यस्थता माइटोफैगी को उत्तेजित करके कोशिका अस्तित्व और लगातार वायरल संक्रमण को भी बढ़ावा देते हैं [37]। पीबी1-एफ2 इन्फ्लूएंजा वायरस की रोगज़नक़ी के लिए एक महत्वपूर्ण विषाणु कारक है, जो थॉमिक्सोविरिडे परिवार का एक घिरा हुआ आरएनए वायरस है। पीबी1-एफ2 माइटोकॉन्ड्रिया को लक्षित करता है और टीओएमएम40 चैनल के माध्यम से आईएमएम में ले जाया जाता है, जिससे माइटोकॉन्ड्रियल झिल्ली क्षमता का नुकसान होता है और माइटोकॉन्ड्रियल फ़ंक्शन बाधित होता है [38-40]। इसके विपरीत, कम रोगजनक उपप्रकार इन्फ्लूएंजा ए पीबी 1- एफ2, सी-टर्मिनल क्षेत्र की कमी के कारण माइटोकॉन्ड्रियल डिसफंक्शन का कारण नहीं बनता है [41]। पीबी1-एफ2 माइटोकॉन्ड्रिया पर टीयूएफएम (टीयू ट्रांसलेशन इलोंगेशन फैक्टर, माइटोकॉन्ड्रियल) के साथ इंटरैक्ट करता है, माइटोफैगी को प्रेरित करता है, और टाइप I इंटरफेरॉन अभिव्यक्ति को रोकता है [42]। हालाँकि, एक हालिया अध्ययन से पता चला है कि H1N1 संक्रमण माइटोकॉन्ड्रियल बढ़ाव को बढ़ावा दे सकता है और OPA1 अभिव्यक्ति को बढ़ाकर और DRP1 अभिव्यक्ति को कम करके मेजबान कोशिका के एंडोप्लाज्मिक रेटिकुलम-माइटोकॉन्ड्रियल संपर्क साइटों को बदल सकता है, जिससे माइटोकॉन्ड्रियल आकृति विज्ञान गतिशीलता में परिवर्तन होता है। इसके अलावा, मिटो-सी (एक नवीन प्रो-विखंडन यौगिक) के साथ कोशिकाओं के उपचार ने माइटोकॉन्ड्रियल फ़ंक्शन के हिस्से को बहाल करके वायरल प्रतिकृति को काफी कम कर दिया है [43]। सीवियर एक्यूट रेस्पिरेटरी सिंड्रोम कोरोनावायरस (SARS-CoV) एक सिंगल-स्ट्रैंडेड पॉजिटिव-स्ट्रैंडेड RNA वायरस है जो जीनस कोरोनावायरस से संबंधित है। इसका NSP2 PHB1 और PHB2 के साथ इंटरैक्ट करता है, जो कई सेलुलर कार्यों में शामिल होता है, जिससे इंट्रासेल्युलर सिग्नलिंग ख़राब हो जाती है और माइटोकॉन्ड्रियल बायोजेनेसिस प्रभावित होती है [44,45]। SARS-CoV विषाणु कारक ORF-9B प्रोटीसोम के माध्यम से DRP1 को भी क्षीण करता है, जिससे माइटोकॉन्ड्रियल संलयन होता है जो मेजबान की जन्मजात प्रतिरक्षा प्रतिक्रिया से बच जाता है [46]। गंभीर तीव्र श्वसन सिंड्रोम कोरोना वायरस 2 (SARS-CoV-2), जो SARS-CoV के ही परिवार का एक सदस्य है, ने वैश्विक सामाजिक और आर्थिक व्यवधान पैदा किया है। हाल के अध्ययनों से पता चला है कि SARS-CoV ऑटोफैगी को विनियमित करने, आरओएस प्रक्रियाओं को बढ़ाने और माइटोकॉन्ड्रियल फ़ंक्शन को कम करके सेल प्रतिकृति को बढ़ावा देने के लिए प्रतिरक्षा प्रतिक्रिया और सेल चयापचय में हेरफेर कर सकता है [47]। SARS-CoV -2 में, ORF9b OMM प्रोटीन आयात तंत्र [48] के TOM70 सबयूनिट के साथ इंटरैक्ट करता है, जिसका MAVS पर संभावित नियामक प्रभाव पड़ता है। SARS-CoV-2 Nsp4, जो SARS-CoV में CM गठन के लिए आवश्यक है, संभावित रूप से माइटोकॉन्ड्रियल आयात मशीनरी (TIM) कॉम्प्लेक्स के साथ इंटरैक्ट करता है [48]। SARS-CoV-2 Nsp8 माइटोकॉन्ड्रियल राइबोसोम के साथ भी संपर्क करता है [48]। अधिक से अधिक अध्ययनों से पता चला है कि वायरस माइटोकॉन्ड्रियल गतिशीलता में हेरफेर करके वायरल प्रतिकृति की पारिस्थितिक साइटों को बनाए रखते हैं (चित्र 1)। इसलिए, वायरस और माइटोकॉन्ड्रियल गतिशीलता का अध्ययन वायरल संक्रमण के उपचार के लिए महत्वपूर्ण दवा लक्ष्य बन सकता है।

चित्र 1. वायरल संक्रमण माइटोकॉन्ड्रियल गतिशीलता को बाधित करता है। विभिन्न वायरस माइटोकॉन्ड्रियल संलयन प्रोटीन (एमएफएन, ओपीए1) या विखंडन प्रोटीन (डीआरपी1) के माध्यम से माइटोकॉन्ड्रियल गतिशीलता को प्रभावित करते हैं और कोशिका अस्तित्व और वायरल दृढ़ता को बढ़ाने के लिए क्षतिग्रस्त माइटोकॉन्ड्रिया को साफ करने के लिए माइटोफैगी को प्रेरित करते हैं।
3. वायरल संक्रमण माइटोकॉन्ड्रिया-प्रेरित कोशिका मृत्यु को नियंत्रित करता है

चीनी जड़ी बूटी सिस्टैंच पौधा-एंटीट्यूमर
एपोप्टोसिस आंतरिक वातावरण की स्थिरता को बनाए रखने के लिए, जीन द्वारा नियंत्रित कोशिका स्वायत्तता और क्रमादेशित मृत्यु की प्रक्रिया है। वर्तमान में, सेल एपोप्टोसिस को तीन मार्गों में विभाजित किया जा सकता है। माइटोकॉन्ड्रिया आंतरिक एपोप्टोटिक मार्ग के माध्यम से कोशिका मृत्यु को प्रभावित करते हैं। जब एपोप्टोसिस प्रेरित होता है, तो बीसीएल -2 पारिवारिक प्रोटीन चैनलों का उपयोग करके माइटोकॉन्ड्रियल झिल्ली प्रोटीन सक्रियण माइटोकॉन्ड्रियल बाहरी झिल्ली पारगम्यता को ट्रिगर करता है और साइटोप्लाज्म में एपोप्टोसिस प्रोटीन (जैसे साइट सी, स्मैक, आदि) जारी करता है। साइट सी और एपोप्टोटिक प्रोटीज एक्टिवेटिंग फैक्टर 1 (एपीएएफ1) परस्पर क्रिया करते हैं, एपोप्टोसोम बनाते हैं और प्रोकैस्पेज़ को सक्रिय करते हैं -9, जो कैस्पेज़ को तोड़ता है और कैस्पेज़ को तोड़ता है, इस प्रकार सेल एपोप्टोसिस को प्रेरित करता है [49]। कई वायरस कोशिका मृत्यु को प्रेरित करके या कोशिका मृत्यु को रोककर लगातार संक्रमण बनाए रखकर वायरल प्रसार को बढ़ावा देते हैं। एचसीवी माइटोकॉन्ड्रियल गतिशीलता को बाधित करके सेल एपोप्टोसिस को रोकता है। एचसीवी संक्रमण DRP1Ser616 के फॉस्फोराइलेशन को प्रेरित करता है, जो माइटोकॉन्ड्रियल विखंडन और माइटोफैगी को ट्रिगर करता है, जिससे सेल एपोप्टोसिस बाधित होता है, जो अंततः वायरल दृढ़ता को बढ़ावा देता है [28]। सीएसएफवी संक्रमण एचसीवी संक्रमण के समान है। सीएसएफवी और एचसीवी संक्रमण खराब माइटोकॉन्ड्रिया को साफ करने और प्रो-एपोप्टोटिक प्रोटीन की रिहाई को रोकने के लिए पिंक1 और पार्किन मार्गों को सक्रिय करके माइटोफैगी की घटना को ट्रिगर करता है, जिससे सेल एपोप्टोसिस को रोकता है और वायरल संक्रमण को बनाए रखता है [28,31]। Drp1 साइलेंसिंग माइटोकॉन्ड्रियल विखंडन, माइटोफैगी और एचसीवी और सीएसएफवी द्वारा प्रेरित अप-विनियमित एपोप्टोसिस संकेतों को अवरुद्ध करता है, जिससे विषाणु स्राव कम हो जाता है [28,31]। दिलचस्प बात यह है कि एचसीवी वायरल प्रोटीन एपोप्टोसिस को प्रेरित करने में एक अलग भूमिका निभाते हैं। उदाहरण के लिए, NS4A प्रोटीन माइटोकॉन्ड्रिया के इंट्रासेल्युलर वितरण को बदल देता है, जिससे माइटोकॉन्ड्रियल क्षति होती है और साइटोप्लाज्म में साइट सी की रिहाई होती है, जिससे कैस्पेज़ -3-मध्यस्थ एपोप्टोसिस [50] सक्रिय होता है। E2 प्रोटीन, Huh-7 कोशिकाओं में ट्रांसफ़ेक्ट होकर, Bcl-2 को डाउन-रेगुलेट करता है और Bax को अप-रेगुलेट करता है, जो माइटोकॉन्ड्रियल-डिपेंडेंट कैस्पेज़ पाथवे [51] के माध्यम से एपोप्टोसिस को प्रेरित कर सकता है। 14-3-3ε प्रोटीन के साथ कोर प्रोटीन की अंतःक्रिया एपोप्टोसिस को सक्रिय करने के लिए बैक्स जारी करती है [52]। NS4B माइटोकॉन्ड्रियल झिल्ली क्षमता में कमी का कारण बनता है, कैस्पेज़ 9 को सक्रिय करता है, और साइट सी जारी करता है, माइटोकॉन्ड्रियल मृत्यु पथ के माध्यम से एपोप्टोसिस को प्रेरित करता है [53]। एनएस4ए और एनएस3-4ए प्रोटीन बैक्स को विनियमित करते हैं और माइटोकॉन्ड्रिया में स्थानांतरित हो जाते हैं, एंटी-एपोप्टोटिक प्रोटीन बीसीएल-एक्सएल की अभिव्यक्ति को कम करते हैं और कैस्पेज़ को सक्रिय करते हैं-9, जिससे माइटोकॉन्ड्रियल-मध्यस्थता से मृत्यु होती है। बैक्स और कैस्पेज़ कैस्केड प्रतिक्रिया, जो अंततः कोशिका मृत्यु को प्रेरित करती है [54]। वायरल प्रोटीन के कार्य और तंत्र और वायरल प्रोटीन की गतिविधि को रोकने वाले पदार्थों पर आगे का शोध क्रोनिक हेपेटाइटिस के उपचार और दवा विकास के लिए नए विचार प्रदान कर सकता है। एचबीवी वायरस एपोप्टोसिस को भी प्रेरित करता है। HBx प्रोटीन एकत्रित माइटोकॉन्ड्रियल संरचना में p53 के साथ दृढ़ता से संपर्क कर सकता है, जिससे कोशिका मृत्यु हो सकती है [55]। इसी तरह, DENV पी53-आश्रित माइटोकॉन्ड्रिया-मध्यस्थता एपोप्टोसिस [56] को प्रेरित करता है। बैक्स के साथ जुड़कर, एचबीएक्स बैक्स और एप्सिलॉन के बीच परस्पर क्रिया में हस्तक्षेप करता है, बैक्स के माइटोकॉन्ड्रिया में स्थानांतरण को बढ़ाता है, माइटोकॉन्ड्रियल पारगम्यता संक्रमण छिद्रों के खुलने को नियंत्रित करता है और कैस्पेज़ और साइटोक्रोम सी जारी करता है, और फिर अंतर्जात माइटोकॉन्ड्रियल एपोप्टोसिस की मध्यस्थता [57,58]। एचबीवी एपोप्टोसिस को भी रोकता है और माइटोकॉन्ड्रियल गतिशीलता को बदलकर वायरल संक्रमण को बनाए रखता है। HBx Mfn2 के सर्वव्यापीकरण को प्रेरित कर सकता है, DRP1 की अभिव्यक्ति को बढ़ावा दे सकता है, माइटोकॉन्ड्रियल विखंडन को जन्म दे सकता है, और सेल एपोप्टोसिस को रोकने और सेल अस्तित्व और वायरस के लगातार संक्रमण को बनाए रखने के लिए PINK {53}} पार्किन मार्ग के माध्यम से माइटोफैगी को प्रेरित कर सकता है [37]। इसके अलावा, SARS-CoV कोशिका एपोप्टोसिस को भी प्रेरित कर सकता है। SARS-CoV 3a प्रोटीन माइटोकॉन्ड्रिया से कैस्पेज़ -9 और साइटोक्रोम सी प्रोटीन रिलीज़ को सक्रिय कर सकता है या बाहरी सिग्नल के माध्यम से कैस्पेज़ -8 को सक्रिय कर सकता है और माइटोकॉन्ड्रियल डेथ पाथवे को नियंत्रित करने के लिए बिड सक्रियण का कारण बन सकता है [59]। SARS-CoV N प्रोटीन माइटोकॉन्ड्रियल झिल्ली क्षमता में कमी और ROS और साइटोक्रोम C रिलीज़ में वृद्धि को प्रेरित करता है, जो एपोप्टोसिस में मध्यस्थता करता है [59,60]। इसके अलावा, SARS-CoV M प्रोटीन माइटोकॉन्ड्रियल साइटोक्रोम c प्रोटीन रिलीज़ को प्रेरित करता है, जो कोशिका एपोप्टोसिस में मध्यस्थता करता है [61]। इसी तरह, SARS-CoV-2 3एक प्रोटीन एपोप्टोसिस को प्रेरित कर सकता है [48]। इसके अलावा, वायरस कोशिका मृत्यु को नियंत्रित करके प्रतिकृति और प्रसार को बढ़ावा दे सकते हैं। उदाहरण के लिए, रोटावायरस, रेओविरिडे परिवार से संबंधित एक डबल-स्ट्रैंडेड आरएनए वायरस, एपोप्टोसिस को प्रेरित कर सकता है। हाल के अध्ययनों से पता चला है कि एनएसपी4 माइटोकॉन्ड्रियल झिल्ली प्रोटीन एडेनिन न्यूक्लियोटाइड ट्रांसलोकेटर और वोल्टेज-निर्भर आयन चैनल (वीडीएसी) के साथ बातचीत के माध्यम से माइटोकॉन्ड्रियल झिल्ली क्षमता और माइटोकॉन्ड्रियल पारगम्यता को बदलता है, साइटोक्रोम सी जारी करता है, कैस्पेज़ को सक्रिय करता है, और एपोप्टोसिस सिग्नल को मध्यस्थ करने के लिए विनियमित करता है। कोशिका एपोप्टोसिस [62]। इसके अलावा, रोटावायरस संक्रमण बैक्स की सांद्रता को नियंत्रित कर सकता है और माइटोकॉन्ड्रियल मार्ग के माध्यम से एपोप्टोसिस में मध्यस्थता कर सकता है [63]। दूसरी ओर, रोटावायरस संक्रमण के शुरुआती चरण में, एनएसपी1 पीआई3के/एक्ट सिग्नलिंग मार्ग को सक्रिय करके या पी53 विनियमन को बाधित करके और सेल में वायरस की प्रारंभिक प्रतिकृति सुनिश्चित करके सेल एपोप्टोसिस को रोकता है [64]। रोटावायरस संक्रमण माइटोकॉन्ड्रियल गतिशीलता को विनियमित करके एपोप्टोसिस में भी मध्यस्थता करता है। रोटावायरस संक्रमण के अंतिम चरण में, NSP4 CDK1 के माध्यम से Drp1 के Ser616 फॉस्फोराइलेशन को प्रेरित करता है और माइटोकॉन्ड्रिया में DRP1 की भर्ती में भाग लेता है, माइटोकॉन्ड्रियल विखंडन की मध्यस्थता करता है, Cyt c जारी करता है, और कैस्पेज़ -9 और कैस्पेज़ -3 को सक्रिय करता है। एपोप्टोसिस को प्रेरित करने और वायरस के प्रसार को सुविधाजनक बनाने के लिए [65]। इसी तरह, इन्फ्लूएंजा ए विषाणु कारक पीबी 1- एफ2 आईएमएम को लक्षित करता है जो माइटोकॉन्ड्रियल शिथिलता का कारण बनता है, और अंतर्जात माइटोकॉन्ड्रियल मार्ग के माध्यम से कोशिका मृत्यु को प्रेरित करता है [38,66]। जीका वायरस एक एकल-फंसे हुए सकारात्मक-फंसे हुए आरएनए वायरस है जो जीनस फ्लेविवायरस से संबंधित है, और जीका वायरस संक्रमण माइटोकॉन्ड्रियल ट्रांसमेम्ब्रेन क्षमता को भी कम कर सकता है, एमएफएन 2 की अभिव्यक्ति को कम कर सकता है, और माइटोकॉन्ड्रियल विखंडन को बढ़ावा दे सकता है, जिससे सेल एपोप्टोसिस प्रेरित हो सकता है। माइटोकॉन्ड्रियल डिवीजन इनहिबिटर 1 (Mdivi-1), माइटोकॉन्ड्रिया विखंडन को रोकने वाला एक छोटा अणु, माइटोकॉन्ड्रियल विखंडन को रोकता है और जीका वायरस संक्रमण के बाद माइटोकॉन्ड्रियल गतिशीलता में सुधार करता है, जिससे कोशिका अस्तित्व में वृद्धि होती है [67]। दिलचस्प बात यह है कि वायरस में सेलुलर प्रतिरक्षा से बचने की विभिन्न रणनीतियाँ विकसित हुई हैं। उदाहरण के लिए, वायरस संक्रमण कोशिका एपोप्टोसिस को प्रेरित कर सकता है ताकि बहाव और इसलिए प्रसार हो सके। इसके अलावा, वायरस माइटोफैगी के माध्यम से कोशिका एपोप्टोसिस को रोक सकते हैं, जिससे उनकी प्रतिकृति सुनिश्चित होती है। वर्तमान में, एपोप्टोसिस और ऑटोफैगी के बीच के तंत्र को पूरी तरह से समझा नहीं गया है, लेकिन प्रत्येक प्रक्रिया का विनियमन कोशिकाओं को संतुलित स्थिति में रखता है [68,69]। कई अध्ययनों से पता चला है कि कई वायरस एपोप्टोसिस को रोकने के लिए माइटोफैगी को ट्रिगर करके वायरल संक्रमण को बनाए रख सकते हैं। एचसीवी माइटोफैगी के माध्यम से विखंडन माइटोकॉन्ड्रिया को साफ करता है, जिससे कोशिका एपोप्टोसिस बाधित होता है। डीआरपी61 या पार्किन को शांत करने से साइटोक्रोम सी का स्राव बढ़ सकता है, एपोप्टोसिस सिग्नलिंग में उल्लेखनीय वृद्धि हो सकती है और कैसपेस3 की गतिविधि बढ़ सकती है। इन परिणामों से पता चलता है कि एचसीवी माइटोफैगी [28] के माध्यम से एपोप्टोसिस को कम करके वायरल दृढ़ता को बढ़ावा देता है। पोर्सिन प्रजनन और श्वसन सिंड्रोम (पीआरआरएसवी), आर्टेरिविरिडे परिवार का एक एकल सकारात्मक-स्ट्रैंड आरएनए वायरस, माइटोकॉन्ड्रियल गतिशीलता को बाधित करके, माइटोफैगी को प्रेरित करके और सेल एपोप्टोसिस को रोककर स्व-प्रतिकृति को बढ़ावा दे सकता है [70]। एचबीवी माइटोकॉन्ड्रियल विखंडन और माइटोफैगी अणुओं को प्रेरित करता है, जो माइटोकॉन्ड्रियल विखंडन और माइटोफैगी में मध्यस्थता करता है और वायरस-प्रेरित कोशिका एपोप्टोसिस को कम करता है। माइटोफैगी के उत्पादन में हस्तक्षेप करने से एपोप्टोसिस संकेत बढ़ता है और वायरस प्रतिकृति कम हो जाती है [37]। इसी तरह, न्यूकैसल रोग वायरस (एनडीवी), एक एकल-फंसे नकारात्मक आरएनए वायरस जो पैरामाइक्सोविरिडे परिवार से संबंधित है, पोर्सिन प्रजनन वायरस और सीएसएफवी माइटोफैगी को प्रेरित करके सेल एपोप्टोसिस को रोक सकते हैं, जिससे वायरस संक्रमण को बढ़ावा मिलता है [31,71]। वायरल संक्रमण के संदर्भ में, एपोप्टोसिस माइटोफैगी को कैसे नियंत्रित करता है और एपोप्टोसिस और माइटोफैगी के बीच पारस्परिक विनियमन के आणविक तंत्र को और अध्ययन की आवश्यकता है। निष्कर्ष में, माइटोकॉन्ड्रियल मार्ग के माध्यम से एपोप्टोसिस को प्रेरित करने वाले वायरस स्व-प्रतिकृति के स्थान को बनाए रखते हैं (चित्रा 2)। इसलिए, वायरस-प्रेरित सेल एपोप्टोसिस के विशिष्ट तंत्र में आगे के शोध से विभिन्न वायरस के लिए नई एंटीवायरल दवाओं की सुविधा मिलेगी।
4. वायरल संक्रमण माइटोकॉन्ड्रिया-प्रेरित जन्मजात प्रतिरक्षा को नियंत्रित करता है

पुरुषों के लिए सिस्टैंच के फायदे - प्रतिरक्षा प्रणाली को मजबूत करें
सिस्टैंच इनहांस इम्युनिटी उत्पादों को देखने के लिए यहां क्लिक करें
【अधिक के लिए पूछें】 ईमेल:cindy.xue@wecistanche.com / व्हाट्स ऐप: 0086 18599088692 / वीचैट: 18599088692
जब कोई वायरस कोशिकाओं को संक्रमित करता है, तो मेजबान टीएलआर, आरएलआर और एनएलआर जैसे रोगज़नक़ पहचान रिसेप्टर्स (पीआरआर) के माध्यम से वायरस को पहचानने के लिए जन्मजात प्रतिरक्षा प्रणाली को सक्रिय करता है। यहां, हम माइटोकॉन्ड्रिया-मध्यस्थता वाले आरएलआर सिग्नलिंग मार्ग को विनियमित करने वाले वायरल संक्रमण पर ध्यान केंद्रित करते हैं। कई वायरल रोगज़नक़-संबंधित आणविक पैटर्न (PAMPs) को रेटिनोइक एसिड-इंड्यूसिबल जीन I (RIG-I) और मेलेनोमा विभेदन-संबद्ध जीन 5 (MDA5) द्वारा पहचाना जाता है; RIG-1 और MDA5 गठन संबंधी परिवर्तनों से गुजरते हैं जिसके परिणामस्वरूप CARD डोमेन एक समजात ऑलिगोमर बनाने के लिए उजागर होता है। RIG-1 और MDA5, N-टर्मिनल CARD डोमेन और MAVS के N-टर्मिनल CARD डोमेन के माध्यम से एक-दूसरे को पहचानते हैं और एक-दूसरे से जुड़ते हैं, MAVS प्रियन-जैसे पॉलिमर बनाते हैं और NF-κB और IRF3/ जैसे डाउनस्ट्रीम सिग्नलिंग मार्ग सक्रिय करते हैं। 7, जिससे जन्मजात एंटीवायरल प्रतिक्रिया में शामिल सूजन संबंधी साइटोकिन्स और इंटरफेरॉन की अभिव्यक्ति प्रेरित होती है। एमएवीएस ओएमएम में आरएलआर मार्ग के निर्णायक एडाप्टर प्रोटीन के रूप में स्थित है। एमएवीएस के कार्य इसके माइटोकॉन्ड्रियल स्थानीयकरण पर निर्भर करते हैं, जो पुष्टि करता है कि माइटोकॉन्ड्रिया जन्मजात प्रतिरक्षा सिग्नलिंग मार्ग में एक महत्वपूर्ण भूमिका निभाता है।

चित्र 2. वायरल संक्रमण माइटोकॉन्ड्रिया-प्रेरित कोशिका मृत्यु को नियंत्रित करता है। विभिन्न वायरस बी-सेल लिंफोमा 2 (बीसीएल-2) परिवार के प्रोटीन में मध्यस्थता करते हैं, साइट सी जारी करते हैं, प्रोकैस्पेज़ -9 को सक्रिय करते हैं, और एपोप्टोसोम बनाते हैं, जिससे सेल एपोप्टोसिस उत्पन्न होता है।
अधिक से अधिक अध्ययनों से पता चला है कि वायरस ने मेजबान प्रतिरक्षा प्रणाली से बचने के लिए अपने विकास के दौरान माइटोकॉन्ड्रिया में आरएलआर सिग्नलिंग मार्ग को बाधित करने के लिए रणनीतियों की एक श्रृंखला विकसित की है (चित्रा 3)। SARS-CoV 3b प्रोटीन MAVS गतिविधि को अवरुद्ध करके टाइप I IFN उत्पादन को रोकता है [72]। इसके अलावा, SARS-CoV -2 का Nsp13 प्रोटीन और 9C प्रोटीन MAVS सिग्नल ट्रांसडक्शन के नियमन में शामिल हो सकता है, जिससे जन्मजात प्रतिरक्षा प्रतिक्रिया में मध्यस्थता होती है [48]। हाल के एक अध्ययन से पता चला है कि मानव बृहदान्त्र उपकला कैंसर कोशिकाओं Caco -2 में SARS-CoV -2 संक्रमण के परिणामस्वरूप MAVS की अभिव्यक्ति में कमी आई है [73]। एचसीवी मेजबान प्रतिरक्षा से बच सकता है, जिससे दीर्घकालिक संक्रमण हो सकता है। NS3/4A को माइटोकॉन्ड्रिया में स्थानीयकृत किया जा सकता है और MAVS के साथ जोड़ा जा सकता है। NS3/4A, Cys- 508 पर MAVS को तोड़ देता है, जिससे MAVS का एन-टर्मिनल टुकड़ा माइटोकॉन्ड्रिया से अलग हो जाता है और एक निष्क्रिय टुकड़ा बन जाता है, जो IFN [74,75] के उत्पादन को रोकता है। इसी तरह, बैट हेपेटोवायरस और सेनेका वैली वायरस आरएनए वायरस हैं, दोनों पिकोर्नविरिडे परिवार से संबंधित हैं, जो एमएवी प्रोटीन के साथ बातचीत करके जन्मजात प्रतिरक्षा सिग्नल ट्रांसडक्शन में भी हस्तक्षेप कर सकते हैं, इस प्रकार वायरल संक्रमण को बनाए रख सकते हैं [76,77]। बैट हेपेटोवायरस 3ABC प्रोटीज़ मानव MAVS के साथ संपर्क करते हैं और IRF3 और NF-κB की सक्रियता को रोकने के लिए MAVS को ग्लू463/ग्लाइ464 पर विभाजित करते हैं, जिससे मानव कोशिकाओं में टाइप I इंटरफेरॉन का उत्पादन अवरुद्ध हो जाता है [76]। सेनेका वैली वायरस 3C प्रोटीज़, Q148 पर MAVS को तोड़ने के लिए अपनी प्रोटीज़ गतिविधि पर निर्भर करता है, जिससे टाइप I इंटरफेरॉन [77] बाधित होता है। इसके अलावा, वायरस प्रोटीसोम मार्ग के माध्यम से एमएवीएस को भी ख़राब कर सकता है और आरएलआर सिग्नलिंग मार्ग को अवरुद्ध कर सकता है। उदाहरण के लिए, एचबीवी एचबीएक्स प्रोटीन एमएवीएस के साथ बातचीत कर सकता है, एमएवीएस के सर्वव्यापीकरण और गिरावट को बढ़ावा दे सकता है, और आरआईजी-आई-एमडीए5 मार्ग को रोक सकता है, जो एक साथ आईएफएन- [78] के उत्पादन को कम कर देता है। एनडीवी वी प्रोटीन आईएफएन उत्पादन को रोकने के लिए प्रोटीसोमल मार्ग के माध्यम से एमएवीएस गिरावट में मध्यस्थता करने के लिए ई 3 यूबिकिटिन लिगेज आरएनएफ 5 को भर्ती करता है [79]। रोटावायरस VP3 प्रोटीन माइटोकॉन्ड्रिया को लक्षित करता है और MAVS के प्रोलाइन-समृद्ध क्षेत्र में SPLTSS मोटिफ के फॉस्फोराइलेशन में मध्यस्थता करता है, जिससे MAVS प्रोटीसोम मार्ग के माध्यम से ख़राब हो जाता है, जिससे आंतों के उपकला कोशिकाओं के रोटावायरस संक्रमण के दौरान IFN- का उत्पादन अवरुद्ध हो जाता है [80]। वायरस MAVS को RIG-1 और MDA5 से जोड़ने को अवरुद्ध करके आरएलआर सिग्नलिंग मार्ग को भी बाधित करते हैं। बाइंडिंग मोटिफ से जुड़कर, ज़िका वायरस एनएस3 आरआईजी-1 और एमडीए5 को माइटोकॉन्ड्रिया में ले जाने से रोकता है, जिससे आरएलआर सिग्नलिंग मार्ग [81] द्वारा मध्यस्थ इंटरफेरॉन उत्पादन अवरुद्ध हो जाता है। DENV NS4A, MAVS के एन-टर्मिनल कार्ड-लाइक (CL) डोमेन और C-टर्मिनल ट्रांसमेम्ब्रेन (TM) डोमेन से जुड़ता है, जो MAVS को RIG-I से जुड़ने से रोकता है और इंटरफेरॉन के उत्पादन को रोकता है [82]। वायरस आरएलआर सिग्नलिंग मार्गों को अवरुद्ध करने के लिए पोस्ट-ट्रांसक्रिप्शनल विनियमन के माध्यम से मेजबान प्रतिरक्षा प्रणाली की एक श्रृंखला को विनियमित करके, माइक्रोआरएनए में हेरफेर करके मेजबान की जन्मजात प्रतिरक्षा से भी बच सकते हैं। वेसिकुलर स्टामाटाइटिस वायरस (वीएसवी), रबविरिडे परिवार का एक एकल-फंसे नकारात्मक आरएनए (एसएसआरएनए) वायरस, संक्रमण आईआरएफ3 के माध्यम से एमआईआर {{59}पी को प्रेरित करता है और प्रकार I अभिव्यक्ति इंटरफेरॉन को कम करने और अत्यधिक सूजन से बचने के लिए एमएवीएस और टीआरएएफ 3 एमआरएनए को नियंत्रित करता है [ 83]। रबडोवायरस कई क्रोकर मैक्रोफेज को संक्रमित करता है, एमआईआर -3570 अभिव्यक्ति को प्रेरित करता है और एमएवीएस अभिव्यक्ति को लक्षित और दबाता है, इस प्रकार वायरस को बढ़ावा देता है [84]। अध्ययनों से पता चला है कि वायरल संक्रमण से प्रेरित एमआईआरबी और एमआईआर{66}} एस्पार्टेट ग्लूटामेट ट्रांसपोर्टर एसएलसी25ए12 के माध्यम से कोशिका कार्य और माइटोकॉन्ड्रियल चयापचय में हेरफेर कर सकते हैं, जिससे एंटीवायरल वायरस के लिए एमएवीएस-मध्यस्थता वाली जन्मजात प्रतिरक्षा ख़राब हो सकती है [85]। दिलचस्प बात यह है कि कोशिकाओं में miR{71}}b और miR{72}} की नकल पेश करने से NADH का स्तर कम हो सकता है, जिसके परिणामस्वरूप NAD/NADH अनुपात में 50% तक की वृद्धि हो सकती है, माइटोकॉन्ड्रियल ऑक्सीजन की खपत में कमी आ सकती है। , और अंततः साइट्रिक एसिड चक्र से चीनी पाचन तक सेलुलर चयापचय मार्गों में परिवर्तन, जबकि लैक्टेट की सामग्री में वृद्धि [85]। नवीनतम शोध से पता चलता है कि हेपेटाइटिस बी वायरस संक्रमण एमएवीएस को माइटोकॉन्ड्रियल एकत्रीकरण और स्थानीयकरण से रोकने के लिए लैक्टेट डिहाइड्रोजनेज-निर्भर लैक्टिक एसिड के माध्यम से सीधे एमएवीएस से जुड़ता है, जिससे आरएलआर सिग्नलिंग मार्ग [86] अवरुद्ध हो जाता है। चूंकि लैक्टिक एसिड बछड़े की मध्यस्थता वाली जन्मजात प्रतिरक्षा प्रतिक्रिया में एक नकारात्मक नियामक भूमिका निभाता है [87], ये दो miRNAs लैक्टिक एसिड विनियमन के माध्यम से जन्मजात प्रतिरक्षा को प्रभावित कर सकते हैं।
5. वायरल संक्रमण माइटोकॉन्ड्रियल मेटाबॉलिज्म को नियंत्रित करता है
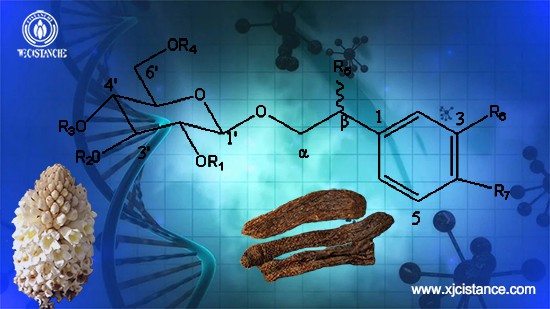
फेनिलथेनॉल ग्लाइकोसाइड सिस्टैंच डेजर्टिकोला का मुख्य सक्रिय घटक है
माइटोकॉन्ड्रिया कोशिकाओं के ऊर्जा चयापचय केंद्र हैं; वे कार्बोहाइड्रेट, अमीनो एसिड और फैटी एसिड के मैक्रोमोलेक्यूलर चयापचय को विनियमित करके एटीपी का उत्पादन करते हैं। कोशिका का मुख्य ऊर्जा स्रोत एटीपी अणु द्वारा एडेनोसिन डिफॉस्फेट (एडीपी) अणु में डिफॉस्फोराइलेट किया जाता है। इस प्रक्रिया को जारी रखने के लिए, कोशिकाओं को ग्लाइकोलाइसिस, ट्राईकार्बोक्सिलिक एसिड चक्र और ऑक्सीडेटिव फॉस्फोराइलेशन जैसे मार्गों के माध्यम से कुछ मैक्रोमोलेक्यूलर मेटाबोलाइट्स को तोड़ने की आवश्यकता होती है। ग्लूकोज कोशिकाओं के लिए ऊर्जा का प्राथमिक स्रोत है। साइटोप्लाज्म में, एटीपी के दो अणु ग्लूकोज के एक अणु से ग्लाइकोलाइसिस द्वारा निर्मित होते हैं, जिससे दो पाइरूवेट अणु उत्पन्न होते हैं। एटीपी उत्पादन को अनुकूलित करने के लिए, कोशिकाएं ऑक्सीडेटिव फॉस्फोराइलेशन (ओएक्सपीएचओएस) से गुजरती हैं, जो ट्राईकार्बोक्सिलिक एसिड चक्र के साथ माइटोकॉन्ड्रियल पाइरूवेट वाहक (एमपीसी) के माध्यम से पाइरूवेट को माइटोकॉन्ड्रियल मैट्रिक्स में ऑक्सीकरण करती है। अंत में, माइटोकॉन्ड्रियल इलेक्ट्रॉन परिवहन श्रृंखला के माध्यम से एक ग्लूकोज अणु का पूर्ण ऑक्सीकरण 36 एटीपी अणु उत्पन्न करता है। हालांकि ऑक्सीडेटिव फॉस्फोराइलेशन उच्च ऊर्जा दक्षता पैदा करता है, यह एक धीमी प्रक्रिया है और तेजी से विभाजित होने वाली कोशिकाओं, जैसे सक्रिय प्रतिरक्षा कोशिकाओं या कैंसर कोशिकाओं की ऊर्जा आवश्यकताओं को पूरा नहीं कर सकती है। इसलिए, इन कोशिकाओं को अपनी गतिविधि बनाए रखने के लिए तेजी से ऊर्जा उत्पन्न करने के लिए एरोबिक ग्लाइकोलाइसिस (जिसे वारबर्ग प्रभाव भी कहा जाता है) शुरू करने की आवश्यकता होती है। इसके अलावा, भुखमरी और आपातकाल के दौरान, लाइपेज लिपिड को मुक्त फैटी एसिड में बदल देता है, जो फैटी एसिड ऑक्सीकरण के लिए माइटोकॉन्ड्रिया में प्रवेश करता है, इस प्रकार सेलुलर ऊर्जा चयापचय का संतुलन बनाए रखता है।

चित्र 3. वायरल संक्रमण माइटोकॉन्ड्रिया-प्रेरित जन्मजात प्रतिरक्षा को नियंत्रित करता है। वायरस कोशिका पर आक्रमण करने के बाद, आरएलआर वायरल आरएनए को पहचानते हैं और एंटीवायरल सिग्नल मार्ग को सक्रिय करने के लिए माइटोकॉन्ड्रियल एंटीवायरल सिग्नल (एमएवीएस) के साथ बातचीत करते हैं। विभिन्न वायरस आरएलआर सिग्नलिंग मार्ग को अवरुद्ध करके मेजबान की जन्मजात प्रतिरक्षा से बचते हैं।
कई वायरस इंट्रासेल्युलर अस्तित्व को बढ़ाने के लिए मेजबान सेल चयापचय को सक्रिय रूप से दोबारा आकार दे सकते हैं। एचसीवी संक्रमण कोशिका चयापचय में परिवर्तन का कारण बनता है, जो ग्लाइकोलाइसिस के दौरान कार्बोहाइड्रेट प्रवाह को बढ़ाता है और एरोबिक ऑक्सीडेटिव फास्फारिलीकरण और साइट्रिक एसिड चक्र की गतिविधियों को कम करता है, जो संक्रमण के बाद कुछ दिनों या हफ्तों के भीतर कोशिका को वारबर्ग प्रभाव की ओर बहुत तेजी से निर्देशित कर सकता है। एक सेल [88–90]। हाल के एक अध्ययन में, माइटोकॉन्ड्रियल श्वसन श्रृंखला परिसर के कुछ महत्वपूर्ण घटकों को एचसीवी संक्रमण के छह दिन बाद डाउन-रेगुलेट पाया गया, जिसमें एमटी-एनडी1, एमटी-एनडी3, एमटी-एनडी4, एमटी-एनडी4एल और एमटी-सीओ2 शामिल हैं। ]. इसके अलावा, एचसीवी-संक्रमित सीडी8+टी कोशिका चक्र [92,93] में एमटीएनडी, सीओएक्स और एफ0/एफ1एटीपी सिंथेज़ का डाउन-रेगुलेशन पाया गया। यह दिखाया गया है कि एचसीवी माइटोकॉन्ड्रियल श्वसन श्रृंखला परिसर की अभिव्यक्ति को बदलकर ऑक्सीडेटिव फास्फारिलीकरण की गतिविधि को व्यवस्थित रूप से सीमित करता है [94]। एचआईएफ -1 और प्रोटो-ओन्कोजीन सी-माइसी एचसीवी-संक्रमित कोशिकाओं में महत्वपूर्ण रूप से व्यक्त होते हैं, जो ग्लूकोकाइनेज (जीके), फॉस्फोग्लुकोज -1 (पीएफके {27} सहित कई ग्लाइकोलाइटिक प्रमुख एंजाइमों की अभिव्यक्ति को प्रेरित करते हैं। }), और पाइरूवेट काइनेज (पीके) [95-97]। इसके अलावा, एचसीवी संक्रमण हेक्सोकिनेस 2 अभिव्यक्ति के अपनियमन को प्रेरित करता है और एचसीवी प्रोटीन एनएस5ए [98] के साथ बातचीत के माध्यम से हेक्सोकिनेस गतिविधि को बढ़ाता है। DENV संक्रमण ग्लूकोज ट्रांसपोर्टर 1 और हेक्सोकाइनेज 2 [99] के अपग्रेडेशन को भी प्रेरित करता है। ग्लाइकोलाइटिक मार्ग के अवरोध ने DENV के RNA संश्लेषण और संक्रामक विषाणुओं के उत्पादन को काफी कम कर दिया, जिससे पता चला कि DENV अपनी प्रतिकृति को बनाए रखने के लिए सेलुलर ग्लाइकोलाइसिस को फिर से तैयार कर सकता है [99]। दिलचस्प बात यह है कि DENV प्रोटीन का मेजबान चयापचय पर अलग-अलग प्रभाव पड़ता है। DENV NS1 प्रोटीन GADPH की ग्लाइकोलाइटिक गतिविधि को बढ़ाने के लिए GAPDH के साथ इंटरैक्ट करता है [100]। हालाँकि, GAPDH के साथ DENV NS3 प्रोटीन की परस्पर क्रिया के परिणामस्वरूप GAPDH ग्लाइकोलाइसिस गतिविधि कम हो गई [101]। एचसीवी और डीईएनवी संक्रमण कोशिका चयापचय को नया आकार दे सकते हैं, माइटोकॉन्ड्रियल फैटी एसिड ऑक्सीकरण को बढ़ा सकते हैं और ऊर्जा प्रदान कर सकते हैं [102-104]। इस बीच, माइटोकॉन्ड्रिया में फैटी एसिड परिवहन का अवरोध और -ऑक्सीकरण का विनियमन वायरल प्रतिकृति को प्रभावित कर सकता है [103]। ज़िका वायरस मेजबान संसाधनों का उपयोग कर सकता है और विभिन्न चयापचय मार्गों में कोशिका की स्थिति को विनियमित करने के लिए विभिन्न कोशिकाओं में कोशिका चयापचय को पुन: प्रोग्राम कर सकता है, जिससे इसकी स्व-प्रतिकृति की सुविधा मिलती है [105-108]। एचआईवी सीडी 4+ टी कोशिकाओं में प्रतिकृति बनाता है और ऑक्सीडेटिव फास्फारिलीकरण से एरोबिक ग्लाइकोलाइसिस तक चयापचय पुन: प्रोग्रामिंग की ओर ले जाता है [109]। एचआईवी संक्रमण ग्लूकोज ट्रांसपोर्टर की वृद्धि को प्रेरित करता है, अधिक ग्लूकोज ग्रहण करता है, और ग्लाइकोलाइटिक एंजाइम लैक्टेट डीहाइड्रोजनेज ए (एलडीएचए) हेक्सोकाइनेज को बढ़ाता है, इस प्रकार एरोबिक ग्लाइकोलाइसिस को सक्रिय करता है, जो इसके लिए अनुकूल है। एचआईवी रिवर्स ट्रांसक्रिप्शन, एकीकरण, और विषाणु उत्पादन [110-113]। एरोबिक ग्लाइकोलाइसिस को बढ़ाने के अलावा, एचआईवी संक्रमित सीडी 4+ टी कोशिकाएं ग्लूटामाइन चयापचय का कारण बन सकती हैं और उत्पादक एचआईवी संक्रमण के दौरान ग्लूटामाइन का पुन: उपयोग कर सकती हैं [114,115]। प्राथमिक ऊर्जा स्रोतों के रूप में ग्लूकोज और ग्लूटामाइन के अलावा, एचआईवी सीडी {59}} टी कोशिकाओं [115] को संक्रमित करने के लिए ऊर्जा स्रोत के रूप में फैटी एसिड ऑक्सीकरण का भी उपयोग करता है। एक हालिया अध्ययन से पता चला है कि एचआईवी संक्रमण एरोबिक ग्लाइकोलाइसिस को प्रेरित करता है, जो संक्रामकता बनाए रखने के लिए कणों में पैक किए गए कारकों को नियंत्रित करके वायरस की गुणवत्ता को नियंत्रित करने में मदद करता है [116]। यद्यपि माइटोकॉन्ड्रियल चयापचय का वायरल संक्रमण से गहरा संबंध है, लेकिन वह तंत्र जिसके द्वारा वायरस माइटोकॉन्ड्रियल चयापचय को लक्षित करते हैं और वायरस कोशिका चयापचय द्वारा उत्पादित ऊर्जा का उपयोग कैसे करते हैं, यह अभी भी स्पष्ट नहीं है।
6. समापन टिप्पणियाँ
पिछले कुछ दशकों में, माइटोकॉन्ड्रिया को वायरल संक्रमण और मेजबान जन्मजात प्रतिरक्षा में महत्वपूर्ण भूमिका निभाते हुए दिखाया गया है; हालाँकि, होस्ट-वायरस इंटरैक्शन में माइटोकॉन्ड्रिया की भूमिका का और अध्ययन करने की आवश्यकता है। वायरल संक्रमण माइटोकॉन्ड्रियल फ़ंक्शन में हेरफेर करके अपने लिए एक व्यवहार्य पारिस्थितिक स्थान बना सकते हैं। वायरस माइटोकॉन्ड्रिया-प्रेरित कोशिका मृत्यु और माइटोकॉन्ड्रिया-मध्यस्थता वाली जन्मजात प्रतिरक्षा प्रणाली को प्रेरित करता है ताकि माइटोकॉन्ड्रियल गतिशीलता को विनियमित करके इसकी प्रतिकृति और संचरण को सुविधाजनक बनाया जा सके। हाल के वर्षों में, कोशिका चयापचय के नियामक केंद्र के रूप में माइटोकॉन्ड्रिया की भूमिका ने अधिक ध्यान आकर्षित किया है। वायरस कोशिका चयापचय में हेरफेर कर सकते हैं, चयापचय मार्गों को पुन: प्रोग्राम कर सकते हैं, और कोशिकाओं में वायरल निशानों को बनाए रखने के लिए चयापचयों का पुन: उपयोग कर सकते हैं। हालाँकि, माइटोकॉन्ड्रिया और उनके चयापचय पर शोध अभी भी प्रारंभिक अवस्था में है। उन तंत्रों की गहराई में जाना जिनके द्वारा वायरस संक्रमण को बनाए रखने के लिए माइटोकॉन्ड्रिया-मध्यस्थता वाले कोशिका चयापचय का उपयोग करते हैं, भविष्य के शोध के लिए एक रोमांचक क्षेत्र है।
संदर्भ
1. किरियामा, वाई.; नोची, एच. माइटोकॉन्ड्रिया के इंट्रा- और इंटरसेलुलर गुणवत्ता नियंत्रण तंत्र। सेल 2017, 7, 1. [क्रॉसरेफ] [पबमेड]
2. हेल्स, केजी; फुलर, एमटी विकासात्मक रूप से विनियमित माइटोकॉन्ड्रियल संलयन एक संरक्षित, उपन्यास, पूर्वानुमानित GTPase द्वारा मध्यस्थता करता है। सेल 1997, 90, 121-129। [क्रॉसरेफ]
3. चेन, एच.; डेटमर, एसए; इवाल्ड, ए.जे.; ग्रिफिन, ईई; फ़्रेज़र, एसई; चैन, डीसी मिटोफ्यूसिन्स एमएफएन1 और एमएफएन2 माइटोकॉन्ड्रियल संलयन को समन्वित रूप से नियंत्रित करते हैं और भ्रूण के विकास के लिए आवश्यक हैं। जे. सेल बायोल. 2003, 160, 189-200। [क्रॉसरेफ]
4. चेन, एच.; चोमिन, ए.; चान, डीसी संलयन के विघटन के परिणामस्वरूप माइटोकॉन्ड्रियल विविधता और शिथिलता होती है। जे. बायोल. रसायन. 2005, 280, 26185-26192। [क्रॉसरेफ]
5. सिपोलाट, एस.; मार्टिंस डी ब्रिटो, ओ.; दाल ज़िलियो, बी.; स्कोरानो, एल. ओपीए1 को माइटोकॉन्ड्रियल संलयन को बढ़ावा देने के लिए माइटोफ्यूसिन 1 की आवश्यकता होती है। प्रोक. नेटल. अकाद. विज्ञान. यूएसए 2004, 101, 15927-15932। [क्रॉसरेफ] [पबमेड]
6. कोशिबा, टी.; डेटमर, एसए; कैसर, जेटी; चेन, एच.; मैककैफ़री, जेएम; चैन, डीसी माइटोफुसिन कॉम्प्लेक्स द्वारा माइटोकॉन्ड्रियल टेथरिंग का संरचनात्मक आधार। विज्ञान 2004, 305, 858–862। [क्रॉसरेफ]
7. काओ, वाईएल; मेंग, एस.; चेन, वाई.; फेंग, जेएक्स; गु, डीडी; यू, बी.; ली, वाईजे; यांग, जेवाई; लियाओ, एस.; चान, डीसी; और अन्य। एमएफएन1 संरचनाएं माइटोकॉन्ड्रियल संलयन के लिए महत्वपूर्ण न्यूक्लियोटाइड-ट्रिगर डिमराइजेशन को प्रकट करती हैं। प्रकृति 2017, 542, 372-376। [क्रॉसरेफ]
8. ओटेरा, एच.; मिहारा, के. माइटोकॉन्ड्रियल गतिशीलता के आणविक तंत्र और शारीरिक कार्य। जे. बायोकेम. 2011, 149, 241-251। [क्रॉसरेफ]
9. रोजो, एम.; लेग्रोस, एफ.; चेटो, डी.; लोम्बेस, ए. मेम्ब्रेन टोपोलॉजी और माइटोफ्यूसिन्स का माइटोकॉन्ड्रियल लक्ष्यीकरण, ट्रांसमेम्ब्रेन के सर्वव्यापी स्तनधारी होमोलॉग। जे. सेल विज्ञान. GTPase Fzo. 2002, 115, 1663-1674।
10. आनंद, आर.; इंतज़ार।; बेकर, एमजे; क्लैड्ट, एन.; शॉस, ए.सी.; रुगर्ली, ई.; लैंगर, टी. आई-एएए प्रोटीज़ YME1L और OMA1 माइटोकॉन्ड्रियल संलयन और विखंडन को संतुलित करने के लिए OPA1 को तोड़ते हैं। जे. सेल बायोल. 2014, 204, 919-929। [क्रॉसरेफ] [पबमेड]
11. टोंडेरा, डी.; ग्रैंडेमेंज, एस.; जर्डेन, ए.; कार्बोव्स्की, एम.; मैटेनबर्गर, वाई.; हर्ज़िग, एस.; दा क्रूज़, एस.; क्लर्क, पी.; रश्के, आई.; मर्कविर्थ, सी.; और अन्य। तनाव-प्रेरित माइटोकॉन्ड्रियल हाइपरफ्यूज़न के लिए एसएलपी-2 आवश्यक है। ईएमबीओ जे. 2009, 28, 1589-1600। [क्रॉसरेफ] [पबमेड]
12. इंगरमैन, ई.; पर्किन्स, ईएम; मैरिनो, एम.; मियर्स, जेए; मैककैफ़री, जेएम; हिंसाव, जेई; नुन्नारी, जे. डीएनएम1 सर्पिल बनाता है जो संरचनात्मक रूप से फ़िफ़िट माइटोकॉन्ड्रिया के अनुरूप होता है। जे. सेल बायोल. 2005, 170, 1021-1027। [क्रॉसरेफ]
13. जी, डब्ल्यूके; हैच, एएल; मेरिल, आरए; स्ट्रैक, एस.; हिग्स, एचएन एक्टिन फिलामेंट्स डायनेमिन GTPase Drp1 की माइटोकॉन्ड्रियल विखंडन साइटों पर ऑलिगोमेरिक परिपक्वता को लक्षित करते हैं। ईलाइफ 2015, 4, ई11553। [क्रॉसरेफ] [पबमेड]
14. तागुची, एन.; इशिहारा, एन.; जोफुकु, ए.; ओका, टी.; मिहारा, के. डायनामिन-संबंधित GTPase Drp1 का माइटोटिक फॉस्फोराइलेशन माइटोकॉन्ड्रियल विखंडन में भाग लेता है। जे. बायोल. रसायन. 2007, 282, 11521-11529। [क्रॉसरेफ] [पबमेड]
15. सैटो, टी.; नाह, जे.; ओका, एसआई; मुकाई, आर.; मोंडेन, वाई.; मेजिमा, वाई.; इकेदा, वाई.; स्किअरेटा, एस.; लियू, टी.; ली, एच.; और अन्य। Rab9 द्वारा मध्यस्थता वाला एक वैकल्पिक माइटोफैगी मार्ग हृदय को इस्केमिया से बचाता है। जे. क्लिन. जांच। 2019, 129, 802-819। [क्रॉसरेफ]
16. चांग, सीआर; ब्लैकस्टोन, सी. Drp1 का चक्रीय एएमपी-निर्भर प्रोटीन काइनेज फॉस्फोराइलेशन इसकी GTPase गतिविधि और माइटोकॉन्ड्रियल आकृति विज्ञान को नियंत्रित करता है। जे. बायोल. रसायन. 2007, 282, 21583-21587। [क्रॉसरेफ] [पबमेड]
17. रिक्टर, वी.; सिंह, एपी; क्वांसाकुल, एम.; रयान, एमटी; ओसेलामे, एलडी पावरहाउस को विभाजित करना: माइटोकॉन्ड्रियल विखंडन के तंत्र में संरचनात्मक अंतर्दृष्टि। सेल मोल. जीवन विज्ञान. 2015, 72, 3695-3707। [क्रॉसरेफ]
18. यूं, वाई.; क्रुएगर, ईडब्ल्यू; ओसवाल्ड, बी.जे.; मैकनिवेन, एमए माइटोकॉन्ड्रियल प्रोटीन hFis1 डायनामिन जैसे प्रोटीन DLP1 के साथ बातचीत के माध्यम से स्तनधारी कोशिकाओं में माइटोकॉन्ड्रियल विखंडन को नियंत्रित करता है। मोल. सेल बायोल. 2003, 23, 5409-5420। [क्रॉसरेफ]
19. ओटेरा, एच.; वांग, सी.; क्लेलैंड, एमएम; सेतोगुची, के.; योकोटा, एस.; यूले, आरजे; मिहारा, के. एमएफएफ स्तनधारी कोशिकाओं में माइटोकॉन्ड्रियल विखंडन के दौरान Drp1 की माइटोकॉन्ड्रियल भर्ती के लिए एक आवश्यक कारक है। जे. सेल बायोल. 2010, 191, 1141-1158। [क्रॉसरेफ]
20. यू, आर.; जिन, एसबी; लेंडाहल, यू.; निस्टर, एम.; झाओ, जे. ह्यूमन Fis1 संलयन मशीनरी के निषेध के माध्यम से माइटोकॉन्ड्रियल गतिशीलता को नियंत्रित करता है। ईएमबीओ जे. 2019, 38, ई99748। [क्रॉसरेफ]
21. पामर, सीएस; ओसेलामे, एलडी; लाइन, डी.; कौट्सोपोलोस, ओएस; फ्रेज़ियर, एई; रयान, एमटी MiD49 और MiD51, माइटोकॉन्ड्रियल विखंडन मशीनरी के नए घटक। ईएमबीओ प्रतिनिधि 2011, 12, 565-573। [क्रॉसरेफ]
22. झाओ, जे.; लियू, टी.; जिन, एस.; वांग, एक्स.; क्यू, एम.; उहलेन, पी.; टोमिलिन, एन.; शुप्लियाकोव, ओ.; लेंडाहल, यू.; निस्टर, एम. ह्यूमन MIEF1 माइटोकॉन्ड्रियल बाहरी झिल्ली में Drp1 की भर्ती करता है और विखंडन के बजाय माइटोकॉन्ड्रियल संलयन को बढ़ावा देता है। ईएमबीओ जे. 2011, 30, 2762-2778। [क्रॉसरेफ]
23. बारबेरो, जी.; डि लोरेंजो, जी.; अस्ति, ए.; रिबर्सानी, एम.; बेलोनी, जी.; ग्रेगोरियो, बी.; फ़िलिस, जी.; बार्बरिनी, जी. क्रोनिक हेपेटाइटिस सी के रोगियों में हेपैटोसेलुलर माइटोकॉन्ड्रियल परिवर्तन: अल्ट्रास्ट्रक्चरल और जैव रासायनिक निष्कर्ष। पूर्वाह्न। जे. गैस्ट्रोएंटेरोल. 1999, 94, 2198-2205। [क्रॉसरेफ]
24. श्वेर, बी.; रेन, एस.; पीट्स्चमैन, टी.; कार्टेनबेक, जे.; केहल्के, के.; बार्टेंस्क्लेगर, आर.; येन, टीएस; ओट, एम. एक नवीन सी-टर्मिनल स्थानीयकरण रूपांकन के माध्यम से माइटोकॉन्ड्रिया में हेपेटाइटिस सी वायरस कोर प्रोटीन का लक्ष्यीकरण। जे. विरोल. 2004, 78, 7958-7968। [क्रॉसरेफ] [पबमेड]
25. कोरेनागा, एम.; वांग, टी.; ली, वाई.; शोवाल्टर, एलए; चान, टी.; सन, जे.; वेनमैन, एसए हेपेटाइटिस सी वायरस कोर प्रोटीन माइटोकॉन्ड्रियल इलेक्ट्रॉन परिवहन को रोकता है और प्रतिक्रियाशील ऑक्सीजन प्रजातियों (आरओएस) उत्पादन को बढ़ाता है। जे. बायोल. रसायन. 2005, 280, 37481-37488। [क्रॉसरेफ] [पबमेड]
26. माचिदा, के.; चेंग, केटी; लाई, सीके; जेंग, केएस; सुंग, वीएम; लाई, एमएम हेपेटाइटिस सी वायरस प्रतिक्रियाशील ऑक्सीजन प्रजातियों के उत्पादन के साथ माइटोकॉन्ड्रियल पारगम्यता संक्रमण को ट्रिगर करता है, जिससे डीएनए क्षति और STAT3 सक्रियण होता है। जे. विरोल. 2006, 80, 7199-7207। [क्रॉसरेफ] [पबमेड]
27. वांग, टी.; कैंपबेल, आर.वी.; यी, एमके; नींबू, एसएम; वेनमैन, एसए वायरल-प्रेरित माइटोकॉन्ड्रियल डिसफंक्शन में हेपेटाइटिस सी वायरस कोर प्रोटीन की भूमिका। जे. वायरल. हेपत. 2010, 17, 784-793। [क्रॉसरेफ]
28. किम, एसजे; सैयद, जीएच; खान, एम.; चिउ, डब्ल्यूडब्ल्यू; सोहेल, एमए; गिश, आरजी; सिद्दीकी, ए. हेपेटाइटिस सी वायरस माइटोकॉन्ड्रियल विखंडन को ट्रिगर करता है और वायरल दृढ़ता को बढ़ावा देने के लिए एपोप्टोसिस को कमजोर करता है। प्रोक. नेटल. अकाद. विज्ञान. यूएसए 2014, 111, 6413-6418। [क्रॉसरेफ]
29. सिउ, जीके; झोउ, एफ.; यू, एमके; झांग, एल.; वांग, टी.; लियांग, वाई.; चेन, वाई.; चान, एचसी; यू, एस. हेपेटाइटिस सी वायरस एनएस5ए प्रोटीन माइटोकॉन्ड्रियल विखंडन को प्रेरित करने के लिए फॉस्फेटिडिलिनोसिटॉल 4-किनेज III के साथ सहयोग करता है। विज्ञान. प्रतिनिधि 2016, 6, 23464। [क्रॉसरेफ]
30. हारा, वाई.; यानाटोरी, आई.; इकेदा, एम.; कियोकेज, ई.; निशिना, एस.; टोमियामा, वाई.; टोएडा, के.; किशी, एफ.; काटो, एन.; इमामुरा, एम.; और अन्य। हेपेटाइटिस सी वायरस कोर प्रोटीन माइटोकॉन्ड्रियल विध्रुवण के संदर्भ में पार्किन के साथ बातचीत करके माइटोफैगी को दबा देता है। पूर्वाह्न। जे. पैथोल. 2014, 184, 3026-3039। [क्रॉसरेफ]
31. गौ, एच.; झाओ, एम.; जू, एच.; युआन, जे.; वह, डब्ल्यू.; झू, एम.; डिंग, एच.; यी, एल.; चेन, जे. सीएसएफवी ने एपोप्टोसिस को रोकने के लिए माइटोकॉन्ड्रियल विखंडन और माइटोफैगी को प्रेरित किया। ऑनकोटारगेट 2017, 8, 39382-39400। [क्रॉसरेफ]
32. फैन, एस.; वू, के.; झाओ, एम.; युआन, जे.; मा, एस.; झू, ई.; चेन, वाई.; डिंग, एच.; यी, एल.; चेन, जे. एलडीएचबी निषेध माइटोफैगी को प्रेरित करता है और सीएसएफवी संक्रमण की प्रगति को सुविधाजनक बनाता है। ऑटोफैगी 2020, 16, 1-20। [क्रॉसरेफ] [पबमेड]
33. झी, बी.; झाओ, एम.; सॉन्ग, डी.; वू, के.; यी, एल.; ली, डब्ल्यू.; ली, एक्स.; वांग, के.; चेन, जे. सीएसएफवी द्वारा ऑटोफैगी का प्रेरण और टाइप I आईएफएन स्राव का दमन। ऑटोफैगी 2020, 16, 1-23। [क्रॉसरेफ]
34. बार्बियर, वी.; लैंग, डी.; वालोइस, एस.; रोथमैन, एएल; मेडिन, सीएल डेंगू वायरस डीआरपी ट्रिगर माइटोकॉन्ड्रियल विखंडन की हानि के माध्यम से माइटोकॉन्ड्रियल बढ़ाव को प्रेरित करता है। वायरोलॉजी 2017, 500, 149-160। [क्रॉसरेफ]
35. यू, सीवाई; लियांग, जे जे; ली, जेके; ली, वाईएल; चांग, बीएल; सु, सीआई; हुआंग, डब्ल्यूजे; लाइ, एमएम; लिन, वाईएल डेंगू वायरस मिटोफ्यूसिन्स को तोड़कर माइटोकॉन्ड्रियल फ्यूजन को खराब कर देता है। PLoS पैथोग. 2015, 11, ई1005350। [क्रॉसरेफ]
36. यू, वाईएस; पार्क, वाईजे; ली, एचएस; ओन्ह, एनटीके; चो, मेरा; हेओ, जे.; ली, ईएस; चो, एच.; पार्क, YY; चो, एच. माइटोकॉन्ड्रिया यूबिकिटिन लिगेज, मार्च 5 यकृत रोगजनन में हेपेटाइटिस बी वायरस एक्स प्रोटीन समुच्चय का समाधान करता है। कोशिका मृत्यु डिस. 2019, 10, 938. [क्रॉसरेफ] [पबमेड]
37. किम, एसजे; खान, एम.; क्वान, जे.; टिल, ए.; सुब्रमणि, एस.; सिद्दीकी, ए. हेपेटाइटिस बी वायरस माइटोकॉन्ड्रियल गतिशीलता को बाधित करता है: एपोप्टोसिस को कम करने के लिए विखंडन और माइटोफैगी को प्रेरित करता है। PLoS पैथोग. 2013, 9, ई1003722। [क्रॉसरेफ] [पबमेड]
38. चेन, डब्ल्यू.; कैल्वो, पीए; मालिडे, डी.; गिब्स, जे.; शुबर्ट, यू.; बेसिक, आई.; बस्ता, एस.; ओ'नील, आर.; शिकली, जे.; पलेसी, पी.; और अन्य। एक नवीन इन्फ्लूएंजा ए वायरस माइटोकॉन्ड्रियल प्रोटीन जो कोशिका मृत्यु को प्रेरित करता है। नेट. मेड. 2001, 7, 1306-1312। [क्रॉसरेफ]
39. गिब्स, जेएस; मालिडे, डी.; हॉर्नुंग, एफ.; बेनिंक, जेआर; येवडेल, जेडब्ल्यू इन्फ्लूएंजा ए वायरस पीबी1-एफ2 प्रोटीन एक अनुमानित बुनियादी एम्फ़िपैथिक हेलिक्स के माध्यम से आंतरिक माइटोकॉन्ड्रियल झिल्ली को लक्षित करता है जो माइटोकॉन्ड्रियल फ़ंक्शन को बाधित करता है। जे. विरोल. 2003, 77, 7214-7224। [क्रॉसरेफ]
40. यमादा, एच.; चौनान, आर.; हिगाशी, वाई.; कुरिहारा, एन.; किडो, एच. माइटोकॉन्ड्रियल इन्फ्लूएंजा ए वायरस पीबी1-F2 प्रोटीन का लक्ष्यीकरण अनुक्रम और माइटोकॉन्ड्रिया में इसका कार्य। FEBS लेट. 2004, 578, 331-336। [क्रॉसरेफ] [पबमेड]
41. योशिज़ुमी, टी.; इचिनोहे, टी.; सासाकी, ओ.; ओटेरा, एच.; कावाबाता, एस.; मिहारा, के.; कोशिबा, टी. इन्फ्लुएंजा ए वायरस प्रोटीन पीबी1-F2 टॉम40 चैनलों के माध्यम से माइटोकॉन्ड्रिया में स्थानांतरित हो जाता है और जन्मजात प्रतिरक्षा को ख़राब कर देता है। नेट. कम्यून. 2014, 5, 4713. [क्रॉसरेफ]
42. वांग, आर.; झू, वाई.; रेन, सी.; यांग, एस.; तियान, एस.; चेन, एच.; जिन, एम.; झोउ, एच. इन्फ्लुएंजा ए वायरस प्रोटीन पीबी1-F2 माइटोफैगी को प्रेरित करके जन्मजात प्रतिरक्षा को ख़राब करता है। ऑटोफैगी 2021, 17, 496-511। [क्रॉसरेफ]
43. पिला-कैस्टेलानोस, आई.; मोलिनो, डी.; मैककेलर, जे.; लाइन्स, एल.; दा ग्रेका, जे.; तौज़िएट, एम.; चांटेलूप, एल.; मिकेलियन, आई.; मेनिएल-स्किक्लिन, एल.; कोडोग्नो, पी.; और अन्य। एक नई एंटीवायरल रणनीति के रूप में इन्फ्लूएंजा वायरस संक्रमण से प्रेरित माइटोकॉन्ड्रियल मॉर्फोडायनामिक्स परिवर्तन। PLoS पैथोग. 2021, 17, e1009340।
44. कॉर्निलेज़-टाइ, सीटी; लियाओ, एल.; येट्स, जेआर, तीसरा; कुह्न, पी.; बुकमीयर, एमजे सीवियर एक्यूट रेस्पिरेटरी सिंड्रोम कोरोना वायरस नॉनस्ट्रक्चरल प्रोटीन 2 माइटोकॉन्ड्रियल बायोजेनेसिस और इंट्रासेल्युलर सिग्नलिंग में शामिल एक मेजबान प्रोटीन कॉम्प्लेक्स के साथ इंटरैक्ट करता है। जे. विरोल. 2009, 83, 10314-10318। [क्रॉसरेफ]
45. मर्कविर्थ, सी.; लैंगर, टी. माइटोकॉन्ड्रिया के भीतर प्रोहिबिटिन फ़ंक्शन: कोशिका प्रसार और क्राइस्ट मोर्फोजेनेसिस के लिए आवश्यक भूमिकाएँ। बायोचिम। बायोफिज़। एक्टा 2009, 1793, 27-32। [क्रॉसरेफ]
46. शि, सीएस; क्यूई, एचवाई; बौलारन, सी.; हुआंग, एनएन; अबू-असब, एम.; शेलहैमर, जेएच; केहरल, जेएच सार्स-कोरोनावायरस ओपन रीडिंग फ्रेम{{3}बी माइटोकॉन्ड्रिया और एमएवीएस/टीआरएएफ3/टीआरएएफ6 सिग्नलोसोम को लक्षित करके जन्मजात प्रतिरक्षा को दबा देता है। जे. इम्यूनोल. 2014, 193, 3080-3089। [क्रॉसरेफ] [पबमेड]
47. सिंह, एम.; बंसल, वी.; फेस्चोटे, सी. मानव कोरोनोवायरस प्रवेश कारकों का एक एकल-कोशिका आरएनए अभिव्यक्ति मानचित्र। सेल प्रतिनिधि 2020, 32, 108175। [क्रॉसरेफ] [पबमेड]
48. गॉर्डन, डीई; जंग, जीएम; बौहादौ, एम.; जू, जे.; ओबेर्निएर, के.; सफ़ेद, के.एम.; ओ'मीरा, एमजे; रेजेलज, वी.वी.; गुओ, जेजेड; स्वानी, डीएल; और अन्य। एक SARS-CoV-2 प्रोटीन इंटरेक्शन मानचित्र दवा के पुनर्प्रयोजन के लक्ष्यों का खुलासा करता है। प्रकृति 2020, 583, 459-468। [क्रॉसरेफ] [पबमेड]
49. ऐसहान, डी.; जियांग, एक्स.; मॉर्गन, महानिदेशक; ह्यूसर, जेई; वांग, एक्स.; एके, सीडब्ल्यू एपोप्टोसोम की त्रि-आयामी संरचना: असेंबली, प्रोकास्पेज़ -9 बाइंडिंग और सक्रियण के लिए निहितार्थ। मोल. सेल 2002, 9, 423-432। [क्रॉसरेफ]
50. नोमुरा-ताकीगावा, वाई.; नागानो-फ़ूजी, एम.; डेंग, एल.; किताज़ावा, एस.; इशिदो, एस.; सदा, के.; होट्टा, एच. हेपेटाइटिस सी वायरस का गैर-संरचनात्मक प्रोटीन 4ए माइटोकॉन्ड्रिया पर जमा हो जाता है और कोशिकाओं को माइटोकॉन्ड्रिया-मध्यस्थ एपोप्टोसिस से गुजरने का खतरा पैदा कर देता है। जे जनरल विरोल। 2006, 87, 1935-1945। [क्रॉसरेफ] [पबमेड]
51. चिउ, एचएल; हसीह, वाईएस; हसीह, एमआर; चेन, टीवाई एचसीवी ई2 माइटोकॉन्ड्रियल-संबंधित कैस्पेज़ मार्ग के माध्यम से हुह -7 कोशिकाओं के एपोप्टोसिस को प्रेरित कर सकता है। जैव रसायन. बायोफिज़। रेस. कम्यून. 2006, 345, 453-458। [क्रॉसरेफ]
52. ली, एसके; पार्क, एसओ; जो, सीओ; किम, वाईएस एप्सिलॉन प्रोटीन के साथ एचसीवी कोर प्रोटीन की परस्पर क्रिया एपोप्टोसिस को सक्रिय करने के लिए बैक्स जारी करती है। जैव रसायन. बायोफिज़। रेस. कम्यून. 2007, 352, 756-762। [क्रॉसरेफ] [पबमेड]
53. झाओ, पी.; हान, टी.; गुओ, जे जे; झू, एसएल; वांग, जे.; एओ, एफ.; जिंग, एमजेड; वह, वाईएल; वू, जेडएच; हां, एलबी एचसीवी एनएस4बी माइटोकॉन्ड्रियल मृत्यु मार्ग के माध्यम से एपोप्टोसिस को प्रेरित करता है। वायरस रेस. 2012, 169, 1-7. [क्रॉसरेफ] [पबमेड]
54. जावेद, एफ.; मंज़ूर, एस. जीनोटाइप 3ए का एचसीवी गैर-संरचनात्मक एनएस4ए प्रोटीन, बैक्स और कैस्पेज़ कैस्केड को सक्रिय करके माइटोकॉन्ड्रिया-मध्यस्थता से मृत्यु को प्रेरित करता है। सूक्ष्म जीव। पाथोग. 2018, 124, 346-355। [क्रॉसरेफ] [पबमेड]
55. तकादा, एस.; शिराकाटा, वाई.; कनेनिवा, एन.; कोइके, के. माइटोकॉन्ड्रिया के साथ हेपेटाइटिस बी वायरस एक्स प्रोटीन का जुड़ाव परमाणु परिधि पर माइटोकॉन्ड्रियल एकत्रीकरण का कारण बनता है, जिससे कोशिका मृत्यु होती है। ऑन्कोजीन 1999, 18, 6965-6973। [क्रॉसरेफ] [पबमेड]
56. नसीरुद्दीन, एएम; वांग, एल.; लियू, डीएक्स मानव और पशु कोशिकाओं के डेंगू वायरस संक्रमण द्वारा पी 53- आश्रित और माइटोकॉन्ड्रिया-मध्यस्थता कोशिका मृत्यु मार्ग का प्रेरण। सूक्ष्मजीव संक्रमित करते हैं। 2008, 10, 1124-1132। [क्रॉसरेफ]
57. गाओ, WY; ली, डी.; कै, डीई; हुआंग, XY; झेंग, बीवाई; हुआंग, YH; चेन, जेडएक्स; वैंग, एक्सजेड हेपेटाइटिस बी वायरस एक्स प्रोटीन माइटोकॉन्ड्रियल पारगम्यता संक्रमण छिद्र के मॉड्यूलेशन के माध्यम से एचएल -7702 कोशिकाओं को ऑक्सीडेटिव तनाव-प्रेरित एपोप्टोसिस के प्रति संवेदनशील बनाता है। ओंकोल. प्रतिनिधि 2017, 37, 48-56। [क्रॉसरेफ] [पबमेड]
58. किम, एचजे; किम, एसवाई; किम, जे.; ली, एच.; चोई, एम.; किम, जेके; आह, जेके हेपेटाइटिस बी वायरस एक्स प्रोटीन बैक्स के माइटोकॉन्ड्रिया में स्थानांतरण को बढ़ाकर एपोप्टोसिस को प्रेरित करता है। आईयूबीएमबी लाइफ 2008, 60, 473-480। [क्रॉसरेफ]
59. पधान, के.; मिनाक्षी, आर.; तौहीद, एमएबी; जमील, एस. गंभीर तीव्र श्वसन सिंड्रोम कोरोना वायरस 3ए प्रोटीन पी38 एमएपी किनेसे सक्रियण के माध्यम से माइटोकॉन्ड्रियल मृत्यु मार्ग को सक्रिय करता है। जे जनरल विरोल। 2008, 89, 1960-1969। [क्रॉसरेफ] [पबमेड]
60. झांग, एल.; वेई, एल.; जियांग, डी.; वांग, जे.; कांग्रेस, एक्स.; फी, आर. सार्स-सीओवी न्यूक्लियोकैप्सिड प्रोटीन प्रेरित एपोप्टोसिस ऑफ सीओएस-1 जो माइटोकॉन्ड्रियल मार्ग द्वारा मध्यस्थ है। आर्टिफ. कोशिकाएँ रक्त पदार्थ। अचल. जैव प्रौद्योगिकी। 2007, 35, 237-253। [क्रॉसरेफ]
61. चान, सीएम; मा, सीडब्ल्यू; चान, WY; चान, एचवाई सार्स-कोरोनावायरस मेम्ब्रेन प्रोटीन एक्ट सर्वाइवल पाथवे को संशोधित करके एपोप्टोसिस को प्रेरित करता है। आर्क बायोकेम. बायोफिज़। 2007, 459, 197-207।
62. ग्युरेरो, आर.; ग्युरेरो, सी.; अकोस्टा, ओ. रोटावायरस आइसोलेट Wt1-5 के संक्रमण से मानव तीव्र लिम्फोब्लास्टिक ल्यूकेमिया सेल लाइन रेह में कोशिका मृत्यु का प्रेरण। बायोमेडिसिन 2020, 8, 242। [क्रॉसरेफ] [पबमेड]
63. मार्टिन-लैटिल, एस.; मूसन, एल.; ऑट्रेट, ए.; कोल्बेरे-गैरापिन, एफ.; ब्लोंडेल, बी. बैक्स माइटोकॉन्ड्रियल मार्ग के माध्यम से रोटावायरस-प्रेरित एपोप्टोसिस के दौरान सक्रिय होता है। जे. विरोल. 2007, 81, 4457-4464। [क्रॉसरेफ] [पबमेड]
64. भौमिक, आर.; हलदर, यूसी; चट्टोपाध्याय, एस.; नायक, एमके; चावला-सरकार, एम. रोटावायरस-एनकोडेड नॉनस्ट्रक्चरल प्रोटीन 1 ट्यूमर सप्रेसर प्रोटीन पी53 को लक्षित करके सेलुलर एपोप्टोटिक मशीनरी को नियंत्रित करता है। जे. विरोल. 2013, 87, 6840-6850। [क्रॉसरेफ]
65. मुखर्जी, ए.; पात्रा, यू.; भौमिक, आर.; चावला-सरकार, एम. रोटावायरल नॉनस्ट्रक्चरल प्रोटीन 4 संक्रमण के दौरान डायनामिन-संबंधित प्रोटीन 1-निर्भर माइटोकॉन्ड्रियल विखंडन को ट्रिगर करता है। सेल माइक्रोबायोल. 2018, 20, ई12831। [क्रॉसरेफ] [पबमेड]
66. ज़मारिन, डी.; गार्सिया-सास्त्रे, ए.; जिओ, एक्स.; वांग, आर.; पैलेज़, पी. इन्फ्लुएंजा वायरस पीबी1-F2 प्रोटीन माइटोकॉन ड्रायल ANT3 और VDAC1 के माध्यम से कोशिका मृत्यु को प्रेरित करता है। PLoS पैथोग. 2005, 1, ई4. [क्रॉसरेफ]
67. यांग, एस.; गोर्शकोव, के.; ली, ईएम; जू, एम.; चेंग, वाईएस; सन, एन.; सोहिलियन, एफ.; डी वैल, एन.; मिंग, जी.; गीत, एच.; और अन्य। बढ़े हुए माइटोकॉन्ड्रियल विखंडन के माध्यम से जीका वायरस-प्रेरित न्यूरोनल एपोप्टोसिस। सामने। माइक्रोबायोल. 2020, 11, 598203। [क्रॉसरेफ]
68. न्यूमैन, एस.; एल मादीदी, एस.; फलेट्टी, एल.; हॉन, एफ.; लबीब, एस.; शेज्टमैन, ए.; मौरर, यू.; बोर्नर, सी. वायरस माइटोकॉन्ड्रिया-मध्यस्थता एपोप्टोसिस को कैसे नियंत्रित करते हैं? वायरस रेस. 2015, 209, 45-55। [क्रॉसरेफ] [पबमेड]
69. मैउरी, एमसी; ज़ल्क्वर, ई.; किम्ची, ए.; क्रोमर, जी. स्व-भोजन और आत्म-हत्या: ऑटोफैगी और एपोप्टोसिस के बीच क्रॉसस्टॉक। नेट. आदरणीय मोल. सेल बायोल. 2007, 8, 741-752. [क्रॉसरेफ]
70. ली, एस.; वांग, जे.; झोउ, ए.; खान, एफए; हू, एल.; झांग, एस. पोर्सिन प्रजनन और श्वसन सिंड्रोम वायरस एपोप्टोसिस को कम करने के लिए माइटोकॉन्ड्रियल विखंडन और माइटोफैगी को ट्रिगर करता है। ऑनकोटारगेट 2016, 7, 56002-56012।
71. मेंग, जी.; ज़िया, एम.; वांग, डी.; चेन, ए.; वांग, वाई.; वांग, एच.; यू, डी.; वेई, जे. मिटोफैगी फेफड़ों के कैंसर कोशिकाओं में आंतरिक एपोप्टोसिस को अवरुद्ध करके ऑनकोलिटिक न्यूकैसल रोग वायरस की प्रतिकृति को बढ़ावा देता है। ऑनकोटारगेट 2014, 5, 6365-6374।
72. फ्रुंड्ट, ईसी; यू, एल.; पार्क, ई.; लेनार्डो, एमजे; जू, एक्सएन गंभीर तीव्र श्वसन सिंड्रोम कोरोनोवायरस ओपन रीडिंग फ्रेम 3बी प्रोटीन के उपकोशिकीय स्थानीयकरण के लिए आणविक निर्धारक। जे. विरोल. 2009, 83, 6631-6640। [क्रॉसरेफ]
73. बोजकोवा, डी.; क्लैन, के.; कोच, बी.; क्रॉस, डी.; सिसेक, एस.; सिनाटल, जे.; मुंच, सी. SARS-CoV संक्रमित मेजबान कोशिकाओं के प्रोटिओमिक्स से चिकित्सा लक्ष्यों का पता चलता है। प्रकृति 2020, 583, 469-472। [क्रॉसरेफ] [पबमेड]
74. माइलान, ई.; कुरेन, जे.; हॉफमैन, के.; मुरादपुर, डी.; बाइंडर, एम.; बार्टेंस्क्लेगर, आर.; Tschopp, J. कार्डिफ़ RIG-I एंटीवायरल मार्ग में एक एडेप्टर प्रोटीन है और हेपेटाइटिस सी वायरस द्वारा लक्षित है। प्रकृति 2005, 437, 1167-1172। [क्रॉसरेफ] [पबमेड]
75. ली, एक्सडी; सन, एल.; सेठ, आरबी; पिनेडा, जी.; चेन, जेडजे हेपेटाइटिस सी वायरस प्रोटीज एनएस3/4ए जन्मजात प्रतिरक्षा से बचने के लिए माइटोकॉन्ड्रियल एंटीवायरल सिग्नलिंग प्रोटीन को माइटोकॉन्ड्रिया से अलग कर देता है। प्रोक. नेटल. अकाद. विज्ञान. यूएसए 2005, 102, 17717-17722। [क्रॉसरेफ] [पबमेड]
76. फेंग, एच.; सैंडर, एएल; मोरेरा-सोतो, ए.; यामाने, डी.; ड्रेक्सलर, जेएफ; लेमन, एसएम हेपेटोवायरस 3एबीसी प्रोटीज और माइटोकॉन्ड्रियल एंटीवायरल सिग्नलिंग प्रोटीन (एमएवीएस) का विकास। जे. हेपाटोल. 2019, 71, 25-34। [क्रॉसरेफ] [पबमेड]
77. कियान, एस.; फैन, डब्ल्यू.; लियू, टी.; वू, एम.; झांग, एच.; कुई, एक्स.; झोउ, वाई.; हू, जे.; वेई, एस.; चेन, एच.; और अन्य। सेनेका वैली वायरस दरार के लिए एडेप्टर प्रोटीन एमएवीएस, टीआरआईएफ और टैंक को लक्षित करके मेजबान प्रकार I इंटरफेरॉन उत्पादन को दबा देता है। जे. विरोल. 2017, 91, ई00823-17. [क्रॉसरेफ] [पबमेड]
78. वेई, सी.; नी, सी.; गीत, टी.; लियू, वाई.; यांग, एक्स.; झेंग, जेड.; जिया, वाई.; युआन, वाई.; गुआन, के.; जू, वाई.; और अन्य। हेपेटाइटिस बी वायरस एक्स प्रोटीन माइटोकॉन्ड्रियल एंटीवायरल सिग्नलिंग प्रोटीन को डाउनरेगुलेट करके जन्मजात प्रतिरक्षा को बाधित करता है। जे. इम्यूनोल. 2010, 185, 1158-1168। [क्रॉसरेफ]
79. सन, वाई.; झेंग, एच.; यू, एस.; डिंग, वाई.; वू, डब्ल्यू.; माओ, एक्स.; लियाओ, वाई.; मेंग, सी.; उर रहमान, ज़ेड.; टैन, एल.; और अन्य। न्यूकैसल रोग वायरस वी प्रोटीन ई3 यूबिकिटिन लिगेज आरएनएफ5 के माध्यम से मेजबान प्रकार I इंटरफेरॉन उत्पादन को रोकने के लिए माइटोकॉन्ड्रियल एंटीवायरल सिग्नलिंग प्रोटीन को नष्ट कर देता है। जे. विरोल. 2019, 93, ई00322-19। [क्रॉसरेफ]
80. डिंग, एस.; झू, एस.; रेन, एल.; फेंग, एन.; गीत, वाई.; जीई, एक्स.; ली, बी.; फ्लेवेल, आरए; ग्रीनबर्ग, एचबी रोटावायरस वीपी3 आंतों के उपकला कोशिकाओं में टाइप III इंटरफेरॉन अभिव्यक्ति को बाधित करने के लिए गिरावट के लिए एमएवीएस को लक्षित करता है। ईलाइफ 2018, 7, e39494। [क्रॉसरेफ] [पबमेड]
