अज्ञात गिटेलमैन सिंड्रोम के कारण जीवन-घातक हाइपोकैलिमिया के साथ उन्नत क्रोनिक किडनी रोग
Oct 19, 2023
हम क्यों थकेंगे? हम थकान की समस्या को कैसे हल कर सकते हैं?
【संपर्क】ईमेल: george.deng@wecistanche.com / व्हाट्सएप:008613632399501/वीचैट:13632399501
अमूर्त।हम एक ऐसे मामले की रिपोर्ट कर रहे हैं जिसमें एक 58- वर्षीय महिला में ओलिगुरिया, थकान, एनोरेक्सिया, कब्ज, हाइपोवोलेमिक लक्षण और प्रयोगशाला परीक्षणों में गंभीर हाइपोकैलेमिया (1.7 mEq/L), हाइपोनेट्रेमिया (120 mEq/L) के लक्षण दिखाई दे रहे हैं। , उच्च सीरम क्रिएटिनिन (एससीआर, 6.46 मिलीग्राम/डीएल) और यूरिया (352 मिलीग्राम/डीएल)। रोगी को पहले क्रोनिक किडनी रोग (सीकेडी) का निदान किया गया था, जिसमें 1 वर्ष पहले एससीआर 2.58 मिलीग्राम/डीएल तक था, और उसके पिछले सभी प्रयोगशाला परीक्षणों में हाइपोकैलिमिया दिखाया गया था, जिसका कम-सामान्य रक्त के बावजूद रूढ़िवादी उपायों और इप्लेरेनोन के साथ इलाज किया गया था। दबाव और सामान्य हृदय कार्य। पोटेशियम की कमी को बहाल करने, हाइपोवोलेमिक हाइपोनेट्रेमिया को वापस लाने और गुर्दे के कार्य को समर्थन देने (4 डायलिसिस सत्र सहित) के लिए समन्वित उपाय लागू किए गए थे। इसके अलावा, सावधानीपूर्वक निदान दृष्टिकोण से मूत्र में अनुचित रूप से उच्च सोडियम और पोटेशियम हानि, हाइपोकैल्सीयूरिया और हाइपररेनिनेमिक हाइपरल्डोस्टेरोनिज़्म का पता चला, जिससे गिटेलमैन सिंड्रोम और हाइपोकैलिमिया से संबंधित क्रोनिक ट्यूबलोइंटरस्टीशियल नेफ्रोपैथी का निदान हुआ। महत्वपूर्ण रूप से, उच्च पोटेशियम और उदार सोडियम आहार पर निर्देशों के एक सरल सेट के अनुपालन ने रोगी को न केवल यूवोलेमिक, लक्षणों से मुक्त और सामान्य इलेक्ट्रोलाइट्स के साथ रहने में सक्षम बनाया, बल्कि गुर्दे के कार्य के एक महत्वपूर्ण हिस्से को ठीक करने और पहले के सीकेडी चरण में स्थिर होने में भी सक्षम बनाया। . गिटेलमैन सिंड्रोम एक दुर्लभ विकार है जिसका सरल उपायों से आसानी से निदान और इलाज किया जा सकता है; जीवन-घातक जटिलताओं से बचने के लिए इसका शीघ्र निदान आवश्यक है।
सिस्टैंच एक थकान-विरोधी और सहनशक्ति बढ़ाने वाले के रूप में कार्य कर सकता है, और प्रायोगिक अध्ययनों से पता चला है कि सिस्टैंच ट्यूबुलोसा का काढ़ा प्रभावी रूप से वजन उठाने वाले तैराकी चूहों में क्षतिग्रस्त यकृत हेपेटोसाइट्स और एंडोथेलियल कोशिकाओं की रक्षा कर सकता है, एनओएस 3 की अभिव्यक्ति को बढ़ा सकता है, और हेपेटिक ग्लाइकोजन को बढ़ावा दे सकता है। संश्लेषण, इस प्रकार थकान-रोधी प्रभावकारिता बढ़ाता है। फेनिलएथेनॉइड ग्लाइकोसाइड से भरपूर सिस्टैंच ट्यूबुलोसा अर्क सीरम क्रिएटिन कीनेज, लैक्टेट डिहाइड्रोजनेज और लैक्टेट के स्तर को काफी कम कर सकता है, और आईसीआर चूहों में हीमोग्लोबिन (एचबी) और ग्लूकोज के स्तर को बढ़ा सकता है, और यह मांसपेशियों की क्षति को कम करके थकान-विरोधी भूमिका निभा सकता है। और चूहों में ऊर्जा भंडारण के लिए लैक्टिक एसिड संवर्धन में देरी हो रही है। कंपाउंड सिस्टैंच ट्यूबुलोसा टैबलेट ने वजन वहन करने वाले तैराकी के समय को काफी लंबा कर दिया, हेपेटिक ग्लाइकोजन रिजर्व में वृद्धि की, और चूहों में व्यायाम के बाद सीरम यूरिया स्तर को कम कर दिया, जिससे इसका थकान-विरोधी प्रभाव दिखा। सिस्टैंचिस का काढ़ा व्यायाम करने वाले चूहों में सहनशक्ति में सुधार कर सकता है और थकान को दूर करने में तेजी ला सकता है, और लोड व्यायाम के बाद सीरम क्रिएटिन कीनेस की ऊंचाई को भी कम कर सकता है और व्यायाम के बाद चूहों के कंकाल की मांसपेशियों की संरचना को सामान्य रख सकता है, जो इंगित करता है कि इसका प्रभाव है शारीरिक शक्ति को बढ़ाने वाला और थकान दूर करने वाला। सिस्टैंचिस ने नाइट्राइट-जहर वाले चूहों के जीवित रहने के समय को भी काफी बढ़ा दिया और हाइपोक्सिया और थकान के खिलाफ सहनशीलता को बढ़ाया।

हर समय थके हुए पर क्लिक करें
कीवर्ड
गिटेलमैन सिंड्रोम - हाइपोकैलिमिया - हाइपोकैलेमिक नेफ्रोपैथी
परिचय
गिटेलमैन सिंड्रोम (जीएस), जिसे पारिवारिक हाइपोकैलिमिया-हाइपोमैग्नेसीमिया भी कहा जाता है, एक दुर्लभ वंशानुगत नमक खोने वाली ट्यूबलोपैथी है। यह कई उत्परिवर्तनों के कारण होता है, जिनमें से सबसे आम डिस्टल कन्वॉल्यूटेड ट्यूब्यूल (डीसीटी) में थियाजाइड-संवेदनशील NaCl कोट्रांसपोर्टर (एनसीसी) को एन्कोडिंग करने वाले एसएलसी12ए3 जीन से संबंधित है, और ऑटोसोमल रिसेसिव पैटर्न के साथ विरासत में मिला है [1]। यह शीर्षस्थ कोट्रांसपोर्टर DCT [2] के प्रारंभिक भाग में NaCl पुनर्अवशोषण में विशेष रूप से हस्तक्षेप करता है। आमतौर पर, सिंड्रोम में एनसीसी के माध्यम से बिगड़ा हुआ एपिकल परिवहन से उत्पन्न इलेक्ट्रोलाइट विकारों का एक संयोजन शामिल होता है, यानी, हाइपोकैलिमिया, मेटाबॉलिक अल्कलोसिस, हाइपोमैग्नेसीमिया और हाइपोकैल्सीयूरिया, जो एनसीसी पर थियाजाइड मूत्रवर्धक की कार्रवाई की नकल करते हैं [3]। जीएस की नैदानिक प्रस्तुति व्यापक रूप से भिन्न होती है, जबकि अनुपचारित बीमारी के दीर्घकालिक परिणामों को खराब रूप से परिभाषित किया जाता है।
इसमें, हम अज्ञात एटियोलॉजी के क्रोनिक किडनी रोग (सीकेडी) वाले एक रोगी का वर्णन करते हैं, जिसमें डायलिसिस-निर्भर गुर्दे की शिथिलता के साथ-साथ जीवन-घातक हाइपोकैलिमिया और गंभीर हाइपोनेट्रेमिया शामिल है, जिसे सावधानीपूर्वक निदान प्रक्रिया के बाद जीएस को जिम्मेदार ठहराया गया था, जिससे इलेक्ट्रोलाइट गड़बड़ी को ठीक किया जा सके। और गुर्दे की कार्यक्षमता में निरंतर सुधार होता है।

मामला का बिबरानी
एक 58- वर्षीय श्वेत महिला हमारे तृतीयक अस्पताल के आपातकालीन विभाग में कुछ दिन पहले शुरू हुई ओलिगुरिया, थकान और एनोरेक्सिया की शिकायत लेकर आई थी, और नियमित रूप से लैक्टुलोज द्वारा लक्षणानुसार कब्ज का इलाज किया गया था। पिछले प्रयोगशाला परीक्षण के परिणामों से पता चला कि सीकेडी (सीरम क्रिएटिनिन (एससीआर) 2.5 साल पहले 1.74 मिलीग्राम/डीएल, 13 महीने पहले 2.58 मिलीग्राम/डीएल, 11 महीने पहले 1.93 मिलीग्राम/डीएल, 5 महीने पहले 1.98 मिलीग्राम/डीएल और 5.12 मिलीग्राम/डीएल था। 1 सप्ताह पहले) सीरम पोटेशियम और सोडियम 3.39 mEq/L और 132 mEq/L के साथ 2.5 साल पहले, 2.37 mEq/L और 132.5 mEq/L 13 महीने पहले, 2.31 mEq/L और 129.7 mEq/L 11 महीने पहले, 3.47 mEq/L और 127.1 mEq/L 5 महीने पहले, 1.79 mEq/L और 119 mEq/L 5 दिन पहले, क्रमशः। उसके पिछले मेडिकल इतिहास में डिस्लिपिडेमिया, हाइपोथायरायडिज्म और थैलेसीमिया लक्षण शामिल थे। उसे दिन में एक बार इप्लेरेनोन 25 मिलीग्राम (ओडी), दिन में दो बार 675 मिलीग्राम पोटेशियम बाइकार्बोनेट की चमकीली गोलियाँ (बोली), 25-हाइड्रॉक्सीकोलेकैल्सीफेरॉल 400 आईयू ओडी, कैल्शियम कार्बोनेट 500 मिलीग्राम ओडी, एपोइटिन अल्फ़ा 5, {{49} मिल रहा था। } हर 3 सप्ताह में चमड़े के नीचे IU, फोलिक एसिड 5 mg od, सिमवास्टेटिन 20 mg od, लेवोथायरोक्सिन 25 ug od, और बड़ी खुराक में लैक्टुलोज़, विशेष रूप से अंतिम सप्ताह के दौरान। किसी अन्य निर्धारित एजेंट का उपयोग छोड़कर इलेक्ट्रॉनिक रिकॉर्ड के माध्यम से रोगी के पिछले नुस्खों की व्यापक खोज।
चिकित्सीय परीक्षण में, रोगी का तापमान 36.1 डिग्री सेल्सियस था, उसका रक्तचाप (बीपी) 109/60 एमएमएचजी था, उसकी हृदय गति (एचआर) 60 बीट/मिनट थी, और कमरे की हवा में उसकी ऑक्सीजन संतृप्ति (एसपी02) 98% थी। . हृदय और फेफड़े के गुदाभ्रंश और पेट की नैदानिक परीक्षा में कोई असामान्य निष्कर्ष सामने नहीं आया, लेकिन कम इंट्रावास्कुलर वॉल्यूम (त्वचा में मरोड़, ठंडे हाथ-पैर और सूखी श्लेष्मा झिल्ली) के नैदानिक संकेत मौजूद थे। शेष शारीरिक परीक्षा अचूक थी।
धमनी रक्त गैसों के विश्लेषण से पता चला कि pH=7.225, HCO3 -=9.9 mEq/L, pCO{5}}.9 mmHg, आयन गैप (AG)=23.1 mEq /एल, क्लोराइड (सीएल– )=86 एमईक्यू/एल। तालिका 1 में दर्शाए गए प्रयोगशाला परिणामों में ऊंचा एससीआर (6.46 मिलीग्राम/डीएल) और यूरिया (352 मिलीग्राम/डीएल), हेमाटोक्रिट 22.6%, कम सीरम पोटेशियम (1.7 एमईक्यू/एल) और सोडियम स्तर (120 एमईक्यू/एल) और दिखाया गया है। उच्च मैग्नीशियम (4.8 मिलीग्राम/डीएल)। यूरिनलिसिस प्रोटीन और हीमोग्लोबिन के लिए सकारात्मक था, जबकि तलछट में प्रति उच्च-शक्ति क्षेत्र में 50-55 ल्यूकोसाइट्स और 51 - 80 लाल रक्त कोशिकाएं दिखाई दीं। इलेक्ट्रोकार्डियोग्राम (ईसीजी) में प्रमुख यू तरंगें और लंबे समय तक क्यूटी अंतराल (480 एमएस) का पता चला, जबकि किडनी के अल्ट्रासाउंड में कॉर्टिकोमेडुलरी भेदभाव के नुकसान के साथ सामान्य के भीतर रुकावट और किडनी के आकार का कोई सबूत नहीं दिखा।
नैदानिक और प्रयोगशाला निष्कर्षों की गंभीरता और तात्कालिकता के आधार पर, रोगी को अल्पकालिक इकाई में 2 घंटे के भीतर 250 एमएल सामान्य सेलाइन (एन/एस) के साथ 27 एमईक्यू पोटेशियम क्लोराइड (केसीएल) के साथ अंतःशिरा (आईवी) द्रव चिकित्सा प्राप्त हुई। हमारे अस्पताल का. इसके बाद, मरीज को आगे की जांच और उपचार के लिए नेफ्रोलॉजी विभाग में भर्ती कराया गया। अगले दिनों में, रोगी को सावधानीपूर्वक KCl अनुपूरण (81 से 108 mEq/दिन तक) और सावधानीपूर्वक बाइकार्बोनेट प्रशासन के साथ IV द्रव प्रशासन के साथ इलाज किया गया। पहले 8 घंटों के भीतर मरीज की मूत्राधिक्य 700 एमएल और अगले दिन के दौरान 1,200 एमएल थी। दूसरे दिन, एससीआर (5.6 मिलीग्राम/डीएल) और यूरिया स्तर (316 मिलीग्राम/डीएल) में सुधार नहीं होने के कारण उच्च डायलिसिस पोटेशियम के साथ हेमोडायलिसिस (कुल 4 सत्र) की शुरुआत हुई। मरीज को 2 यूनिट लाल रक्त कोशिकाएं भी चढ़ाई गईं और एपोइटिन उपचार शुरू किया गया। सकारात्मक मूत्र संस्कृति के आधार पर सिप्रोफ्लोक्सासिन 200 मिलीग्राम बोली के साथ एक एंटीबायोटिक आहार भी शुरू किया गया था।

दूसरे दिन किए गए 24-घंटे के मूत्र संग्रह में 485 मिलीग्राम/24 घंटे पर क्रिएटिनिन, 7 ग्राम/24 घंटे पर यूरिया, 2.32 ग्राम/24 घंटे पर प्रोटीन, 79 एमईक्यू/24 घंटे पर सोडियम और 8 एमईक्यू/ पर पोटेशियम का उत्सर्जन दिखाया गया। 24 घंटे, 42% पोटेशियम (FeK) के आंशिक उत्सर्जन और 16.49 mEq/g के मूत्र पोटेशियम-से-क्रिएटिनिन अनुपात (यूके: UC) के अनुरूप। रोगी को अंतिम हेमोडायलिसिस सत्र 6वें दिन प्राप्त हुआ; इसके बाद, एससीआर 3 और 3.5 मिलीग्राम/डीएल और यूरिया 80 - 100 मिलीग्राम/डीएल के बीच रहा। सीरम पोटेशियम 10वें दिन सामान्य स्तर (3.6 mEq/L) पर पहुंच गया; इस दिन, मूत्र में पोटेशियम का उत्सर्जन 34 mEq/24 घंटे था, जो 27% FeK के अनुरूप था, और मूत्र में पोटेशियम की निरंतर हानि का संकेत दे रहा था। उसके बाद, सीरम स्तर के आधार पर IV KCl अनुपूरण को पोटेशियम ग्लूकोनेट के मौखिक अनुपूरण से बदल दिया गया।
तीसरे दिन, मरीज़ का बीपी 103/55 एमएमएचजी पर होने के साथ, प्लाज्मा रेनिन गतिविधि (पीआरए) 18.72 एनजी/एमएल/एच पर थी (लेटी हुई स्थिति में संदर्भ सीमा: 0.2 - 1.4 एनजी/एमएल/एच), और एल्डोस्टेरोन 36 एनजी/डीएल (संदर्भ सीमा: 1.0 - 16 एनजी/डीएल) पर, जो भारी माध्यमिक हाइपरल्डोस्टेरोनिज़्म का संकेत देता है। 5वें दिन, एक इकोकार्डियोग्राम से सामान्य सीमा और सामान्य सिस्टोलिक फ़ंक्शन (बाएं वेंट्रिकुलर इजेक्शन अंश 60 - 65%), हल्के ट्राइकसपिड और माइट्रल वाल्व रिगर्जेटेशन, हल्के महाधमनी वाल्व कैल्सीफिकेशन और पेरिकार्डियल तरल पदार्थ की न्यूनतम मात्रा के भीतर चैम्बर आकार का पता चला। हृदय की पिछली दीवार. यह ध्यान दिया जाना चाहिए कि रोगी को पहले एक हृदय रोग विशेषज्ञ और एक नेफ्रोलॉजिस्ट के पास भेजा गया था और 3 और 4 साल पहले, 2 बार पीआरए और एल्डोस्टेरोन माप लिया गया था, एक बार सामान्य दिखा, और दूसरी बार थोड़ा ऊंचा स्तर दिखा; उसका सीटी स्कैन भी कराया गया था जिसमें अधिवृक्क ग्रंथियां सामान्य दिख रही थीं।
अस्पताल में भर्ती होने के 13 दिनों के बाद, मरीज को उच्च पोटेशियम (प्रतिदिन दो केले) और उदार सोडियम आहार के साथ-साथ निम्नलिखित आहार का सेवन करने के निर्देश के साथ अस्पताल से छुट्टी दे दी गई: फोलिक एसिड 5 मिलीग्राम ओडी, कैल्शियम कार्बोनेट 500 मिलीग्राम 3 बार। दिन (टीआईडी), पोटेशियम बाइकार्बोनेट 1,350 मिलीग्राम बोली, लेवोथायरोक्सिन 22 यूजी ओडी, सिमवास्टैटिन 20 मिलीग्राम ओडी, अल्फाकैल्सीडोल 1 यूजी ओडी, और एपोइटिन अल्फ़ा 5, 000 आईयू चमड़े के नीचे सप्ताह में 3 बार। चार दिन बाद, नेफ्रोलॉजी क्लिनिक में रोगी का मूल्यांकन SCr=1.99 mg/dL और K{15}}.5 mEq/L के साथ किया गया, जिससे पोटेशियम बाइकार्बोनेट बंद हो गया। मरीज ~ 1, 2, और 5 महीने के बाद क्लिनिक में आया; उसके प्रयोगशाला परिणाम तालिका 1 में प्रस्तुत किए गए हैं। जैसा कि उसी तालिका में दिखाया गया है, उच्च पोटेशियम और उदार सोडियम सेवन (80 - 90 एमईक्यू/दिन और 136 - 182 एमईक्यू/दिन) पर निर्देशों का पालन करके, रोगी यूवोलेमिया को बनाए रखने में सक्षम था। और सामान्य सीरम पोटेशियम, लक्षणों (चक्कर आना, कब्ज, आदि) से मुक्त हो, और गुर्दे के कार्य की एक महत्वपूर्ण डिग्री (एससीआर=1.5 मिलीग्राम/डीएल) पुनः प्राप्त करें।
बहस
जीएस एक सामान्य विरासत में मिली ट्यूबलोपैथी है, जिसमें श्वेत लोगों में हेटेरोज़ायगोट का प्रसार ~ 1% अनुमानित है [4]। प्रारंभिक डीसीटी में एनसीसी के कार्य-क्षम उत्परिवर्तन के कारण Na+ पुनर्अवशोषण कम हो गया, साथ ही आइसोटोनिक पानी की बर्बादी भी हुई। परिणामी हाइपोवोलेमिक उत्तेजना रेनिन-एंजियोटेंसिन-एल्डोस्टेरोन प्रणाली (माध्यमिक हाइपरल्डोस्टेरोनिज्म) को सक्रिय करती है। Na+ डिलीवरी के साथ-साथ डिस्टल नेफ्रॉन में एल्डोस्टेरोन का स्तर बढ़ने से K+ (कलियूरिया) और H+ (एसिड्यूरिया) के बदले में Na+ का पुनर्अवशोषण होता है [5]। बढ़ी हुई मैग्नीसुरिया और हाइपोकैल्सीयूरिया भी आमतौर पर दिखाई देती है। जीएस का संदेह निम्नलिखित मानदंडों पर आधारित है [3]: 1) अनुचित गुर्दे पोटेशियम बर्बादी के साथ क्रोनिक हाइपोकैलिमिया (एफईके और यूके में वृद्धि: यूसी); 2) चयापचय क्षारमयता; 3) अनुचित वृक्क मैग्नीशियम बर्बादी (FeMg में वृद्धि) के साथ हाइपोमैग्नेसीमिया; 4) हाइपोकैल्सीयूरिया (FeCa कम); 5) क्लोराइड (FeCl) का आंशिक उत्सर्जन > 0.5%; 6) उच्च पीआरए; 7) निम्न या सामान्य-निम्न बीपी; 8) सामान्य गुर्दे का अल्ट्रासाउंड [3]।
हालाँकि जीएस के कुछ मरीज़ स्पर्शोन्मुख रह सकते हैं, उनमें से अधिकांश में विभिन्न प्रकार के नैदानिक लक्षण और संकेत दिखाई दे सकते हैं, जिनमें नमक की लालसा, थकान, न्यूरोमस्कुलर लक्षण (चक्कर आना, पेरेस्टेसिया, कार्पोपेडल ऐंठन, मांसपेशियों में कमजोरी, जोड़ों का दर्द), गुर्दे के लक्षण (बहुमूत्रता) शामिल हैं। पॉलीडिप्सिया, नॉक्टुरिया), गैस्ट्रोइंटेस्टाइनल शिकायतें (कब्ज, पेट दर्द), हृदय संबंधी लक्षण (धड़कन, वेंट्रिकुलर अतालता), और विकासात्मक गड़बड़ी (छोटा कद, विकास और/या यौवन में देरी) [3, 6]। ध्यान दें, फुजीमुरा एट अल। [7] पता चला कि 50% से अधिक जीएस रोगियों का निदान यादृच्छिक रक्त परीक्षणों के माध्यम से किया जाता है, भले ही वे अलग-अलग समय के लिए कई लक्षणों का अनुभव करते हों।

यह मामला जीएस के संबंध में महत्वपूर्ण सबक पर प्रकाश डालता है। सबसे पहले, हमारे रोगी में, कई वर्षों तक अत्यधिक विचारोत्तेजक लक्षणों और लगातार हाइपोकैलिमिया और हाइपोनेट्रेमिया के अस्तित्व के बावजूद, निदान में लंबे समय तक देरी हुई थी। रोगी को पहले विभिन्न विशिष्टताओं के चिकित्सकों द्वारा देखा गया था, जिनमें सामान्य चिकित्सक, एक हृदय रोग विशेषज्ञ और यहां तक कि एक नेफ्रोलॉजिस्ट भी शामिल थे, जिनमें से सभी ने उपरोक्त को नजरअंदाज कर दिया और हाइपोकैलिमिया का लक्षणात्मक रूप से पोटेशियम अनुपूरण और इप्लेरेनोन की शुरुआत के साथ इलाज किया, शायद एक की गलत व्याख्या के कारण सामान्य पीआरए और एल्डोस्टेरोन परीक्षण और सामान्य अधिवृक्क आकृति विज्ञान। हालाँकि, PRA और एल्डोस्टेरोन में वृद्धि का पता नहीं लगाया जा सका होता, यदि उस समय हाइपोवोल्मिया को अस्थायी रूप से बहाल कर दिया गया होता, जिससे PRA और एल्डोस्टेरोन लगभग सामान्य स्तर पर वापस आ जाते। दूसरे, इस क्रोनिक हाइपोकैलिमिया के कारण गुर्दे की कार्यक्षमता में उत्तरोत्तर कमी आई, जो उसके अस्पताल में भर्ती होने से 1 वर्ष पहले ही 2.58 के एससीआर (अनुमानित ग्लोमेरुलर निस्पंदन दर (ईजीएफआर) 20 एमएल/मिनट/1.73एम2, यानी, सीकेडी चरण 4 के बराबर) तक पहुंच गया। रोगी को लंबे समय में गुर्दे की रिप्लेसमेंट थेरेपी शुरू करने की आवश्यकता की संभावना के बारे में सूचित किया जाता है। सुपरइम्पोज़्ड एक्यूट किडनी इंजरी (एकेआई), संभवतः मात्रा में कमी के कारण, गुर्दे की कार्यप्रणाली को और कम कर देती है और हेमोडायलिसिस की शुरुआत की आवश्यकता होती है। हालाँकि, हाइपोकैलिमिया से जुड़े क्रोनिक इंटरस्टिशियल नेफ्रैटिस का उचित निदान और अस्पताल के अंदर और बाहर के उपायों के सीधे सेट के साथ अंतर्निहित जीएस की उचित देखभाल ने रोगी को बड़े पैमाने पर गुर्दे की कार्यप्रणाली को ठीक करने में सक्षम बनाया, जो 1.5 मिलीग्राम के एससीआर तक पहुंच गया। /डीएल और ईजीएफआर 38 एमएल/मिनट/1.73एम2।
हमारे क्लिनिक में प्रवेश पर, रोगी को हाइपोवोलेमिया, ऑलिगुरिया, गंभीर हाइपोकैलिमिया, हाइपोनेट्रेमिया, हाइपोक्लोरेमिया और बढ़े हुए एजी के साथ आंशिक रूप से मुआवजा मेटाबोलिक एसिडोसिस के साथ प्रस्तुत किया गया, जो संभवतः हाइपोवोल्मिया के कारण हाइपोक्लोरेमिक मेटाबोलिक अल्कलोसिस के सह-अस्तित्व की ओर इशारा करता है। उपरोक्त के आधार पर, अंतिम चरण में प्रगतिशील सीकेडी के बजाय सीकेडी पर एकेआई का कार्यशील निदान लगाया गया। आपातकालीन प्रयासों को हाइपोकैलिमिया, हाइपोवोलेमिक हाइपोनेट्रेमिया और प्रीरेनल एकेआई की प्रगतिशील बहाली की दिशा में निर्देशित किया गया था। इसके अलावा, अंतर्निहित बीमारी के निर्णायक निदान तक पहुंचने के लिए समानांतर प्रयास किया गया।
Following continuous administration of isotonic solutions enriched with potassium, serum potassium levels were increasing slowly, a fact indicating the presence of chronic, severe total-body potassium deficit. In the case of our patient, an underlying salt-wasting tubular disorder, aggravated by intestinal losses due to lactulose overuse was possible. In any case, two calculations of FeK and UK: UC, both validated tools in the assessment of hypokalemia in healthy and diseased populations [3, 8], confirmed inappropriate kaliuresis despite very low serum potassium. Results of high PRA and aldosterone were compatible with hyperreninemic hyperaldosteronism. These findings, together with the high urine chloride concentration (>15 - 20 एमईक्यू/एल), मूत्र कैल्शियम 63 मिलीग्राम/24 घंटे (< 100 mg/24h), and the absence of use of thiazide diuretics, pointed towards the diagnosis of GS as the most plausible cause of our patient's clinical presentation, according to existing diagnostic algorithms (Figure 1) [9, 10]. Our patient presented with hypermagnesemia, instead of the hypomagnesemia anticipated by the diagnostic features of GS. This finding could be explained either by reduced renal magnesium excretion in the presence of reduced renal function [11], or by overconsumption of lactulose, as this laxative can increase the intestinal absorption of Mg2+ when it is catabolized to organic acids in the large intestine [12].

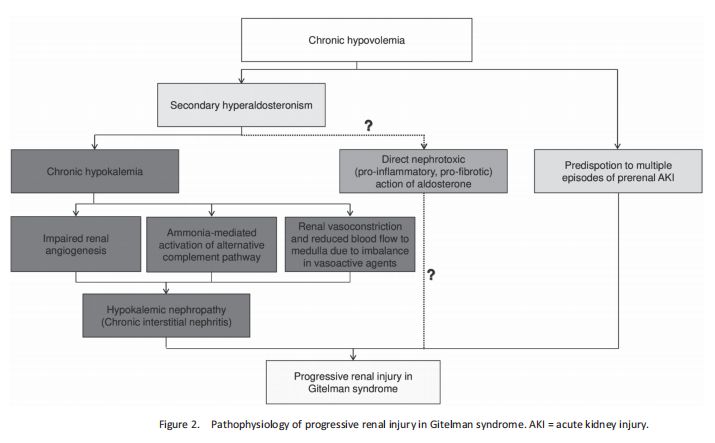
जीएस वाले हमारे रोगी में सीकेडी का विकास बहुघटकीय मूल का हो सकता है (चित्र 2)। क्रोनिक हाइपोकैलेमिया स्वयं ट्यूबलर वैक्यूलाइजेशन, सिस्टिक संरचनाओं और रीनल बायोप्सी में इंटरस्टीशियल फाइब्रोसिस के साथ ट्यूबलोइंटरस्टीशियल नेफ्रैटिस का कारण बनता है [13]। सुझाए गए तंत्रों में बिगड़ा हुआ रीनल एंजियोजेनेसिस और सहवर्ती पेरिटुबुलर केशिका हानि शामिल है जो खराब संवहनी एंडोथेलियल ग्रोथ फैक्टर (वीईजीएफ) अभिव्यक्ति [14] से जुड़ा है, वासोएक्टिव एजेंटों में असंतुलन (स्थानीय एंडोटिलिन और एंजियोटेंसिन II में वृद्धि, रीनल कैलिकेरिन और एनओ में कमी) शामिल है। वृक्क वाहिका संकुचन और वृक्क मज्जा में रक्त के प्रवाह और ऑक्सीजन में कमी [15, 16], और स्थानीय अमोनियाजेनेसिस में वृद्धि के कारण वैकल्पिक पूरक मार्ग का सक्रियण होता है [17]। इसके अलावा, क्रोनिक हाइपोवोल्मिया रोगियों को प्रीरेनल एकेआई के कई एपिसोड का अनुभव कराता है, खासकर जब आसन्न कारक सह-अस्तित्व में होते हैं (उदाहरण के लिए, निर्जलीकरण, और डायरिया एपिसोड) [18]। अंत में, पुरानी मात्रा में कमी से प्रेरित एल्डोस्टेरोन का उच्च स्तर प्रत्यक्ष नेफ्रोटॉक्सिक कार्रवाई कर सकता है, जो कि मिनरलोकॉर्टिकॉइड रिसेप्टर्स के सक्रियण द्वारा अपेक्षित प्रो-इंफ्लेमेटरी और प्रो-फाइब्रोटिक प्रभावों से संबंधित है, जैसा कि पहले AKI, उच्च रक्तचाप और के मॉडल में दिखाया गया था। मधुमेह संबंधी गुर्दे की बीमारी और कैल्सीनुरिनहिबिटर विषाक्तता के मामले [19]। इस परिकल्पना को जीएस और बार्टर सिंड्रोम वाले रोगियों में गुर्दे के कार्य के एक अवलोकन अध्ययन द्वारा समर्थित किया गया था, जिसमें निष्कर्ष निकाला गया था कि हाइपोकैलिमिया की डिग्री को जीएफआर हानि की डिग्री के साथ सीधे सहसंबद्ध नहीं किया जा सकता है, और संभवतः एल्डोस्टेरोन स्वयं इस हानि में एक प्रमुख भूमिका निभाता है। [20]. हालाँकि, जीएस के 6 रोगियों के एक छोटे से अध्ययन में, बढ़े हुए ऑक्सीडेटिव तनाव और आरएचओ किनेज़ मार्ग के सक्रियण के कारण एल्डोस्टेरोन के प्रो-इंफ्लेमेटरी और प्रोफाइब्रोटिक प्रभावों की अनुपस्थिति को नोट किया गया था [21]। इस प्रकार, इस प्रकार के व्यक्तियों में विशेष रूप से और अधिक शोध की आवश्यकता है।
हमारे मरीज के संबंध में एक दिलचस्प तथ्य यह है कि कुछ वर्षों से उसकी किडनी की कार्यक्षमता लगातार कम थी और अस्पताल में भर्ती होने के बाद कुछ ही महीनों में इसमें काफी सुधार हुआ। हालाँकि, ट्यूबलोइंटरस्टीशियल रोग वाले कुछ रोगियों में, यह देखते हुए कि क्रोनिक फ़ाइब्रोटिक ट्यूबलोइंटरस्टीशियल चोट की अपरिवर्तनीय क्षति व्यापक नहीं है, रोगजनक कारक की वापसी न केवल स्थिर हो सकती है, बल्कि गुर्दे के कार्य में थोड़ा सुधार भी कर सकती है [22, 23]। ऐसे मामलों में, व्यापक क्षति के बिना ग्लोमेरुली के एक हिस्से की उपस्थिति बरकरार नेफ्रॉन में बढ़े हुए निस्पंदन की अनुमति दे सकती है, जो पारंपरिक सिद्धांत के अनुसार, नष्ट हुए नेफ्रॉन के साथ खोए गए कार्य के लिए, कम से कम आंशिक रूप से क्षतिपूर्ति कर सकता है [24 , 25]। जहां तक हमारी जानकारी है, यह हाइपोकैलिमिया से जुड़े क्रोनिक ट्यूबलोइंटरस्टीशियल नेफ्रोपैथी वाले रोगी का पहला मामला है, जिसने रोगजनक कारक को वापस लेने के कुछ महीनों के भीतर अपने गुर्दे के कार्य को प्रभावशाली ढंग से दोगुना कर दिया है।
निष्कर्ष में, यह मामला इस तथ्य पर प्रकाश डालता है कि जीएस के उचित निदान की विफलता के कारण हाइपोवोल्मिया और हाइपोकैलेमिया का दीर्घकालिक सह-अस्तित्व हो सकता है, जिससे डायलिसिस की आवश्यकता होने पर गुर्दे की कार्यप्रणाली में महत्वपूर्ण हानि हो सकती है। ऐसे मामलों में, हाइपोवोल्मिया के साथ प्रभावशाली रूप से कम सीरम पोटेशियम को हमेशा चिकित्सकों को ट्यूबलर विकार की संभावना की याद दिलानी चाहिए और प्रासंगिक नैदानिक कार्य को ट्रिगर करना चाहिए जो आसानी से उचित निदान प्रकट कर सकता है। इससे प्रासंगिक गड़बड़ियों को ठीक करने के लिए सरल उपाय किए जा सकते हैं और सबसे महत्वपूर्ण बात यह है कि तीव्र चरण के बाद, सरल आहार उपायों पर रोगी का उचित मार्गदर्शन किया जा सकता है जो सामान्य इलेक्ट्रोलाइट और द्रव संतुलन को संरक्षित कर सकते हैं, पुराने लक्षणों को हल कर सकते हैं और रखरखाव में परिणाम दे सकते हैं। या गुर्दे की कार्यप्रणाली में भी सुधार।
अनुदान
यह पेपर किसी भी स्रोत द्वारा समर्थित नहीं था और लेखकों के मूल प्रयास का प्रतिनिधित्व करता है।

एक ऐसी स्थिति जिसमें सरकारी अधिकारी का निर्णय उसकी व्यक्तिगत रूचि से प्रभावित हो
किसी ने घोषणा नहीं की.
संदर्भ
[1] वर्गास-पुसौ आर, दहान के, काहिला डी, वेनिस ए, रिवेरा-मुनोज़ ई, डेबैक्स एच, ग्रिसार्ट बी, ब्रिडौक्स एफ, अनविन आर, मौलिन बी, हेमैन जेपी, वैन्टीघेम एमसी, रिगोथियर सी, डसोल बी, गोडिन एम, निवेट एच, डबॉर्ग एल, टैक आई, जिमेनेज-रोकप्लो एपी, हाउइलियर पी, एट अल। गिटेलमैन सिंड्रोम में उत्परिवर्तन का स्पेक्ट्रम। जे एम सोक नेफ्रोल. 2011; 22: 693-703.
[2] सुब्रमण्यम एआर, एलिसन डीएच। दूरस्थ कुंडलित नलिका. क्लिन जे एम सोक नेफ्रोल। 2014; 9: 2147-2163.
[3] ब्लैंचर्ड ए, बोकेनहाउर डी, बोलिग्नानो डी, कैलो एलए, कोसिन्स ई, डेवुयस्ट ओ, एलिसन डीएच, केरेट फ्रैंकल एफई, नोअर्स एनवी, कोनराड एम, लिन एसएच, वर्गास-पोसौ आर। गिटेलमैन सिंड्रोम: सर्वसम्मति और मार्गदर्शन किडनी रोग: वैश्विक परिणामों में सुधार (केडीआईजीओ) विवाद सम्मेलन। किडनी इंट. 2017; 91: 24-33. क्रॉसरेफ पबमेड
[4] नोअर्स एनवीएएम, लेवचेंको ईएन। गिटेलमैन सिंड्रोम. ऑर्फ़नेट जे रेयर डिस। 2008; 3: 22. क्रॉसरेफ पबमेड
[5] फ़िलिपेटोस टीडी, रिज़ोस सीवी, तज़ावेल्ला ई, एलिसाफ़ एमएस। गिटेलमैन सिंड्रोम: एसिड-बेस और इलेक्ट्रोलाइट असामान्यताओं के अंतर्निहित पैथोफिज़ियोलॉजिकल तंत्र का विश्लेषण। इंट यूरोल नेफ्रोल। 2018; 50: 91-96. क्रॉसरेफ पबमेड
[6] फुलचिएरो आर, एसईओ-मेयर पी. बार्टर सिंड्रोम और गिटेलमैन सिंड्रोम। पीडियाट्र क्लिन नॉर्थ एम. 2019; 66: 121-134. क्रॉसरेफ पबमेड
[7] फुजीमुरा जे, नोज़ू के, यामामुरा टी, मिनामिकावा एस, नाकानिशी के, होरिनौची टी, नागानो सी, साकाकिबारा एन, नाकानिशी के, शिमा वाई, मियाको के, नोज़ू वाई, मोरिसाडा एन, नागासे एच, निनचोजी टी, काइतो एच , इइजिमा के. गिटेलमैन सिंड्रोम वाले मरीजों में नैदानिक और आनुवंशिक विशेषताएं। किडनी अंतर्राष्ट्रीय प्रतिनिधि 2018; 4: 119-125. क्रॉसरेफ पबमेड
[8] ली जे, मा एच, लेई वाई, वान क्यू। हाइपोकैलिमिया में गुर्दे की पोटेशियम हानि के लिए स्पॉट मूत्र के नमूने से मापदंडों का नैदानिक मूल्य। क्लिन चिम एक्टा. 2020; 511: 221-226. क्रॉसरेफ पबमेड
[9] पामर बीएफ, क्लेग डीजे। किडनी विकारों के निदान में चयनित मूत्र रसायन का उपयोग। क्लिन जे एम सोक नेफ्रोल। 2019; 14: 306-316. क्रॉसरेफ पबमेड
[10] लिम एस. हाइपोकैलिमिया के प्रति दृष्टिकोण। एक्टा मेड इंडोन्स। 2007; 39: 56-64. PubMed
[11] नवारो-गोंजालेज जेएफ, मोरा-फर्नांडीज सी, गार्सियापेरेज़ जे। क्रोनिक रीनल फेल्योर और डायलिसिस में अव्यवस्थित मैग्नीशियम होमियोस्टैसिस के नैदानिक निहितार्थ। सेमिन डायल. 2009; 22: 37-44. क्रॉसरेफ पबमेड
[12] सेकी एन, हमानो एच, इइयामा वाई, असानो वाई, कोकुबो एस, यामूची के, तमुरा वाई, यूनिशी के, कुडोउ एच। कैल्शियम और मैग्नीशियम अवशोषण पर लैक्टुलोज का प्रभाव: वयस्क पुरुषों में स्थिर आइसोटोप का उपयोग करके एक अध्ययन। जे न्यूट्र विज्ञान विटामिनोल (टोक्यो)। 2007; 53: 5-12. क्रॉसरेफ पबमेड
[13] यालामंचिली एचबी, कैल्प-इनल एस, झोउ एक्सजे, चौधरी डी. हाइपोकैलेमिक नेफ्रोपैथी। किडनी अंतर्राष्ट्रीय प्रतिनिधि 2018; 3: 1482-1488. क्रॉसरेफ पबमेड
[14] रेउंगजुई एस, रोनकल सीए, सातो डब्ल्यू, ग्लुशकोवा ओए, क्रोकर बीपी, सुगा एस, ओयांग एक्स, तुंगसांगा के, नाकागावा टी, जॉनसन आरजे, म्यू डब्ल्यू। हाइपोकैलेमिक नेफ्रोपैथी बिगड़ा हुआ एंजियोजेनेसिस से जुड़ा है। जे एम सोक नेफ्रोल. 2008; 19: 125-134. क्रॉसरेफ पबमेड
[15] सुगा एसआई, फिलिप्स एमआई, रे पीई, रैले जेए, वियो सीपी, किम वाईजी, माज़ाली एम, गॉर्डन केएल, ह्यूजेस जे, जॉनसन आरजे। हाइपोकैलिमिया गुर्दे की चोट और वासोएक्टिव मध्यस्थों में परिवर्तन उत्पन्न करता है जो नमक संवेदनशीलता को बढ़ावा देते हैं। एम जे फिजियोल रीनल फिजियोल। 2001; 281: एफ620-एफ629. क्रॉसरेफ पबमेड
[16] सुगा एस, यासुई एन, योशिहारा एफ, होरियो टी, कवानो वाई, कांगावा के, जॉनसन आरजे। एंडोटिलिन ए रिसेप्टर नाकाबंदी और एंडोटिलिन बी रिसेप्टर नाकाबंदी विभिन्न तंत्रों द्वारा हाइपोकैलेमिक नेफ्रोपैथी में सुधार करती है। जे एम सोक नेफ्रोल. 2003; 14: 397- 406. क्रॉसरेफ पबमेड
[17] टॉलिन्स जेपी, होस्टेट्टर एमके, होस्टेट्टर टीएच। चूहे में हाइपोकैलेमिक नेफ्रोपैथी। क्रोनिक ट्यूबलर चोट में अमोनिया की भूमिका। जे क्लिन निवेश. 1987; 79: 1447-1458. क्रॉसरेफ पबमेड
[18] बोनफैंटे एल, डेविस पीए, स्पिनेलो एम, एंटोनेलो ए, डी'एंजेलो ए, सेम्प्लिसिनी ए, कैलो एल। क्रोनिक रीनल फेल्योर, एंड-स्टेज रीनल डिजीज, और गिटेलमैन सिंड्रोम में पेरिटोनियल डायलिसिस। एम जे किडनी डिस. 2001; 38: 165-168. क्रॉसरेफ पबमेड
[19] बैरेरा-चिमल जे, गिरेरड एस, जैसर एफ. मिनरलोकॉर्टिकॉइड रिसेप्टर विरोधी और किडनी रोग: पैथोफिजियोलॉजिकल आधार। किडनी इंट. 2019; 96: 302-319. क्रॉसरेफ पबमेड
[20] वॉल्श एसबी, अनविन ई, वर्गास-पुसौ आर, हाउइलियर पी, अनविन आर। क्या हाइपोकैलिमिया नेफ्रोपैथी का कारण बनता है? बार्टर या गिटेलमैन सिंड्रोम वाले रोगियों में गुर्दे की कार्यप्रणाली का एक अवलोकन संबंधी अध्ययन। क्यूजेएम. 2011; 104: 939-944. क्रॉसरेफ पबमेड
[21] रावरोट्टो वी, सिमियोनी एफ, सब्बादीन सी, पैग्निन ई, मैओलिनो जी, अरमानिनी डी, कैलो एलए। गिटेलमैन सिंड्रोम में एल्डोस्टेरोन के प्रोइन्फ्लेमेटरी/प्रोफाइब्रोटिक प्रभाव, उच्च रक्तचाप के विपरीत एक मानव मॉडल। जे एंडोक्रिनोल निवेश। 2019; 42: 521-526. क्रॉसरेफ पबमेड
[22] मेयर्स सीएम, पेराज़ेला एमए। क्रोनिक ट्यूबलोइंटरस्टीशियल रोग। इन: गिल्बर्ट एसजे, वेनर डीई (संस्करण)। किडनी रोगों पर नेशनल किडनी फाउंडेशन का प्राइमर। सातवां संस्करण. फिलाडेल्फिया, पीए: एल्सेवियर; 2018. पी. 404-411.
[23] अडिगा ए, गोल्डफार्ब डीएस। गुर्दे की बीमारी के साथ मेसालेमिन का संबंध। सलाह क्रोनिक किडनी डिस. 2020; 27: 72-76. क्रॉसरेफ पबमेड
[24] ब्रेनर बीएम, लॉलर ईवी, मैकेंज़ी एचएस। हाइपरफिल्ट्रेशन सिद्धांत: नेफ्रोलॉजी में एक आदर्श बदलाव। किडनी इंट. 1996; 49: 1774-1777. क्रॉसरेफ पबमेड
[25] हेलाल आई, फिक-ब्रोस्नाहन जीएम, रीड-गिटोमर बी, श्रियर आरडब्ल्यू। ग्लोमेरुलर हाइपरफिल्ट्रेशन: परिभाषाएँ, तंत्र और नैदानिक निहितार्थ। नेट रेव नेफ्रोल. 2012; 8: 293-300.
【संपर्क】ईमेल: george.deng@wecistanche.com / व्हाट्सएप:008613632399501/वीचैट:13632399501






