उम्र बढ़ने में प्रतिरक्षा स्मृति: माइक्रोबायोटा, मस्तिष्क, चयापचय, और एपिजेनेटिक्स 3 को कवर करने वाला एक व्यापक परिप्रेक्ष्य
Jul 08, 2022
कृपया संपर्क करेंoscar.xiao@wecistanche.comअधिक जानकारी के लिए
चयापचय और प्रतिरक्षा स्मृति की परस्पर क्रिया
चयापचय और चयापचय सूजन प्रमुख प्रक्रियाएं हैं जो उम्र बढ़ने से प्रभावित होती हैं और प्रभावित होती हैं। टाइप 2 डायबिटीज मेलिटस, हृदय रोग और मोटापा जैसे मेटाबोलिक रोग भी उम्र से संबंधित रोग माने जाते हैं। इन स्थितियों के साथ पुरानी सूजन होती है, जिसे मेटाफ्लेमेशन कहा जाता है, जो पोषक तत्वों की अधिकता से प्रेरित होता है। हालांकि ट्रिगर अलग-अलग हो सकते हैं, मेटाफ्लेमेशन और सूजन के अंतर्निहित तंत्र काफी समान हैं।

माइटोकॉन्ड्रियल डिसफंक्शन, सेन्सेंट कोशिकाओं और सेलुलर मलबे का संचय, और जन्मजात प्रतिरक्षा प्रतिक्रियाओं का अतिसक्रियकरण, जैसे कि सूजन, दोनों प्रक्रियाओं में योगदान करते हैं [120]। इसलिए, सेलुलर उम्र बढ़ने, चयापचय, और कालानुक्रमिक उम्र बढ़ने में सूजन और उम्र से संबंधित चयापचय रोगों के बीच परस्पर क्रिया को समझना महत्वपूर्ण है।
टी सेल चयापचय
मौन टी कोशिकाएं मुख्य रूप से कैटोबोलिक प्रक्रियाओं का उपयोग करती हैं, जबकि सक्रिय कोशिकाएं प्रोटीन उत्पादन और प्रसार का समर्थन करने के लिए उपचय प्रक्रियाओं पर निर्भर करती हैं। एनाबॉलिक पथों को प्रेरित करने के लिए कोशिकाओं को एक महत्वपूर्ण सेरीन / थ्रेओनीन किनसे, रैपामाइसिन (एमटीओआर) के स्तनधारी लक्ष्य को सक्रिय करने की आवश्यकता होती है। विकास और प्रसार को बढ़ावा देते हुए, एमटीओआर ग्लूकोज परिवहन और ग्लाइकोलाइसिस को भी नियंत्रित करता है।सिस्टैंच ट्यूबुलोसा खुराक redditग्लाइकोलाइसिस ऊर्जा उत्पन्न करने के मुख्य मार्गों में से एक है। हालांकि यह ऊर्जावान रूप से कुशल नहीं है - एक ग्लूकोज अणु से केवल 2 एडेनोसिन ट्राइफॉस्फेट (एटीपी) अणु उत्पन्न हो सकते हैं - यह बहुत तेजी से ऊर्जा उत्पन्न करता है, जो सक्रिय और प्रोलिफ़ेरेटिंग टी कोशिकाओं के लिए उपयोग किया जाता है [122]। ग्लूकोज के प्रसंस्करण से एटीपी प्राप्त होता है, एनएडीएच, और पाइरूवेट। पाइरूवेट को तब लैक्टेट में परिवर्तित किया जाता है और ग्लाइकोलाइसिस के मामले में लैक्टिक एसिड के रूप में निर्यात किया जाता है या अन्यथा ऑक्सीडेटिव फास्फारिलीकरण (OXPHOS) के लिए माइटोकॉन्ड्रिया में ले जाया जाता है।

अधिक जानने के लिए कृपया यहां क्लिक करें
OXPHOS एक अधिक कुशल बायोएनेरजेनिक मार्ग है, जो प्रत्येक ग्लूकोज अणु [123] से 36 एटीपी अणुओं का उत्पादन करता है। इस मामले में, पाइरूवेट एसिटाइल-सीओए में परिवर्तित हो जाता है और ट्राइकारबॉक्सिलिक एसिड चक्र (टीसीए चक्र) में प्रवेश करता है, जो इलेक्ट्रॉन दाताओं एनएडीएच और एफएडीएच 2 के माध्यम से इलेक्ट्रॉन परिवहन श्रृंखला (टीसीए) से जुड़ा होता है। टीसीए चक्र को अमीनो एसिड और फैटी एसिड के ऑक्सीकरण द्वारा फिर से भरा जा सकता है। फैटी एसिड ऑक्सीकरण (एफएओ) मुख्य रूप से कम ऊर्जा मांग वाली कोशिकाओं द्वारा उपयोग किया जाता है और सीडी 8 मेमोरी और सीडी 4 प्लस ट्रेग विकास [124] में महत्वपूर्ण भूमिका निभाता है। सक्रिय टी कोशिकाएं अपने ग्लूटामाइन तेज को बढ़ाती हैं और ग्लूटामिनोलिसिस को उपज-केटोग्लूटारेट के लिए करती हैं, जो टीसीए चक्र में प्रवेश करती है।
इसके अतिरिक्त, टीसीए चक्र मेटाबोलाइट्स ऊर्जा उत्पादन के अलावा अन्य तरीकों से प्रतिरक्षा कार्यों को नियंत्रित कर सकते हैं। उदाहरण के लिए, एसिटाइल-सीओए हिस्टोन एसिटिलीकरण [125] के लिए प्रमुख सहकारक के रूप में कार्य करता है। सक्रिय टी कोशिकाओं में, हिस्टोन एसिटिलिकेशन के माध्यम से आईएफएनवाई उत्पादन के लिए एसिटाइल-सीओए की आवश्यकता होती है [126]। एसिटाइल-सीओए माइटोकॉन्ड्रियल प्रोटीन [127] के एसिटिलीकरण में भी योगदान देता है, जिसके जन्मजात और अनुकूली प्रतिरक्षा कोशिकाओं [128] दोनों के लिए व्यापक कार्यात्मक परिणाम होते हैं।
मौन भोली टी कोशिकाएं OXPHOS [129] के साथ अपनी ऊर्जा जरूरतों को पूरा करती हैं।सिस्टैंचIL-7 और TCR सिग्नलिंग उनके चयापचय नियमन और अस्तित्व के लिए आवश्यक हैं [130, 131]। जब टी कोशिकाएं सक्रिय होती हैं, तो प्रभावकारी कार्यों और बायोमास उत्पादन के लिए ऊर्जा की तत्काल आवश्यकता होती है। कोशिकाएं ग्लूकोज ट्रांसपोर्टर 1 (GLUT1) जैसे ट्रांसपोर्टरों को अपग्रेड करती हैं और एरोबिक ग्लाइकोलाइसिस में संलग्न होती हैं, रास्ते के माध्यम से साइटोकिन उत्पादन को बढ़ावा देती हैं, जैसे कि फॉस्फॉइनोसाइटाइड 3-किनेज (PI3K) -AKT-mTOR अक्ष और माइटोजेन-सक्रिय प्रोटीन किनेज (MAPK) सिग्नलिंग [132]। प्रभावकारक कार्यों के लिए ग्लाइकोलाइटिक स्विच की आवश्यकता होती है, उदाहरण के लिए, IFNy उत्पादन, लेकिन प्रसार के लिए आवश्यक नहीं है [133]। OXPHOS का उपयोग प्रसार और उत्तरजीविता उद्देश्यों के लिए भी किया जा सकता है। हालांकि सक्रिय टी कोशिकाएं कार्यात्मक रूप से ग्लाइकोलाइसिस पर निर्भर करती हैं, ओएक्सपीएचओएस निश्चित रूप से डिस्पेंसेबल नहीं है: जब ओएक्सपीएचओएस ओलिगोमाइसिन से बाधित होता है, तो टी सेल सक्रियण और प्रसार अवरुद्ध हो जाता है [133]।
हालांकि वे आराम की स्थिति में ओएक्सपीएचओएस और एफएओ पर भरोसा करते हैं, मेमोरी टी कोशिकाओं को एंटीजन मुठभेड़ पर जल्दी और कुशलता से प्रतिक्रिया करने की आवश्यकता होती है। इसलिए, वे भोले टी कोशिकाओं की तुलना में जल्दी ग्लाइकोलाइसिस में स्थानांतरित हो सकते हैं [134]। ग्रेटर माइटोकॉन्ड्रियल द्रव्यमान और एक मजबूत माइटोकॉन्ड्रियल अतिरिक्त श्वसन क्षमता को इस बायोएनेरजेनिक लाभ [135, 136] से जोड़ा गया है। इसके अतिरिक्त, माइटोकॉन्ड्रियल फ्यूजन मेमोरी टी कोशिकाओं के विकास और कार्य के लिए आवश्यक है [137]।
टी सेल चयापचय पर उम्र बढ़ने का प्रभाव
बढ़ी हुई p38 MAPK गतिविधि सेन्सेंट टी कोशिकाओं की विशेषताओं में से एक है। p38 को रोकना एमटीओआर-स्वतंत्र तरीके से टेलोमेरेस गतिविधि, प्रसार, ऑटोफैगी और माइटोकॉन्ड्रियल फिटनेस में सुधार करता है। MAPK निषेध इन्फ्लूएंजा-टीकाकृत पुराने चूहों में टी सेल और एंटीबॉडी प्रतिक्रियाओं को भी बढ़ाता है [138]।
PI3K में गेन-ऑफ-फंक्शन म्यूटेशन वाले मरीजों में अनुभवहीन टी कोशिकाओं का क्षय होता है, लेकिन बुजुर्गों की तरह ही सेन्स-सेंट इफ़ेक्टर कोशिकाओं का एक संचय होता है [139]। रैपामाइसिन उपचार के साथ इनहिबिट-इन एमटीओआर गतिविधि इन रोगियों में सेन्सेंट फेनोटाइप को आंशिक रूप से पुनर्स्थापित करती है। इसलिए, अति सक्रिय PI3K/AKT/mTOR सिग्नलिंग को टी सेल सेनेसेंस के ड्राइवरों में से एक के रूप में सुझाया गया है।
वृद्ध भोली टी कोशिकाओं में उच्च माइटोकॉन्ड्रियल द्रव्यमान होता है, लेकिन दिलचस्प रूप से, कम माइटोकॉन्ड्रियल श्वसन क्षमता, संभवतः श्वसन श्रृंखला जीन के ट्रांसक्रिप्शनल डाउनरेगुलेशन के कारण [140]। इसके अलावा, वृद्ध भोली टी कोशिकाओं में एक-कार्बन चयापचय के एंजाइम की कमी होती है, और फॉर्मेट और ग्लाइसिन के साथ पूरक, एक-कार्बन चयापचय मेटाबोलाइट्स, सेल अस्तित्व और सक्रियण में सुधार करता है [14]।
टी सेल मेमोरी की पीढ़ी के लिए ऑटोफैगी महत्वपूर्ण है, और स्पर्मिडाइन द्वारा ऑटोफैगी को शामिल करने से वृद्ध चूहों में इन्फ्लूएंजा टीकाकरण के खिलाफ सीडी 8 प्लस टी सेल प्रतिक्रियाओं में सुधार होता है [142]। सीडी 4 प्लस मेमोरी बुजुर्गों की टी कोशिकाएं अपंजीकृत ऑक्सीडेटिव फास्फारिलीकरण, प्रतिक्रियाशील ऑक्सीजन प्रजातियों (आरओएस) उत्पादन, और फैटी एसिड ऑक्सीकरण [143] को प्रदर्शित करती हैं।bioflavonoidsयुवा कोशिकाओं की तुलना में उनके पास सिर्तुइन 1 (एसआईआरटी 1), एक एनएडी-आश्रित डीएसेटाइलेज़ की उच्च अभिव्यक्ति है। SIRT1 और AMPK, दो महत्वपूर्ण पोषक तत्व-संवेदी अणु और mTOR के नकारात्मक नियामक, एक दूसरे को सकारात्मक रूप से प्रभावित करते हैं [144]। CD4 प्लस मेमोरी कोशिकाओं के विपरीत, उम्र बढ़ने से जुड़ी टर्मिनली विभेदित मेमोरी CD8 प्लस CD28-T कोशिकाओं में एक उच्च ग्लाइकोलाइटिक क्षमता, जो उनकी डाउनग्रेड की गई SIRTI अभिव्यक्ति [145] से जुड़ी है।
CD8 प्लस TEMRA कोशिकाओं में ग्लाइकोलाइसिस और ग्लूटामिनोलिसिस-संबंधित जीन की उच्च अभिव्यक्ति होती है और भोले और EM कोशिकाओं की तुलना में एक बड़ा ATP पूल होता है [146]। TEMRA कोशिकाओं में अपग्रेडित ग्लाइकोलाइटिक प्रतिलेखन के बावजूद, बेसल ग्लाइकोलाइसिस का स्तर भोले और EM कोशिकाओं के समान है। EM कोशिकाओं की तरह, TEMRA कोशिकाएं सक्रिय होने पर ग्लाइकोलाइसिस और OXPHOS को तेजी से बढ़ा सकती हैं [146]। कार्य के संदर्भ में, TEMRA कोशिकाएँ साइटोटोक्सिसिटी और साइटोकिन उत्पादन में सक्षम हैं, उनके जीर्ण अवस्था और बिगड़ा माइटोकॉन्ड्रियल फ़ंक्शन [17, 36] के बावजूद।
लंबे समय तक सीएमवी संक्रमण, जो प्रतिरक्षा को बढ़ावा देने के लिए जाना जाता है, टी कोशिकाओं के सेलुलर चयापचय को भी बदलता है, ग्लूकोज तेज बढ़ाता है, ग्लाइकोलाइसिस को बढ़ावा देता है, लिपिड राफ्ट का पुनर्गठन करता है, और कोलेस्ट्रॉल चयापचय को परेशान करता है [147, 148]। इसके अलावा, आजीवन सीएमवी के कारण पुरानी सूजन। संक्रमण अग्नाशय-कोशिकाओं को बाधित करता है और बुजुर्गों में टाइप 2 मधुमेह के जोखिम को बढ़ाता है [149]।
बी सेल चयापचय
टी कोशिकाओं को विनियमित करने वाले चयापचय मार्ग भी बी सेल फ़ंक्शन के लिए आवश्यक हैं, हालांकि बी सेल चयापचय पर बहुत अधिक शोध नहीं हुआ है। जब बीसीआर और टी सेल सहायता द्वारा प्रतिजन मान्यता पर एक बी सेल सक्रिय होता है, तो यह पीआई 3 के / एकेटी / एमटीओआर सिग्नलिंग को सक्रिय करता है [150]। सक्रिय टी कोशिकाओं की तरह, सक्रिय बी कोशिकाओं को बायोमास और प्रसार को बढ़ाने के लिए तेजी से ऊर्जा उत्पादन की आवश्यकता होती है। नतीजतन, ऑक्सीजन की खपत, OXPHOS, और माइटोकॉन्ड्रियल रीमॉडेलिंग [151] के साथ-साथ ग्लूकोज और ग्लूटामाइन तेज बढ़ जाता है। OXPHOS और TCA चक्र के ग्लूटामाइन-ईंधन को B कोशिका वृद्धि और कार्य के लिए महत्वपूर्ण बायोएनेरजेनिक मार्ग के रूप में सुझाया गया है, जबकि ग्लूकोज डिस्पेंसेबल था [152]।
एक अध्ययन से पता चला है कि सक्रिय बी कोशिकाओं में माइटोकॉन्ड्रिया अधिक होते हैं लेकिन माइटोकॉन्ड्रियल डीएनए की समान मात्रा होती है, यह दर्शाता है कि माइटोकॉन्ड्रियल प्रतिकृति के बजाय कई न्यूक्लियॉइड के साथ भोले बी सेल माइटोकॉन्ड्रिया का विखंडन सक्रियण पर होता है [152]। एक अन्य अध्ययन ने सुझाव दिया कि माइटोकॉन्ड्रियल रीमॉडेलिंग और आरओएस स्तर सक्रिय बी कोशिकाओं के भाग्य का निर्धारण करते हैं। सक्रियण पर बढ़े हुए माइटोकॉन्ड्रियल द्रव्यमान और उच्च आरओएस स्तर वाली कोशिकाओं को वर्ग स्विच पुनर्संयोजन के लिए नियत किया जाता है, जबकि घटी हुई माइटोकॉन्ड्रियल द्रव्यमान वाली कोशिकाएं प्लाज्मा सेल भेदभाव से गुजरती हैं [153]।
जीसी में सक्रिय बी कोशिकाओं की ऊर्जा की जरूरतें अक्सर बदल जाती हैं [154]।कितना सिस्टैंच लेना हैहाइपोक्सिक प्रकाश क्षेत्र में, कोशिकाएं कम ऑक्सीजन की खपत करती हैं और अधिक ग्लाइकोलाइटिक होती हैं। यहां ग्लाइकोलाइसिस के नियमन के लिए mTORC1 आवश्यक नहीं है, लेकिन यह कोशिकाओं के सकारात्मक चयन और अंधेरे क्षेत्र में प्रवास के लिए c-Myc के साथ मिलकर महत्वपूर्ण है। प्रसार और दैहिक अतिपरिवर्तन के लिए [155,156]।

सिस्टैन्च एंटी-एजिंग कर सकता है
जीसी परिपक्वता पर, जब एक कोशिका मेमोरी बी कोशिकाओं में अंतर करती है, तो चयापचय अवस्था प्रमुख OXPHOS के साथ अधिक मौन हो जाती है। हालांकि, एमटीओआरसी1 और ग्लाइकोलाइसिस का तेजी से पुन: सक्रियण एंटीबॉडी-उत्पादक प्लास्मबलास्ट में बाद में विभेदन के लिए संभव है।[157]। इसके अलावा, मेमोरी बी कोशिकाओं में उच्च बेसल ऑटोफैगी होती है, जो एंटीजन मुठभेड़ों [158,159] तक उनके अस्तित्व के लिए आवश्यक है।
जीसी लंबे समय तक चलने वाली प्लाज्मा कोशिकाओं का भी उत्पादन करते हैं, जो प्रति सेकंड हजारों एंटीबॉडी का उत्पादन कर सकते हैं। यह, स्वाभाविक रूप से, अत्यधिक ऊर्जा की मांग है। प्लाज्मा सेल निर्माण और एंटीबॉडी संश्लेषण [160] के लिए एमटीओआरसी 1 आवश्यक है। प्लाज्मा कोशिकाओं में ग्लूकोज का उच्च स्तर होता है, लेकिन अधिकांश ग्लूकोज का उपयोग प्रोटीन ग्लाइकोसिलेशन [161] के लिए किया जाता है। फिर भी, जब ग्लूकोज ट्रांसपोर्टर ग्लूट को हटा दिया गया तो प्लाज्मा कोशिकाओं का अस्तित्व और एंटीबॉडी उत्पादन बिगड़ा हुआ था [162]। इसके अलावा, ग्लाइकोलाइसिस द्वारा प्रदान किए गए पाइरूवेट का माइटोकॉन्ड्रियल आयात, प्लाज्मा कोशिकाओं के दीर्घकालिक रखरखाव के लिए महत्वपूर्ण है [161]।
अंत में, ऊतक-निवासी बी 1 बी कोशिकाएं ग्लाइकोलाइसिस और ओएक्सपीएचओएस में अन्य बी कोशिकाओं, शास्त्रीय एंटी-बॉडी-उत्पादक और मेमोरी बी कोशिकाओं की तुलना में अधिक सक्रिय हैं। इसके अलावा, ऑटोफैगी माइटोकॉन्ड्रियल फ़ंक्शन और बी 1 कोशिकाओं के स्व-नवीकरण के लिए महत्वपूर्ण है [163]।
बी सेल चयापचय पर उम्र बढ़ने का प्रभाव
बी सेल चयापचय को कैसे नियंत्रित किया जाता है और जीवों की उम्र के रूप में कार्य को प्रभावित करता है, इस पर कम साहित्य है। एक अध्ययन से पता चला है कि वृद्ध व्यक्तियों की एंटीबॉडी-स्रावित बी कोशिकाओं में SIRTI अभिव्यक्ति कम थी, और उच्च SIRT1 स्तर कई इन्फ्लूएंजा वायरस उपभेदों [164] के लिए बेहतर एंटीबॉडी प्रतिक्रिया से जुड़े थे। इसके अलावा, बुजुर्गों की भोले और सक्रिय बी कोशिकाओं में ग्लाइकोलाइटिक क्षमता थोड़ी कम थी और OXPHOS में अधिक उल्लेखनीय कमी थी। चूहों में, वृद्ध B कोशिकाओं में उनके युवा समकक्षों के समान ग्लाइकोलाइसिस और OXPHOS दर थे, लेकिन उत्तेजना पर OXPHOS को और नहीं बढ़ा सकते थे [165] . हालांकि, कोशिकाएं अपनी ऊर्जा की जरूरत को पूरा करने के लिए ग्लाइकोलाइसिस को बढ़ाने में सक्षम थीं।
लेप्टिन, एडिपोसाइट्स द्वारा स्रावित एक प्रो-इंफ्लेमेटरी हार्मोन, मोटे व्यक्तियों [166] के संचलन में अधिक होता है। गैर-मोटे लोगों में, बुजुर्गों में लेप्टिन सांद्रता आश्चर्यजनक रूप से अधिक बढ़ जाती है [167]। सीरम में लेप्टिन की प्रचुरता भी सकारात्मक रूप से कमजोरियों से जुड़ी है[168]। लेप्टिन के संपर्क में आने के बाद, युवा दुबले व्यक्तियों की बी कोशिकाएं ट्रांसक्रिप्शनल प्रोफाइल और एंटीबॉडी स्राव [167] के संबंध में पुराने दुबले और युवा मोटे व्यक्तियों की बी कोशिकाओं के समान प्रोफ़ाइल प्रदर्शित करती हैं। लेप्टिन इन विट्रो में बी कोशिकाओं से इन्फ्लूएंजा-विशिष्ट एंटीबॉडी उत्पादन को भी कम करता है। मोटापा टीकाकरण के लिए बी सेल प्रतिक्रियाओं को कम करने के लिए जाना जाता है, और अध्ययनों से पता चलता है कि लेप्टिन इसके लिए आंशिक रूप से जिम्मेदार हो सकता है [169]।
इसके अतिरिक्त, एंटीबॉडी के पोस्ट-ट्रांसक्रिप्शनल ग्लाइकोसिलेशन उनके कार्य को नियंत्रित करते हैं, और परिवर्तित ग्लाइकोसिलेशन पैटर्न को उम्र बढ़ने से जोड़ा गया है [170,171]। 4-गैलेक्टोसिलट्रांसफेरेज गतिविधि उम्र के साथ बढ़ जाती है [172], जिसके कार्यात्मक परिणाम होंगे, हालांकि अभी तक इसका पता नहीं चला है।
प्रशिक्षित प्रतिरक्षा में चयापचय
मेटाबोलिक रिप्रोग्रामिंग क्रोमेटिन रीमॉडेलिंग के साथ-साथ प्रशिक्षित प्रतिरक्षा (जिसे जन्मजात प्रतिरक्षा स्मृति के रूप में भी जाना जाता है) में अंतर्निहित प्रमुख तंत्रों में से एक है। वास्तव में, चयापचय परिवर्तन एपिजेनेटिक परिवर्तन को प्रेरित कर सकते हैं क्योंकि कुछ मेटाबोलाइट्स, जैसे, एसिटाइल-सीओए, एपिजेनेटिक एंजाइमों को विनियमित कर सकते हैं [173]। Fumarate एपिजेनेटिक परिवर्तनों को चलाने वाले TCA मेटाबोलाइट्स का एक उदाहरण है। यह अपने आप में प्रशिक्षित प्रतिरक्षा को प्रेरित कर सकता है, और इस प्रक्रिया के दौरान इसका संचय IL-6 और TNF [104] के प्रमोटरों में हिस्टोन 3 लाइसिन 4 के ट्राइमेथिलेशन को प्रेरित करता है। यह लाइसिन-विशिष्ट हिस्टोन डेमिथाइलस KDM5 की गतिविधि को बाधित करने वाले फ्यूमरेट के कारण है।
AKT/mTOR/HIFl पाथवे -ग्लूकेन-प्रशिक्षित मोनोसाइट्स में एरोबिक ग्लाइकोलाइसिस को प्रेरित करने के लिए सबसे महत्वपूर्ण मार्ग है [174]। -ग्लूकेन-प्रेरित प्रशिक्षित प्रतिरक्षा के विपरीत, बीसीजी न केवल ग्लाइकोलाइसिस बल्कि ओएक्सपीएचओएस [175] को भी नियंत्रित करता है। ग्लूटामिनोलिसिस और कोलेस्ट्रॉल संश्लेषण -ग्लूकेन-प्रेरित प्रशिक्षित प्रतिरक्षा [104] के लिए अन्य महत्वपूर्ण चयापचय मार्ग हैं। इन मार्गों को बाधित करना इन प्रक्रियाओं को इन विट्रो और विवो में अवरुद्ध करता है। बीसीजी ग्लूटामिनोलिसिस को भी प्रेरित करता है, और प्रशिक्षित प्रतिक्रिया के लिए ग्लूटामाइन की उपलब्धता महत्वपूर्ण है [175]।

प्रशिक्षित प्रतिरक्षा के लिए कोलेस्ट्रॉल का संश्लेषण ही आवश्यक नहीं है, बल्कि मध्यवर्ती मेवलोनेट का संचय है। मेवलोनेट पीढ़ी को अवरुद्ध करना प्रशिक्षित प्रतिरक्षा को रोकता है, जबकि अकेले मेवलोनेट इंसुलिन जैसे विकास कारक 1 (IGF1) रिसेप्टर और mTOR [176] के सक्रियण के माध्यम से मोनोसाइट्स में प्रशिक्षित प्रतिरक्षा को प्रेरित कर सकता है।एक सिस्टैंच क्या है?इसके अलावा, ग्लाइकोलाइसिस और मेवलोनेट मार्ग में परिवर्तन न केवल मोनोसाइट्स में बल्कि एचएसपीसी में भी देखे जाते हैं [108]।
oxLDL, जन्मजात प्रतिरक्षा स्मृति का एक गैर-माइक्रोबियल संकेतक, ग्लाइकोलाइसिस और ऑक्सीजन की खपत दोनों को बढ़ाता है, और उच्च ग्लूकोज उपलब्धता प्रशिक्षित प्रतिरक्षा प्रतिक्रिया को और बढ़ाती है [103]। इसी तरह, कैटेकोलामाइन-प्रेरित प्रशिक्षित प्रतिरक्षा के साथ ग्लाइकोलाइसिस और ऑक्सीजन की खपत में वृद्धि होती है। ध्यान दें, जन्मजात प्रतिरक्षा स्मृति के विभिन्न संकेतकों के लिए विशेष रूप से चयापचय रीवायरिंग भिन्न हो सकती है। उदाहरण के लिए, एल्डोस्टेरोन के साथ उत्तेजना ऊंचा ग्लाइकोलाइसिस या ओएक्सपीएचओएस से जुड़ी नहीं है, लेकिन फैटी एसिड संश्लेषण [177] पर निर्भर है।
अभी तक, प्रशिक्षित प्रतिरक्षा प्रतिक्रिया और संबंधित चयापचय अवस्थाओं को उम्र बढ़ने के संदर्भ में चित्रित नहीं किया गया है। हालांकि, बुजुर्गों में बीसीजी टीकाकरण के कई चल रहे बड़े पैमाने पर अध्ययन जल्द ही वृद्ध प्रतिरक्षा कोशिकाओं (एनसीटी04537663, एनसीटी04417335) के चयापचय पर बीसीजी-प्रेरित प्रशिक्षित प्रतिरक्षा के प्रभावों पर प्रकाश डालेंगे।
प्रतिरक्षा स्मृति में एपिजेनेटिक परिवर्तन की भूमिका
एपिजेनेटिक परिवर्तनों में हिस्टोन संशोधन और डीएनए मिथाइलेशन शामिल हैं जो एक जीन के काम करने के तरीके को नियंत्रित करते हैं। ये संशोधन गतिशील हैं और जीवन भर सभी कोशिकाओं और ऊतकों को प्रभावित करते हैं। पर्यावरण और जीवन शैली, साथ ही उम्र बढ़ने से नाटकीय एपिजेनेटिक परिवर्तन हो सकते हैं। इस समीक्षा के प्रयोजन के लिए, हम इस बात पर ध्यान केंद्रित करेंगे कि आयु-निर्भर एपिजेनेटिक संशोधन कैसे सहज और अनुकूली प्रतिरक्षा स्मृति को बदलते हैं।
अनुकूली प्रतिरक्षा में डीएनए मिथाइलेशन
डीएनए मिथाइलेशन सबसे प्रचुर मात्रा में एपिजेनेटिक संशोधन है जो मिथाइल समूह को साइटोसिन [178] के 5 वें कार्बन में स्थानांतरित करके होता है। डीएनए मिथाइलेशन हमेशा कम जीन अभिव्यक्ति का संकेत नहीं देता है; हालांकि, जीन प्रमोटरों में मिथाइलेशन आमतौर पर खराब TF बाइंडिंग और कम ट्रांसक्रिप्शन [179] से जुड़ा होता है। जैविक सेक्स, आनुवंशिक पृष्ठभूमि, पर्यावरणीय कारक और उम्र डीएनए मिथाइलेशन प्रोफाइल [180] को प्रभावित करते हैं। इन कारकों में, आयु-निर्भर मेथिलिकरण बहुत अच्छी तरह से विशेषता है। उल्लेखनीय रूप से, विभिन्न ऊतकों या कोशिकाओं [180-182] से कुछ CpG साइटों के मिथाइलेशन स्तरों के आधार पर जैविक आयु की भविष्यवाणी करने के लिए विभिन्न गणितीय मॉडल विकसित किए गए हैं।
बढ़ती उम्र डीएनए [183] पर मिथाइलेशन के निशान के प्रगतिशील नुकसान के साथ जुड़ी हुई है, हालांकि कुछ जीन प्रमोटरों [184] में असामान्य हाइपरमेथिलेशन पैटर्न भी देखे जाते हैं। मिथाइलेशन परिदृश्य में परिवर्तन सीडी4 प्लस टी कोशिकाओं में सीडी28 सह-उत्तेजक प्रोटीन का नुकसान है, जो अच्छी तरह से विशेषता उम्र बढ़ने के निशान में से एक है, जिससे बिगड़ा हुआ टी सेल सक्रियण और भेदभाव होता है। सीडी28 प्लस और सीडी28"एल टी कोशिकाओं के मिथाइलेशन प्रोफाइल की तुलना से पता चला कि 296 अलग-अलग मिथाइलेटेड जीन खराब टीसीआर सिग्नलिंग और साइटोटोक्सिक प्रतिक्रिया से जुड़े हैं। कि इन कोशिकाओं में एक उच्च पूर्व-सक्रियण अवस्था है। एक अन्य अध्ययन में बताया गया है कि मध्यम और वृद्धावस्था समूहों में सीडी 4 प्लस टी कोशिकाओं के BACH2 स्थान पर मिथाइलेशन में वृद्धि से BACH2 अभिव्यक्ति कम होती है [195]। BACH2 की प्रतिरक्षा में एक नियामक भूमिका है प्रतिक्रियाओं, सीडी4 प्लस टी सेल भेदभाव को संशोधित करना और सूजन को नियंत्रित करना [196] कुल मिलाकर, डीएनए मिथाइलेशन पैटर्न में परिवर्तन सीडी 4 प्लस टी कोशिकाओं में बुजुर्गों में अधिक सूजन बनने में योगदान करते हैं।
कुछ अध्ययनों ने सक्रियण और रोगों के दौरान बी कोशिकाओं के डीएनए मिथाइलेशन प्रोफाइल पर प्रकाश डाला [197-200]; हालाँकि, बी कोशिकाएँ आयु-निर्भर मेथिलिकरण परिवर्तनों से प्रभावित होती हैं या नहीं यह ज्ञात होना बाकी है।
अनुकूली प्रतिरक्षा में हिस्टोन संशोधन
एन-टर्मिनल हिस्टोन पूंछ एसिटिलीकरण, मिथाइलेशन, फॉस्फोराइलेशन, सर्वव्यापकता, और सम्मोहन [201] सहित पोस्ट-ट्रांसलेशनल एंजाइमेटिक संशोधनों के लिए लक्ष्य हैं; हालांकि, यह समीक्षा मिथाइलेशन और एसिटिलिकेशन पर ध्यान केंद्रित करेगी, जो हिस्टोन संरचना को विनियमित करने वाले सबसे अच्छी तरह से विशेषता वाले परिवर्तन हैं। मिथाइल समूहों को हिस्टोन मिथाइलट्रांसफेरेज़ द्वारा हिस्टोन में जोड़ा जाता है और हिस्टोन डेमिथाइलिस [202] द्वारा हटा दिया जाता है। हिस्टोन 3 लाइसिन 4 (H3K4me3), हिस्टोन 3 लाइसिन 36 (H3K36), और हिस्टोन 3 लाइसिन 79 (H3K79) का ट्राइमेथिलेशन खुले और सक्रिय रूप से लिखित क्षेत्रों [203] से जुड़ा हुआ है। दूसरी ओर, हिस्टोन 3 लाइसिन 9 (H3K9me), हिस्टोन 3 लाइसिन 27 (H3K27me), और हिस्टोन 4lysine 20 (H4K20me) का मोनो-मिथाइलेशन बंद और निष्क्रिय क्रोमैटिन क्षेत्रों से जुड़ा है। इसके अलावा, हिस्टोन एसिटिलीकरण ढीले क्रोमैटिन संरचना और बढ़े हुए जीन प्रतिलेखन [204] के साथ जुड़ा हुआ है। हिस्टोन एसिटाइलट्रांसफेरेज़ लाइसिन एसिटिलीकरण को उत्प्रेरित करते हैं, जबकि हिस्टोन डेसीटाइलिस (एचडीएसी) संशोधन को उलट देते हैं [205]। हिस्टोन के पोस्ट-ट्रांसलेशनल संशोधन न केवल जीन की पहुंच और प्रतिलेखन को प्रभावित करते हैं बल्कि वैकल्पिक स्प्लिसिंग, डीएनए प्रतिकृति और मरम्मत [206] को भी संशोधित करते हैं। हिस्टोन पर हिस्टोन और एपिजेनेटिक निशान उम्र बढ़ने के साथ संक्रमण से गुजरते हैं। पुराने चूहों के HSCs में युवा HSCs [186] की तुलना में अधिक H3K4me3 और H3K27me3 चोटियाँ हैं। इसके अलावा, FLT3 की अभिव्यक्ति, CLPs के नियामकों में से एक, पुराने HSCs में H3K27me3 के कारण कम हो गई थी, जो खराब लिम्फोइड विभेदन क्षमता के बीच एक कड़ी का सुझाव देती है। बुजुर्गों में एचएससी की। युवा और बूढ़े मोनोज़ायगोटिक जुड़वाँ पर किए गए एक व्यापक अध्ययन से पता चला है कि उम्र बढ़ने के दौरान क्रोमैटिन संशोधन गैर-आनुवांशिक हैं [207]। इसके अलावा, हिस्टोन संशोधन प्रोफाइल कुछ हद तक, युवा व्यक्तियों में समरूप और बुजुर्ग विषयों में विषम हैं। व्यक्तियों और बुजुर्गों में कोशिका प्रकारों के बीच हिस्टोन संशोधनों में विषमता देखी गई।

एपिजेनेटिक परिवर्तन बुजुर्गों के सीडी 8 प्लस टी कोशिकाओं में देखे जाने वाले प्रमुख दोषों के अंतर्निहित कारणों में से एक हैं। युवा [208] की तुलना में बुजुर्गों में टी सेल सिग्नलिंग से संबंधित जीन के एन्हांसर और प्रमोटर क्षेत्रों में अधिक बंद क्रोमैटिन क्षेत्र देखे जाते हैं। इसके अलावा, -7R, मेमोरी सीडी8 प्लस टी कोशिकाओं में, बुजुर्गों में कई बंद क्रोमैटिन चोटियों से संबंधित शीर्ष जीनों में से एक है। चूंकि आईएल -7 होमोस्टैसिस और टी और बी कोशिकाओं के रखरखाव को सुनिश्चित करता है, बुजुर्गों में खराब आईएल -7 संकेतन बिगड़ा हुआ अनुकूली प्रतिरक्षा प्रतिक्रिया [209] का एक अंतर्निहित कारण हो सकता है। इसके अलावा, बुजुर्गों में भोले CD8 प्लस कोशिकाओं में खराब परमाणु श्वसन कारक 1 (NRF1) बाइंडिंग [140] से जुड़े जीन प्रमोटरों में क्रोमेटिन की पहुंच कम होती है। ऑक्सीडेटिव फास्फारिलीकरण में NRF1 की भूमिका को ध्यान में रखते हुए, घटी हुई क्रोमेटिन गतिविधि बुजुर्गों में बिगड़ा हुआ CD8 T सेल चयापचय को आंशिक रूप से समझा सकती है [210]। अध्ययन के अन्य महत्वपूर्ण निष्कर्ष यह हैं कि खुले क्रोमैटिन क्षेत्र मेमोरी सेल प्रोफाइल से जुड़े होते हैं, और वृद्ध व्यक्तियों में प्रमोटरों की पहुंच कम हो जाती है।
जैसा कि डीएनए मेथिलिकरण अनुभाग में उल्लेख किया गया है, BACH2 अभिव्यक्ति में उम्र से संबंधित कमी सीडी 4 प्लस टी कोशिकाओं में देखी गई है। एक अन्य तंत्र जो BACH2 जीन प्रतिलेखन को कम करता है, वह मेनिन की कमी के कारण है जो प्रतिरक्षा में कमी [211] में देखी गई है। मेनिन अपने ठिकाने से बंध कर और हिस्टोन एसिटिलीकरण को बनाए रखते हुए BACH2 अभिव्यक्ति को प्रेरित करता है। मेनिन के BACH2 ठिकाने के बंधन में कमी और बाद में कम BACH2 अभिव्यक्ति CD4 प्लस T कोशिकाओं में प्रतिरक्षण में योगदान करती है। पुराने और युवा चूहों में बी सेल अग्रदूतों में एपिजेनेटिक परिवर्तनों की जांच करने वाले एक अध्ययन ने इन परिवर्तनों को जीन अभिव्यक्तियों के साथ जोड़ा [212]। इससे पता चला कि वृद्ध प्री-बी कोशिकाएं इंसुलिन रिसेप्टर सब्सट्रेट 1 (आईआरएसआई) के प्रमोटर साइट पर H3K4me3 की हानि प्रदर्शित करती हैं, जो कम ट्रांसक्रिप्शन से जुड़ी होती है। चूंकि अस्थि मज्जा में बी कोशिकाओं के विकास के लिए इंसुलिन संकेतन आवश्यक है [213], कम इंसुलिन वृद्धि कारक (आईजीएफ) संकेतन से बी कोशिका के विकास में दोष हो सकते हैं।
प्रशिक्षित प्रतिरक्षा की पहचान के रूप में एपिजेनेटिक रिप्रोग्रामिंग
एक अलग एपिजेनेटिक प्रोफ़ाइल पहले अपमान के बाद प्रशिक्षित प्रतिरक्षा प्रतिक्रियाओं को नियंत्रित करती है। कुछ संक्रमणों या उत्तेजनाओं के परिणामस्वरूप, प्राइमेड कोशिकाएं एक एपिजेनेटिक रिप्रोग्रामिंग से गुजरती हैं जो उन्हें सूजन और चयापचय से संबंधित जीनों के प्रतिलेखन की सुविधा के द्वारा एक विषम संक्रमण पर मजबूत प्रतिक्रिया देने की अनुमति देती है [106]।
H3K4me3 -ग्लूकेन उपचार के बाद मोनोसाइट्स में पहला विशिष्ट एपिजेनेटिक चिह्न है [91]। आगे के विश्लेषण से पता चला कि H3K4me3 चोटियाँ TNF, IL6, IL18, DESTINY और MYD88 जीन के प्रमोटर साइटों पर समृद्ध हैं, यह दर्शाता है कि इन क्षेत्रों में जीन ट्रांसक्रिप्शन अधिक सक्रिय हैं। इसके अलावा, बढ़ा हुआ H3K27ac प्रशिक्षित कोशिकाओं में एक अच्छी तरह से चित्रित हिस्टोन चिह्न है, जो ग्लाइकोलाइसिस और PI3K/AKT मार्ग सक्रियण को बढ़ावा देता है [174, 214]। H3K4me3 और H3K27ac में संवर्धन के अलावा, घटी हुई H3K9me3 साइटोकाइन उत्पादन और ग्लाइकोलाइसिस [175] से संबंधित जीन के प्रमोटरों में पाई गई। चूंकि H3K9me3 एक दमनकारी चिह्न है, कम ट्राइमेथिलेशन खुले क्रोमैटिन क्षेत्रों की उपस्थिति का सुझाव देता है। इन अध्ययनों से पता चलता है कि प्रशिक्षित प्रतिरक्षा प्रतिक्रियाएं एपिजेनेटिक संशोधनों द्वारा संशोधित होती हैं जो बढ़ी हुई साइटोकिन प्रतिक्रियाओं और विशिष्ट चयापचय परिवर्तनों की सुविधा प्रदान करती हैं। प्रशिक्षित कोशिकाएं एक सामान्य एपिजेनेटिक प्रोफ़ाइल साझा करती हैं; हालाँकि, विभिन्न उत्तेजनाओं से मामूली अद्वितीय एपिजेनेटिक परिवर्तन हो सकते हैं।
संक्रमण और कुछ उत्तेजनाएं जन्मजात प्रतिरक्षा कोशिकाओं के डीएनए मिथाइलेशन प्रोफाइल, साथ ही हिस्टोन पर निशान छोड़ती हैं [215]। अध्ययन बीसीजी टीकाकरण के बाद एंटी-माइकोबैक्टीरियम प्रतिक्रिया में डीएनए मेथिलिकरण की भूमिका को प्रदर्शित करता है, गैर-उत्तरदाताओं से भेदभाव करने वाले उत्तरदाताओं [216,217]। बीसीजी टीकाकरण के उत्तरदाताओं को भड़काऊ जीन [216] के प्रमोटरों में कम डीएनए मेथिलिकरण की विशेषता थी। हालांकि, क्या डीएनए (डी) मिथाइलेशन गैर-विशिष्ट सुरक्षात्मक प्रतिक्रियाओं के विकास में प्रत्यक्ष भूमिका निभाता है, इसकी अभी भी जांच की जा रही है।
वयस्कों की तरह, बुजुर्गों में हिस्टोन संशोधनों द्वारा प्रशिक्षित प्रतिरक्षा को संशोधित किया जाता है। Giamarellos-Bourboulis और उनके सहयोगियों ने हाल ही में दिखाया कि बुजुर्गों में BCG टीकाकरण पर साइटोकिन उत्पादन में वृद्धि TNF और IL6 जीन [113] के प्रमोटर क्षेत्रों में H3K27 के एसिटिलीकरण के साथ हुई थी। हालांकि, वयस्कों और वृद्ध व्यक्तियों के बीच जन्मजात प्रतिरक्षा स्मृति विकास के बाद एपिजेनेटिक मतभेदों की तुलना करने और प्रशिक्षित प्रतिरक्षा के संदर्भ में उम्र बढ़ने से एपिजेनेटिक निशान कैसे प्रभावित होते हैं, इसका पता लगाने के लिए आगे के अध्ययनों को वारंट किया गया है।
आंत माइक्रोबायोटा मॉड्यूलेटिंग इम्यून मेमोरी
उम्र बढ़ने के कारण मनुष्य के पूरे शरीर में परिवर्तन होते हैं, और वहाँ रहने वाले खरबों रोगाणुओं को कोई छूट नहीं है। आंत माइक्रोबायोटा की संरचना और विविधता गतिशील रूप से शैशवावस्था में बदल जाती है, वयस्कता के दौरान अपेक्षाकृत स्थिर रहती है, और बुढ़ापे के साथ घटने लगती है [218]।
माइक्रोबायोटा और अनुकूली प्रतिरक्षा प्रणाली की सहभागिता
एक निश्चित स्तर की प्रतिरक्षा प्रतिक्रिया को प्रेरित करके और सूजन को ठीक करके अनुकूली प्रतिरक्षा प्रणाली को शिक्षित करने में आंत माइक्रोबायोटा की आवश्यक भूमिका होती है। उदाहरण के लिए, बैक्टेरॉइड्स फ्रैगिलिस, आंत में एक सहभोज, सीडी 4 प्लस टी सेल भेदभाव को टी हेल्पर 1 (थ 1) और थ 2 [219] में बढ़ाता है और नियंत्रित करता है। आंत बैक्टीरिया और टीजीएफ की उपस्थिति में, भोले सीडी 4 प्लस टी कोशिकाएं ट्रेग बन जाती हैं, प्रतिरक्षा होमियोस्टैसिस को बनाए रखने के लिए आईएल -10 का उत्पादन। दूसरी ओर, आंत के लिम्फोइड फॉलिकल्स में Tregs और Th17 कोशिकाएं B सेल वर्ग स्विचिंग को प्रेरित करती हैं, जिसके परिणामस्वरूप IgA स्राव होता है [220,221]। बी कोशिकाओं से माइक्रोबायोटा से जुड़े आईजीए, आईजीएम और आईजीजी स्राव भी टी सेल सहायता के बिना टीएलआर सिग्नलिंग सक्रियण के माध्यम से होते हैं [22]।
अनुकूली प्रतिरक्षा प्रणाली जन्मजात प्रतिरक्षा प्रणाली द्वारा मध्यस्थता वाले कमैंसल आंत रोगाणुओं के खिलाफ भड़काऊ प्रतिक्रिया को सीमित कर सकती है। बी कोशिकाओं द्वारा उत्पादित आईजीए को स्थायी मेजबान-सूक्ष्मजीव बातचीत के एक भाग के रूप में समझाया गया है, जो लाभकारी सूक्ष्मजीवों के खिलाफ भड़काऊ प्रतिक्रिया को नियंत्रित करता है [223]। इसके अलावा, आंतों के Treg कोशिकाएं आंतों के प्रतिजनों के लिए TCRs को व्यक्त करती हैं, जैसे कि चयापचय उत्पाद और कमेंसल्स, जबकि शरीर में अन्य Tregs स्व-प्रतिजनों के लिए TCRs व्यक्त करते हैं [224]। इस तरह, आंतों के Tregs आंतों के प्रतिजनों के खिलाफ प्रतिरक्षा प्रतिक्रिया को दबाते हैं और एक प्रतिरक्षा नियामक खेलते हैं। आंत में भूमिका।
माइक्रोबायोटा कैसे अनुकूली प्रतिरक्षा प्रणाली के विकास को आश्चर्यजनक रूप से आकार देता है, यह रोगाणु-मुक्त चूहों में भी प्रदर्शित किया गया था: आंत में माइक्रोबियल प्रजातियों की कमी माध्यमिक लिम्फोइड ऊतक विकास [225], और कम आईजीए उत्पादन [226] में दोषों की विशेषता है, और कम Th17 कोशिकाओं और Tregs [227]। यह ध्यान दिया जाना चाहिए कि आंत में माइक्रोबियल प्रजातियों द्वारा उत्पादित शॉर्ट-चेन फैटी एसिड (एससीएफए) प्रतिरक्षा प्रणाली के विकास और प्रतिक्रियाओं में बहुत योगदान देते हैं [228]।
व्यक्तियों को बीमारियों से बचाने के लिए एक स्वस्थ आंत माइक्रोबायोटा संरचना महत्वपूर्ण है। एक उदाहरण के रूप में, आईएल -10 आईजीए प्लस प्लाज्मा कोशिकाओं को स्रावित करता है और आंत में उत्पन्न होने वाले प्लास्मबलास्ट चूहों में प्रेरित प्रायोगिक ऑटोइम्यून एन्सेफेलोमाइलाइटिस के लिए प्रतिरोध प्रदान करते हैं [229]। एक अन्य अध्ययन में बताया गया है कि आंत माइक्रोबायोटा जीएम-सीएसएफ और आईएल -17 एक स्राव [230] को प्रेरित करके एसपी न्यूमोनिया और के। न्यूमोनिया से प्रेरित श्वसन संक्रमण से बचाता है।
उम्र बढ़ने में डिस्बिओसिस की भूमिका
आंत डिस्बिओसिस की घटना, माइक्रोबियल प्रजातियों का असंतुलन, उम्र के साथ बढ़ता है और कई स्वास्थ्य समस्याओं से जुड़ा होता है [231]। हालांकि, यह स्पष्ट नहीं है कि उम्र बढ़ने के दौरान प्रतिरक्षा कोशिकाओं के सेलुलर और आणविक परिवर्तन आंत माइक्रोबायोटा की संरचना और कामकाज को प्रभावित करते हैं, या यदि उम्र से संबंधित डिस्बिओसिस दोषपूर्ण प्रतिरक्षा प्रतिक्रियाओं को ट्रिगर करता है। यह संभावना है कि दोनों समवर्ती रूप से सत्य हैं, लेकिन इस प्रश्न को हल करने के लिए आंत माइक्रोबायोटा-प्रतिरक्षा प्रणाली की बातचीत की बेहतर समझ आवश्यक है।
व्यक्तियों की उम्र के रूप में, कुछ लाभकारी जीवाणु प्रजातियों में गिरावट, जैसे कि बिफीडोबैक्टीरियम, को रोगजनक प्रजातियों, यानी एंटरोबैक्टीरिया [232] के विकास से बदल दिया जाता है। वृद्ध लोगों [233] में फर्मिक्यूट्स में कमी और प्रोटोबैक्टीरिया में वृद्धि की भी सूचना मिली है। इसके अलावा, गट डिस्बिओसिस कई उम्र से संबंधित बीमारियों से जुड़ा हुआ है, जिसमें मोटापा [234], टाइप 2 मधुमेह [235], अल्जाइमर रोग [236], और संक्रमण की घटनाओं में वृद्धि [237-239] शामिल हैं। डिस्बिओसिस से जुड़ी पुरानी सूजन, सेन्सेंट और निष्क्रिय ट्यूमर कोशिकाओं के कमजोर फागोसाइटोसिस, और ट्यूमर-विशिष्ट सीडी 8 प्लस टी कोशिकाओं [240] के खराब सक्रियण के कारण बुजुर्गों में कैंसर के विकास का जोखिम भी अधिक है।
डिस्बिओसिस को विभिन्न उम्र से संबंधित विकृतियों और वृद्ध व्यक्तियों में समय से पहले मौत के लिए एक प्रमुख कारण होने का प्रस्ताव दिया गया था, जिसमें अतिरिक्त सूजन और कई जटिलताओं को ट्रिगर किया गया था, जिसमें लीकी आंत और गैस्ट्रोइंटेस्टाइनल ट्रैक्ट [228] के कम कार्य शामिल थे। इसके अनुरूप, माइक्रोबियल प्रजातियों की एक विशेष संरचना और विविधता बुजुर्गों में स्वास्थ्य, फिटनेस और जीवित रहने में वृद्धि के साथ सहसंबद्ध है [241,242]। हाल के एक अध्ययन से पता चला है कि स्वस्थ बुजुर्ग अपनी माइक्रोबायोटा संरचना में एक विशेष बहाव का अनुभव करते हैं, जबकि कमजोर बुजुर्गों में यह बहाव गायब है [242]। इसके अलावा, उम्र बढ़ने के दौरान उच्च बैक्टेरॉइड्स बहुतायत होने से 4- वर्ष अनुवर्ती में जीवित रहने की दर में कमी आती है। 15 वर्षों के अनुवर्ती के साथ एक और हालिया काम ने बताया कि एंटरोबैक्टीरिया की बहुतायत बुजुर्गों में जठरांत्र और श्वसन संबंधी कारणों से संबंधित मौतों से जुड़ी हुई थी [243]।
डिस्बिओसिस आंतों की बाधा अखंडता में दोष पैदा कर सकता है, जिसके परिणामस्वरूप जीवाणु प्रजातियों को मेजबान ऊतकों में स्थानांतरित कर दिया जाता है। वे बैक्टीरिया न्यूट्रोफिल और विभेदित Th17 कोशिकाओं [244] की भर्ती के माध्यम से सूजन पैदा करते हैं। उदाहरण के लिए, एक ग्राम-पॉजिटिव पैथोबियोनेट्स ई.गैलिनेरम का स्थानान्तरण, जो आंत अवरोध में दोषों के परिणामस्वरूप होता है, Th17 प्रतिक्रिया और स्वप्रतिपिंड उत्पादन [245] को प्रेरित करता है।
अक्करमेन्सिया आंत अवरोध अखंडता [228] की रक्षा करने और एंटीबॉडी और टी सेल प्रतिक्रियाओं [246] को बढ़ाने के लिए दिखाया गया एक लाभकारी सहभोज है। अक्करमेन्सिया का नुकसान वृद्ध गैर-मानव प्राइमेट और चूहों [247] में इंसुलिन प्रतिरोध के साथ जुड़ा हुआ है। घटी हुई ब्यूटायरेट और अक्करमेनिया बहुतायत आंत के रिसाव को बढ़ाती है, जो बदले में प्रो-भड़काऊ प्रतिक्रियाओं को बढ़ाती है।
दूसरी ओर, एक मानव अध्ययन ने बताया कि बुजुर्गों में अक्कर-उन्माद अधिक प्रचुर मात्रा में है [248]। इसके अलावा, Akkermansia को सीरम IgA और CD8 प्लस T कोशिकाओं के साथ महत्वपूर्ण रूप से सहसंबद्ध किया गया था और वृद्ध लोगों में CD4 प्लस T कोशिकाओं के साथ नकारात्मक रूप से सहसंबद्ध किया गया था। बैक्टीरिया, जो बुजुर्गों में कम प्रचुर मात्रा में होते हैं, मध्यम आयु वर्ग में सीरम आईजीजी स्तर और सीडी 4 प्लस टी सेल बहुतायत के साथ सकारात्मक रूप से सहसंबद्ध थे। अंत में, यह अध्ययन अनुकूली प्रतिरक्षा प्रणाली और आंत माइक्रोबायोटा संरचना के बीच संबंधों पर प्रकाश डालता है, हालांकि उनके बीच सीधा संबंध गायब है।
माइक्रोबायोटा बुजुर्गों में रोग के पाठ्यक्रम और टीके की प्रतिक्रियाओं को भी प्रभावित करता है। भले ही मानव इम्युनोडेफिशिएंसी वायरस (एचआईवी) के लिए एंटीवायरल थेरेपी सफल है और रोगियों की जीवन प्रत्याशा को बढ़ाती है, पुराने एचआईवी प्लस लोग एचवी-बुजुर्गों की तुलना में कॉमरेडिडिटी से अधिक पीड़ित होते हैं। एचआईवी प्लस बुजुर्गों में एचआईवी की तुलना में कम सीडी4 प्लस टी-सेल्स और अधिक सीडी-8 प्लस टी-सेल्स हैं जो 55 से अधिक उम्र के हैं [249]। इसके अलावा, कम सीडी4 प्लस टीसेल काउंट वाले व्यक्तियों में पेट में प्रीवोटेला की प्रचुरता काफी अधिक है। प्रीवोटेला पहले हृदय रोगों से जुड़ा था [250], लेकिन यह प्रतिरक्षा प्रणाली के साथ कैसे संपर्क करता है यह अभी तक स्पष्ट नहीं है। आंत माइक्रोबायोटा में आयु-निर्भर परिवर्तन टीकाकरण के बाद खराब प्रतिरक्षा प्रतिक्रिया में योगदान करने की संभावना है [251]। कुछ अध्ययनों ने बताया कि बुजुर्गों में इन्फ्लूएंजा के टीके के बाद प्रोबायोटिक की खुराक एंटीबॉडी टाइटर्स को बढ़ाती है [252-255], जबकि कुछ अध्ययनों ने सीमित या कोई प्रभाव नहीं दिखाया [87,256,257]। परिणामों में भिन्नता कई कारकों के कारण हो सकती है, जिसमें नमूना आकार, प्रोबायोटिक्स का प्रकार और वितरण मार्ग शामिल हैं। फिर भी, अध्ययनों से दृढ़ता से पता चलता है कि माइक्रोबायोटा में असंतुलन बिगड़ा हुआ प्रतिरक्षा प्रतिक्रिया का कारण बनता है, और स्वस्थ संरचना को बहाल करना बुजुर्गों में बेहतर वैक्सीन प्रतिक्रिया के लिए फायदेमंद हो सकता है।
गट माइक्रोबायोटा द्वारा इनेट इम्यून मेमोरी इंडक्शन
अनुकूली प्रतिरक्षा कोशिकाओं के रूप में, जन्मजात प्रतिरक्षा प्रणाली के सदस्य आंत माइक्रोबायोटा के साथ निकटता से बातचीत करते हैं। कुछ अध्ययनों से पता चलता है कि माइक्रोबायोटा माइक्रोबियल एंटीजन और एससीएफए के साथ कोशिकाओं को भड़काने या सहन करके प्रतिरक्षा स्मृति विकास को नियंत्रित कर सकता है। उदाहरण के लिए, -ग्लूकेन, एक कवक कोशिका भित्ति घटक, और बीसीजी क्रमशः डक्टिन-1 और NOD2 सिग्नलिंग मार्ग के माध्यम से कार्य करता है, [91,100]। चूंकि डेक्टिन -1 और नोड-जैसे रिसेप्टर्स (एनएलआर) आंतों में विभिन्न प्रकार की कोशिकाओं पर पाए जाते हैं, जिनमें गैर-प्रतिरक्षा कोशिकाएं भी शामिल हैं, यह प्रस्तावित करना प्रशंसनीय है कि ये कोशिकाएं आंत माइक्रोबायोम के संपर्क में आने के कारण प्रतिरक्षा स्मृति विकसित करती हैं। . इस तर्क का समर्थन करते हुए, आंत माइक्रोबायोटा से प्राप्त पेप्टिडोग्लाइकन टुकड़े न्युट्रोफिल की हत्या क्षमता को बढ़ावा देने, जन्मजात प्रतिरक्षा प्रणाली को प्रमुख बनाने के लिए दिखाए गए थे [258]।
इसके अलावा, आंत माइक्रोबायोटा को चूहों को संक्रमण से बचाने के लिए मायलोपोइजिस को प्रेरित करने के लिए दिखाया गया था [259], -ग्लूकेन प्रशासन द्वारा प्रशिक्षित प्रतिरक्षा प्रेरण के बाद चूहों के अस्थि मज्जा में मायलोइड पूर्वजों की संख्या में वृद्धि के समान। [108]। अन्य माइक्रोबायोटा-व्युत्पन्न घटक, जैसे कि लिपोपॉलीसेकेराइड (LPS), फ्लैगेलिन, और -ग्लुकन, भी हिम्मत में प्रशिक्षित प्रतिरक्षा को प्रेरित करने में सक्षम हो सकते हैं, हालांकि उत्तेजना की खुराक प्रतिरक्षा स्मृति या सहिष्णुता प्रतिक्रिया के लिए महत्वपूर्ण है [260]। जैसा कि पहले उल्लेख किया गया है, प्रशिक्षित प्रतिरक्षा को व्यापक चयापचय और एपिजेनेटिक प्रोग्रामिंग द्वारा मध्यस्थ किया जाता है। कॉमेन्सल गट रोगाणुओं और रोगाणुओं द्वारा निर्मित अणु और मेटाबोलाइट्स स्वयं जन्मजात और अनुकूली प्रतिरक्षा कोशिकाओं [261] दोनों में इस तरह के परिवर्तनों को प्रेरित करने में सक्षम हैं। उदाहरण के लिए, एंटी-माइक्रोबियल गतिविधि में वृद्धि के बावजूद, आंत के रोगाणुओं द्वारा उत्पादित ब्यूटायरेट का मैक्रोफेज में प्रशिक्षित प्रतिरक्षा के विपरीत प्रभाव पड़ता है, संभवतः कम एमटीओआर गतिविधि और एचडीएसी 3 [262] के निषेध से उपजी है।
यह ध्यान रखना महत्वपूर्ण है कि गैर-प्रतिरक्षा कोशिकाएं, जैसे, फाइब्रोब्लास्ट [263], उपकला कोशिकाएं [264], और आंतों की स्ट्रोमल कोशिकाएं (आईएससी) [265] भी प्रतिरक्षा स्मृति बनाने में सक्षम हैं, जो माध्यमिक संक्रमण के बाद बढ़ी हुई प्रतिक्रिया दिखाती हैं। यह दिखाया गया था कि आईएससी एक माध्यमिक संबंधित या असंबंधित संक्रमण के दौरान संक्रमण को अधिक तेजी से साफ कर सकता है, जो प्रतिरक्षा स्मृति की उपस्थिति का संकेत देता है [266]। इसलिए, गैर-प्रतिरक्षा कोशिकाएं आंत के रोगाणुओं और प्रतिरक्षा प्रणाली के बीच होमोस्टैसिस में भी योगदान करती हैं।
आंत माइक्रोबायोटा और जन्मजात प्रतिरक्षा स्मृति को शामिल करने के बीच मजबूत संबंधों को ध्यान में रखते हुए, यह अनुमान लगाया जा सकता है कि बुजुर्गों में डिस्बिओसिस द्वारा प्रशिक्षित प्रतिरक्षा प्रतिक्रिया को विकृत किया जा सकता है। खराब प्रशिक्षित प्रतिरक्षा प्रतिक्रिया बुजुर्गों को संक्रमण के प्रति अधिक संवेदनशील बना सकती है, जबकि एक विपुल प्रतिक्रिया रोग रोगजनन में योगदान कर सकते हैं। हालांकि, यह समझने के लिए और अधिक शोध की आवश्यकता है कि माइक्रोबायोटा में उम्र से संबंधित परिवर्तन जन्मजात प्रतिरक्षा स्मृति को कैसे प्रभावित करते हैं।
प्रतिरक्षा प्रणाली और मस्तिष्क के बीच क्रॉस टॉक
डीएनए क्षति, अपशिष्ट उत्पादों के संचय, ऑक्सीडेटिव तनाव, अशांत ऊर्जा होमियोस्टेसिस और बिगड़ा हुआ कार्य [267] के माध्यम से उम्र बढ़ने से केंद्रीय तंत्रिका तंत्र (सीएनएस) में काफी गिरावट आती है। मस्तिष्क और बाकी सीएनएस प्रतिरक्षात्मक रूप से अलग नहीं हैं, जैसा कि एक बार सोचा गया था: प्रतिरक्षा प्रणाली और सीएनएस के बीच व्यापक क्रॉस-टॉक है। ब्रेन होमियोस्टेसिस और पुनर्जनन एक मजबूत प्रतिरक्षा प्रणाली पर निर्भर करता है [268]। इसलिए, बुढ़ापे के साथ प्रतिरक्षा प्रणाली का बिगड़ना मस्तिष्क की उम्र बढ़ने और न्यूरोडीजेनेरेटिव रोगों में योगदान देता है और बढ़ाता है।
सीएनएस पैरेन्काइमा में, निवासी प्रतिरक्षा कोशिका प्रकार माइक्रोग्लिया है, जो प्रारंभिक विकास [269] में जर्दी थैली में आदिम मैक्रोफेज पूर्वजों से उत्पन्न होता है। स्वस्थ मस्तिष्क के रखरखाव के लिए माइक्रोग्लिया अत्यंत महत्वपूर्ण है। वे प्रतिरक्षा निगरानी करते हैं, संक्रमणों का जवाब देते हैं, परिसंचारी प्रतिरक्षा प्रणाली के साथ संचार को व्यवस्थित करते हैं, न्यूरॉन्स को विनियमित करते हैं, और मस्तिष्क में अन्य प्रकार की कोशिकाएँ, फागोसाइटोज सेलुलर मलबे, मिसफॉल्ड प्रोटीन, विषाक्त उत्पाद और यहां तक कि सिनेप्स [270]। माइक्रोग्लिया उम्र बढ़ने से बदल जाती है और उम्र से संबंधित न्यूरोडीजेनेरेटिव रोगों में योगदान करती है [271]। उनकी फागोसाइटिक क्षमता बढ़ती उम्र के साथ कम हो जाती है, और वे पुरानी निम्न-श्रेणी की सूजन की स्थिति में योगदान करते हैं। प्रतिरक्षा स्मृति पर इस समीक्षा के फोकस के कारण, हम माइक्रो-ग्लिया पर विस्तार से नहीं जाएंगे और इसके बजाय मस्तिष्क की उम्र बढ़ने के संदर्भ में अनुकूली प्रतिरक्षा और प्रशिक्षित प्रतिरक्षा की भूमिका पर ध्यान केंद्रित करेंगे।
रक्त-मस्तिष्क बाधा (बीबीबी) मस्तिष्क में प्रतिरक्षा कोशिकाओं की घुसपैठ को काफी हद तक रोकता है। हालांकि, कुछ प्रतिरक्षा कोशिका प्रकार मस्तिष्कमेरु द्रव (CSF) और रक्त-CSF अवरोध में कोरॉइड प्लेक्सस (CP) [272] में मौजूद होते हैं। मस्तिष्क के निलय में स्थित सीपी, एम्बेडेड केशिकाओं के साथ एक सीएसएफ-उत्पादक उपकला कोशिका नेटवर्क है। टी कोशिकाएं सीपी में मौजूद होती हैं, और वे सीपी एपिथेलियम [273] के आईएफएनवाई-निर्भर सक्रियण द्वारा सीएसएफ में प्रतिरक्षा सेल तस्करी को नियंत्रित करती हैं।
होमोस्टैसिस के दौरान, चोट लगने पर, या न्यूरोडीजेनेरेटिव स्थितियों [272] के दौरान प्रतिरक्षा कोशिकाएं न्यूरोनल अस्तित्व और न्यूरोजेनेसिस में योगदान करती हैं। सीएनएस को नुकसान एक सुरक्षात्मक टी-सेल प्रतिक्रिया को प्रेरित करता है जो न्यूरोनल नुकसान को रोकता है [274]। सीडी4 प्लस लिम्फोसाइट्स इस "न्यूरोप्रोटेक्टिव इम्युनिटी" में सबसे प्रमुख भूमिका निभाते हैं।
न्यूरोप्रोटेक्टिव टी-सेल इम्युनिटी
सी.पी.सी.डी.4 प्लस टी कोशिकाओं को एक प्रभावक-स्मृति फीनो-प्रकार के साथ आश्रय देता है जो सीएनएस-विशिष्ट स्व-प्रतिजनों को पहचानते हैं [275]। ये कोशिकाएं उपकला और सीएनएस के माध्यम से सीएसएफ के माध्यम से परिसंचरण से संकेत प्राप्त कर सकती हैं और मस्तिष्क के होमियोस्टेसिस को बनाए रखने के लिए एक एकीकृत प्रतिक्रिया को व्यवस्थित कर सकती हैं [276]। एस्ट्रो-साइट्स, एक सेल प्रकार जो सिनेप्स और बीबीबी को बनाए रखने में मदद करता है, विभिन्न अन्य कार्यों के बीच, एक न्यूरोप्रोटेक्टिव फेनोटाइप मानता है और टी कोशिकाओं के साथ सह-संवर्धित होने पर न्यूरोनल एपोप्टोसिस को कम करता है [277]। रीढ़ की हड्डी की चोट के दौरान, सीएनएस-विशिष्ट ऑटोरिएक्टिव टी कोशिकाएं चोट वाली जगह पर चली जाती हैं, पुटी के गठन को रोकती हैं, और अक्षतंतु के संरक्षण में योगदान करती हैं [278]।
टी सेल की कमी वाले चूहों में, पूर्वज कोशिकाओं का प्रसार कम हो जाता है, जिससे नए न्यूरॉन्स की संख्या कम हो जाती है, जबकि अतिरिक्त सीएनएस-विशिष्ट ऑटोरिएक्टिव टी कोशिकाओं [268] के साथ ट्रांसजेनिक चूहों में न्यूरोजेनेसिस को बढ़ावा मिलता है। टी-सेल-व्युत्पन्न साइटोकाइन IFNy का पूरक अल्जाइमर रोग के साथ पुराने चूहों में न्यूरोजेनेसिस को बढ़ा सकता है [279]। सीएनएस-विशिष्ट टी कोशिकाएं स्थानिक सीखने और स्मृति के लिए भी महत्वपूर्ण हैं। इम्युनोडेफिशिएंसी चूहों में, स्थानिक स्मृति क्षीण होती है, लेकिन वृद्ध चूहों में भी प्रतिरक्षा कोशिकाओं के पुनर्गठन के साथ इसे बहाल किया जा सकता है [280]। मोटर न्यूरॉन रोग एमियोट्रोफिक लेटरल स्क्लेरोसिस (एएलएस) के मॉडल में, टी सेल की कमी रोग को तेज करती है, जबकि पुनर्गठन न्यूरोप्रोटेक्शन को बढ़ावा देता है और रोग की प्रगति में देरी करता है [281-283]। हालांकि, ध्यान दें, टी कोशिकाएं पार्किंसंस रोग [284] के माउस मॉडल में डोपामिनर्जिक न्यूरॉन्स की मृत्यु में योगदान करती हैं।
एक तंत्र जिसके माध्यम से टी कोशिकाएं मस्तिष्क के रखरखाव में सुधार करती हैं, वह मस्तिष्क-व्युत्पन्न न्यूरोट्रॉफिक कारक (बीडीएनएफ) का विनियमन है। ट्रोपोमायोसिन रिसेप्टर किनसे बी (ट्रकबी) के माध्यम से बीडीएनएफ सिग्नलिंग व्यापक भूमिका निभाता है, उदाहरण के लिए, वयस्क न्यूरोजेनेसिस में [285], स्मृति गठन , और पुनर्प्राप्ति [286,287], और अवसाद रोधी उपचारों [288] द्वारा नियंत्रित किया जाता है। टी-सेल की कमी वाले चूहों [268] में बीडीएनएफ का स्तर कम होता है। बीडीएनएफ माइलिन-व्युत्पन्न पेप्टाइड के साथ चूहों के अवसादग्रस्त व्यवहार और टीकाकरण से जुड़ा है, सीएनएस-विशिष्ट प्रतिरक्षा उत्पन्न करता है, बीडीएनएफ स्तरों को बहाल करता है, न्यूरोजेनेसिस में सुधार करता है, और अवसादग्रस्तता व्यवहार को कम करता है [289]। इसके अलावा, चूहों में स्वस्थ तनाव प्रतिक्रिया मस्तिष्क और बीडीएनएफ स्तरों में टी सेल तस्करी से जुड़ी है। माइलिन-व्युत्पन्न पेप्टाइड [290] के साथ प्रतिरक्षण द्वारा तनाव के कारण होने वाले चिंताजनक व्यवहार को भी कम किया जाता है। न्यूरॉन्स और माइक्रोग्लिया के अलावा, टी कोशिकाओं को स्वयं बीडीएनएफ [291] का स्राव करने के लिए दिखाया गया है।
माइक्रोग्लियल सक्रियण [292] को कम करके एएलएस में ट्रेग को सुरक्षात्मक और विलंबित रोग प्रगति के रूप में भी दिखाया गया है। अल्जाइमर रोग के मॉडल में, Treg प्रत्यारोपण संज्ञानात्मक क्षमताओं को बढ़ाता है और अमाइलॉइड सजीले टुकड़े को कम करता है [293]। इसके अलावा, एक कम Treg / Th17 अनुपात मल्टीपल स्केलेरोसिस के रोगियों में अधिक गंभीर बीमारी के साथ सहसंबद्ध है, एक दुर्बल करने वाली ऑटोइम्यून बीमारी जो न्यूरॉन्स को प्रभावित करती है [294]।
यद्यपि एक अति-उत्साही प्रतिरक्षा प्रतिक्रिया मस्तिष्क के कार्य को ख़राब कर देगी, स्वस्थ मस्तिष्क होमियोस्टेसिस और चोट से उबरने के लिए एक अच्छी तरह से ट्यून की गई टी सेल प्रतिरक्षा स्पष्ट रूप से महत्वपूर्ण है। इस घटना को लक्षित करने वाले किसी भी हस्तक्षेप को भड़काऊ क्षति से बचने के लिए सावधानीपूर्वक नियंत्रित किया जाना चाहिए; हालांकि, मस्तिष्क स्वास्थ्य में अनुकूली प्रतिरक्षा की भूमिका में अंतर्दृष्टि मस्तिष्क की चोट या उम्र से संबंधित न्यूरोडीजेनेरेटिव रोगों का मुकाबला करने के लिए नए रास्ते खोलती है।
माइक्रोग्लिया में प्रशिक्षित प्रतिरक्षा
हाल के अध्ययनों से पता चलता है कि माइक्रोग्लियल कोशिकाओं में जन्मजात प्रतिरक्षा स्मृति को प्रेरित किया जा सकता है। एक अध्ययन में प्रणालीगत एलपीएस प्रशासन [295] पर कम से कम 6 महीने के लिए मौजूद माइक्रोग्लिया में एपिजेनेटिक रिप्रोग्रामिंग पाया गया। दिलचस्प है, जबकि एक एकल एलपीएस इंजेक्शन ने माइक्रोग्लिया में एक प्रशिक्षित फेनोटाइप को प्रेरित किया, बार-बार एलपीएस इंजेक्शन ने सहिष्णुता को शामिल किया। इसी तरह, माइक्रोग्लिया प्रशिक्षण को प्रेरित करने के लिए कम खुराक वाला टीएनएफ प्रशासन भी पाया गया। अल्जाइमर रोग के माउस मॉडल में, प्रशिक्षित प्रतिरक्षा ने रोग को बढ़ा दिया जबकि सहनशीलता ने इसे कम कर दिया। एक हालिया अध्ययन ने एलपीएस-प्रेरित प्रशिक्षण की खोज की पुष्टि की और प्रदर्शित किया कि प्रणालीगत-ग्लूकन प्रशासन माइक्रोग्लिया [296] में प्रशिक्षित प्रतिरक्षा को भी प्रेरित कर सकता है। हालांकि, माइक्रोग्लिया का प्रशिक्षित फेनोटाइप प्राइमिंग के दो दिन बाद ही देखा गया था और अब 7 दिन पर मौजूद नहीं था, संभवतः निरंतर एपिजेनेटिक रिप्रोग्रामिंग की कमी का संकेत देता है। इसलिए, अलग-अलग खुराक और अलग-अलग इंजेक्शन के नियमों के साथ प्रशिक्षण की ताकत और दृढ़ता की जांच करना सार्थक है।
द एजिंग ब्रेन
उम्र बढ़ने के साथ मस्तिष्क के कई कार्य बिगड़ जाते हैं, कुछ तो जीवन के तीसरे दशक के बाद भी कम होने लगते हैं [297]। बिगड़ा हुआ कार्यों में प्रसंस्करण गति, समस्या-समाधान, द्रव तर्क, अवधारणात्मक क्षमता, मौखिक प्रवाह और कार्यशील स्मृति शामिल हैं। हालांकि, जरूरी नहीं कि ये दोष कालानुक्रमिक उम्र से संबंधित हों। यह क्षति के संचय के माध्यम से बढ़ी हुई रखरखाव की मांग और इन मांगों को पूरा करने के लिए मस्तिष्क की निगरानी करने के लिए प्रतिरक्षा प्रणाली की अक्षमता का परिणाम है। बेशक, उम्र बढ़ने से पहले चर्चा की गई तंत्र के माध्यम से प्रतिरक्षा प्रणाली की मांग और अक्षमता दोनों में योगदान होता है।
वृद्ध माइक्रोग्लिया एक प्रो-भड़काऊ फेनोटाइप [298] विकसित करता है। सिर की चोट या संक्रमण के बाद, वे स्वस्थ युवा मस्तिष्क की तुलना में लंबे समय तक प्रो-इंफ्लेमेटरी साइटोकिन्स की अत्यधिक मात्रा का उत्पादन करते हैं [299]। यह भड़काऊ स्थिति बाधित न्यूरोजेनेसिस की ओर ले जाती है [300, 301]। एक प्रो-भड़काऊ वातावरण बीडीएनएफ और गतिविधि-निर्भर साइटोस्केलेटल-जुड़े प्रोटीन जैसे दीर्घकालिक स्मृति के मॉड्यूलर को भी रोकता है और स्मृति अक्षमता का कारण बनता है [299]। मनुष्यों में उम्र के साथ परिसंचारी BDNF का स्तर घटता है, और मस्तिष्क के स्तर में कृंतक मॉडल [302] में गिरावट देखी जाती है, जो टी सेल संख्या और कार्य में उम्र से संबंधित गिरावट को दर्शा सकता है।
एजिंग भी प्रभावकारी मेमोरी सीडी 8 प्लस टी कोशिकाओं की सीपी और मेनिन्जेस-मस्तिष्क को कवर करने वाली झिल्लियों की बढ़ती भर्ती के साथ जुड़ा हुआ है [303]। इन कोशिकाओं को होमोस्टैसिस के दौरान माइक्रोग्लियल फ़ंक्शन को ख़राब करने के लिए दिखाया गया था, लेकिन चोट लगने पर प्रो-इंफ्लेमेटरी साइटोकिन उत्पादन को बढ़ाता है। इसके अलावा, बुजुर्ग व्यक्तियों में Treg की संख्या बढ़ जाती है; हालाँकि, उनकी प्रवासी क्षमता और कार्य संभावित रूप से ख़राब हैं क्योंकि वे न्यूरोडीजेनेरेशन को नियंत्रित करने में सक्षम नहीं हैं। उदाहरण के लिए, मल्टीपल स्केलेरोसिस के रोगियों के Tregs में कम प्रतिरक्षादमनकारी क्षमता होती है और वे मस्तिष्क में स्क्लेरोटिक घावों में जीवित रहने में असमर्थ होते हैं [304]।
पुरानी सूजन के मामले में, जबकि जन्मजात प्रतिरक्षा कोशिकाएं आमतौर पर सहनशीलता प्रदर्शित करती हैं जिससे साइटोकिन उत्पादन कम हो जाता है, माइक्रोग्लिया एक अधिक भड़काऊ फेनोटाइप प्रदर्शित करने के लिए एक प्राइम प्राप्त करता है, संज्ञानात्मक गिरावट को तेज करता है [305]। इसके अलावा, वृद्ध जीवों में परिसंचारी टीएनएफए के उच्च स्तर को देखा जाता है। जैसा कि ऊपर चर्चा की गई है, माइक्रोग्लिया में प्रशिक्षित प्रतिरक्षा को प्रेरित करके भी नुकसान पहुंचा सकता है। इसलिए, मस्तिष्क के स्वस्थ रखरखाव के लिए एक अच्छी तरह से संतुलित जन्मजात प्रतिरक्षा उतनी ही आवश्यक है जितनी कि अनुकूली प्रतिरक्षा।
सभी कोणों से प्रतिरक्षा उम्र बढ़ने से निपटना
उम्र बढ़ने को धीमा करने या वापस लाने के प्रयास दुर्लभ से बहुत दूर हैं। हालांकि, अधिकांश अध्ययनों द्वारा मूल्यांकन किए गए परिणाम उपायों को इस अर्थ में प्रतिबंधित किया गया है कि वे यंत्रवत अंतर्दृष्टि प्रदान नहीं करते हैं या विशिष्ट प्रक्रियाओं पर ध्यान केंद्रित नहीं करते हैं। फिर भी, कुछ रोमांचक हस्तक्षेप, जिनमें कैलोरी प्रतिबंध, मेटफॉर्मिन और शारीरिक व्यायाम शामिल हैं, प्रतिरक्षा, चयापचय, एपिजेनेटिक्स, माइक्रोबायोटा और तंत्रिका तंत्र (छवि 2) सहित कई स्तरों पर उम्र बढ़ने में हस्तक्षेप करते हैं। निम्नलिखित अध्याय चर्चा करते हैं
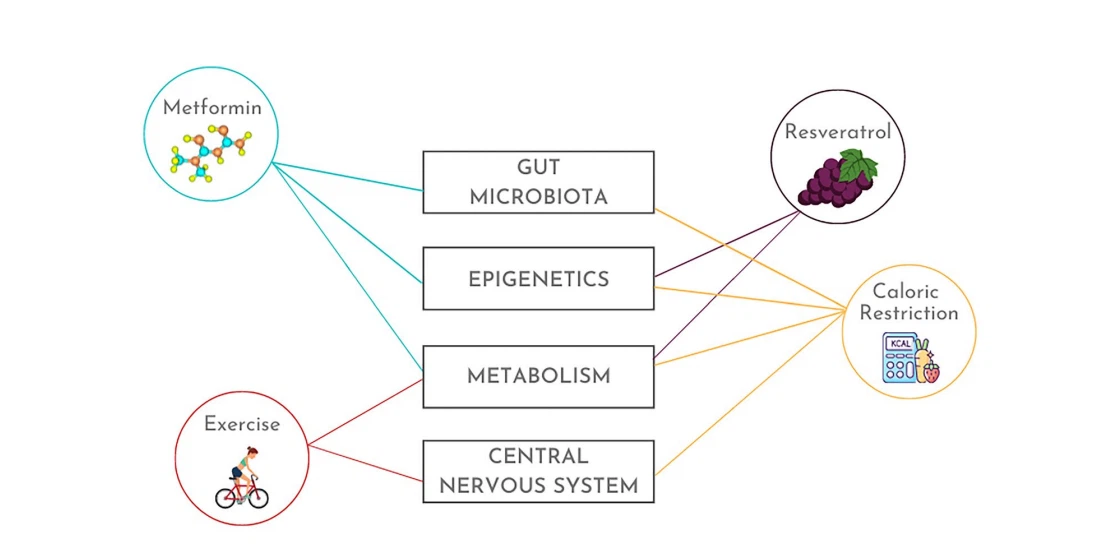
Fig.2 उम्र बढ़ने की प्रक्रिया के कई पहलुओं को लक्षित करने वाले एंटी-एजिंग हस्तक्षेप का वादा करना। मेटफोर्मिन स्टेम सेल की उम्र बढ़ने में देरी करता है, माइटोकॉन्ड्रियल फ़ंक्शन में सुधार करता है, टेलोमेयर को छोटा होने से रोकता है, उम्र से संबंधित एपिजेनेटिक संशोधनों को उलट देता है, और आंत के रिसाव और डिस्बिओसिस को कम करता है। शारीरिक व्यायाम, भले ही जीवन में देर से शुरू किया गया हो, प्रतिरक्षा कोशिका संख्या और कार्यों में सुधार करता है, माइटोकॉन्ड्रियल चयापचय को पुनर्स्थापित करता है, सेलुलर बुढ़ापा रोकता है, संज्ञानात्मक गिरावट का प्रतिकार करता है, और न्यूरोडीजेनेरेटिव रोगों के जोखिम को कम करता है। अंगूर और रेड वाइन में उपलब्ध रेस्वेराट्रोल, एक एंटीऑक्सिडेंट के रूप में कार्य करता है, विभिन्न मॉडल जीवों में जीवनकाल बढ़ाता है, प्रणालीगत सूजन को कम करता है, और एपिजेनेटिक उम्र बढ़ने को धीमा करता है। 20-40 प्रतिशत तक कैलोरी प्रतिबंध जीवनकाल को बढ़ाता है और गैर-मानव प्राइमेट में सर्व-कारण मृत्यु दर को कम करता है, एपिजेनेटिक उम्र बढ़ने में देरी करता है, आंत माइक्रोबायोटा को पुनर्स्थापित करता है, और संज्ञानात्मक गिरावट को धीमा करता है। इन उपचारों द्वारा साझा किए गए सेलुलर तंत्र में उम्र बढ़ने की समस्या से निपटने और सबसे आशाजनक एंटी-एजिंग उपचार के तंत्र का विस्तार करने के लिए एमटीओआर / एकेटी अक्ष की सीमा और एएमपीके और एसआईआरटी 1 की सक्रियता शामिल है।
चयापचय हस्तक्षेप
अधिकांश मानव विकास के लिए, पोषक तत्व दुर्लभ थे, और उन्हें प्राप्त करने के लिए बहुत अधिक शारीरिक गतिविधि की आवश्यकता थी। इस प्रकार, मनुष्य उन परिस्थितियों के अनुकूल होने के लिए विकसित हुआ। पोषक तत्वों की अधिकता के साथ हमारी वर्तमान गतिहीन जीवन शैली, मोटापा, मधुमेह और हृदय रोग [306] जैसे चयापचय रोगों के उच्च प्रसार का कारण बनने का प्रस्ताव है। इसके अलावा, इन स्थितियों के लिए उम्र एक जोखिम कारक है, जैसा कि पहले उल्लेख किया गया है, और प्रतिरक्षात्मकता में चयापचय रोग प्रोफाइल के साथ बहुत कुछ है। इसलिए, चयापचय संबंधी हस्तक्षेपों पर ध्यान केंद्रित करना उम्र बढ़ने और चयापचय संबंधी विकारों से एक साथ निपटने के लिए एक समझदार दृष्टिकोण है। कैलोरी प्रतिबंध (सीआर) और व्यायाम, हमें पैतृक स्थितियों के करीब लाते हैं, अनुसंधान की इस पंक्ति में अग्रणी हैं।
सीआर कुल कैलोरी सेवन में 20-40 प्रतिशत की कमी को दर्शाता है। यीस्ट से गैर-प्राइमेट्स तक, सीआर को बार-बार जीवन काल को बढ़ाने के लिए दिखाया गया है [307]। रीसस बंदरों में, युवा वयस्कता से शुरू होने वाले सीआर ने उम्र से संबंधित कारणों से मृत्यु दर के जोखिम को तीन गुना और सर्व-मृत्यु दर को 1 से कम कर दिया। { {6}}गुना [308]। एक अन्य अध्ययन में, सीआर ने मधुमेह, कैंसर और हृदय रोग की घटनाओं को कम किया, जबकि रोग की शुरुआत में भी देरी [309]। एक विपरीत अध्ययन ने बताया कि जीवित रहने में कोई सुधार नहीं हुआ, हालांकि कैंसर और मधुमेह की घटनाओं में कमी आई थी [310]।
218 गैर-मोटे लोगों के यादृच्छिक नियंत्रित परीक्षण में, एक 2-वर्ष के सीआर आहार ने परिसंचारी टीएनएफ स्तरों को कम कर दिया और बिना किसी हस्तक्षेप-संबंधी प्रतिकूल प्रभाव [311] के बिना कोलेस्ट्रॉल और ट्राइग्लिसराइड्स जैसे कार्डियोमेटाबोलिक जोखिम मार्करों को आश्चर्यजनक रूप से कम कर दिया। अब तक, दीर्घायु पर सीआर के महत्वपूर्ण प्रभाव की रिपोर्ट करने वाला कोई मानव अध्ययन नहीं है। मनुष्यों में सीआर के वादे को मजबूत करने के लिए आनुवंशिक रूप से विविध आबादी वाले बड़े और व्यापक अध्ययन की आवश्यकता है।
सीआर के विभिन्न चयापचय प्रभावों में एमटीओआर का डाउनरेगुलेशन और इंसुलिन सिग्नलिंग और एसआईआरटी 1 का सक्रियण शामिल है, जो सभी प्रतिरक्षा सेल फ़ंक्शन [312] पर व्यापक प्रभाव डालते हैं। सीआर को रीसस बंदरों [313] में टी सेल सेनेसेंस में देरी करने के लिए दिखाया गया है। इसके अलावा, CD4t और CD8 प्लस भोले Tcell पूल का विस्तार किया गया था, और थाइमिक आउटपुट और T सेल प्रसार को बढ़ाया गया था, लेकिन CR के बाद CD8 प्लस कोशिकाओं द्वारा IFNy उत्पादन कम कर दिया गया था। यद्यपि ली गई कैलोरी की संख्या को कम करने से आयु-प्रेरित चयापचय परिवर्तनों को उलटने और स्वास्थ्य और दीर्घायु में सुधार होता है, यह ध्यान रखना महत्वपूर्ण है कि कृन्तकों में कुछ अध्ययनों ने एक खराब अनुकूली प्रतिक्रिया की सूचना दी और बुजुर्ग जानवरों में इन्फ्लूएंजा ए और वेस्ट नाइल वायरस के खिलाफ मृत्यु दर में वृद्धि हुई। सीआर [314,315] के बाद। हालांकि, हाल ही में एक माउस अध्ययन ने एम.ट्यूबरकुलोसिस संक्रमण के खिलाफ सीआर के सुरक्षात्मक प्रभावों का खुलासा किया। यह प्रभाव एमटीओआर निषेध द्वारा विशेषता चयापचय बदलाव से संबंधित था, लेकिन ग्लाइकोलाइसिस को बढ़ाया और एफएओ को कम किया, साथ में
बढ़ी हुई स्वरभंग [316]। एमटीओआर अवरोधक रैपामाइसिन ने सीआर के साथ सहक्रियात्मक रूप से काम किया और आगे चलकर ऑटोफैगी को बढ़ाया, जिससे एम। तपेदिक का अधिक कुशल निषेध हुआ।
सीआर के समान, व्यायाम प्रतिरक्षा के साथ हस्तक्षेप करने का वादा कर रहा है। नियमित रूप से व्यायाम करने वाली वृद्ध महिलाओं में उम्र-मिलान गतिहीन महिलाओं की तुलना में बेहतर एनके और टी सेल कार्य थे [317]। निष्क्रिय टी सेल संख्या और थाइमिक आउटपुट शारीरिक रूप से सक्रिय बुजुर्गों में, युवा वयस्कों के समान, गतिहीन लोगों की तुलना में अधिक थे [318]। उनके पास कम परिसंचारी आईएल -6 और उच्च आईएल -7 भी था, जो टी सेल के विकास के लिए आवश्यक है। हालाँकि, सेन्सेंट सीडी 8 प्लस टी सेल नंबर समूहों के बीच भिन्न नहीं थे। एक 8-सप्ताह के प्रशिक्षण कार्यक्रम के बाद, बुजुर्ग वयस्कों की प्रतिरक्षा कोशिकाओं ने बढ़ी हुई स्वरभंग और डाउनग्रेडेड एनएलआरपी3 इन्फ्लामेसोम [319] प्रदर्शित किया। व्यायाम ने कंकाल की मांसपेशी कोशिकाओं और प्रतिरक्षा कोशिकाओं में समान रूप से माइटोफैगी और माइटोकॉन्ड्रियल बायोजेनेसिस में सुधार किया, उम्र बढ़ने से बिगड़ा सेलुलर चयापचय स्थिति को बहाल किया। [320]।
जीवनशैली में हस्तक्षेप के अलावा, रासायनिक चयापचय नियामकों की भी उनकी उम्र बढ़ने की क्षमता के लिए जांच की जाती है। मेटफोर्मिन, अपने ग्लूकोज-कम करने वाले प्रभाव के लिए 60 से अधिक वर्षों से मनुष्यों में सुरक्षित रूप से उपयोग किया जाता है, कई तंत्रों के माध्यम से उम्र से जुड़े हॉलमार्क को कम करता है। इनमें AMPK का सक्रियण, mTORCl का निषेध, बेहतर माइटोकॉन्ड्रियल बायोजेनेसिस, इंसुलिन / IGF1 सिग्नलिंग का डाउनरेगुलेशन और SIRT1 [321] का सक्रियण शामिल है। इसके अलावा, मेट-फॉर्मिन स्टेम सेल की उम्र बढ़ने में देरी करता है और टेलोमेयर को छोटा करता है। कुल मिलाकर, यह उम्र बढ़ने के सभी लक्षणों पर कार्य करता प्रतीत होता है। वर्तमान में मेटफॉर्मिन (https://www.afar.org/tame-trial) की उम्र बढ़ने की क्षमता का आकलन करने के लिए 65-79 आयु वर्ग के 3000 से अधिक व्यक्तियों के एक बड़े नैदानिक परीक्षण की योजना बनाई जा रही है।
एवरोलिमस, एक अन्य एमटीओआर अवरोधक, बुजुर्गों में इन्फ्लूएंजा टीकाकरण के लिए प्रतिरक्षात्मकता और बेहतर एंटीबॉडी प्रतिक्रियाओं को कमजोर करता है [322]। भले ही इस अध्ययन में अधिकांश प्रतिरक्षा सेल सबसेट में बदलाव नहीं किया गया था, लेकिन प्रोग्राम्ड सेल डेथ प्रोटीन 1 (पीडी -1), थकावट के एक मार्कर के लिए सकारात्मक टी कोशिकाओं को स्पष्ट रूप से कम कर दिया गया था। 264 बुजुर्ग विषयों के साथ एक अनुवर्ती अध्ययन ने एंटीवायरल अभिव्यक्ति को अपग्रेड किया, इन्फ्लूएंजा टीकाकरण के लिए बेहतर प्रतिक्रिया, और कुल मिलाकर कम संक्रमण [323] की सूचना दी। SIRT1 सक्रियण प्रतिरक्षण क्षमता से निपटने का एक और तरीका है। यह बी सेल प्रसार और कार्य में सुधार करने के लिए जाना जाता है, और इसलिए उम्र के साथ घटती एंटीबॉडी प्रतिक्रियाओं में सुधार करने में मदद कर सकता है [324]। SIRT1 प्रोटीन और हिस्टोन डीसेटाइलेशन [325] के माध्यम से चयापचय पथ को संशोधित कर सकता है। SIRTl के लक्ष्यों में NF-KB, हाइपोक्सिया-इंड्यूसीबल कारक 1-अल्फ़ा (HIFla), और FOXO प्रतिलेखन कारक शामिल हैं। इसके अलावा, SIRT1 सक्रियण बीसीजी-प्रेरित प्रशिक्षित प्रतिरक्षा प्रतिक्रिया [326] को प्रबल करता है। SIRT 1- के साथ माउस अध्ययन के बावजूद, विलंबित आयु-संबंधित फेनोटाइप और बढ़े हुए जीवनकाल [327, 328] दिखाने वाले सक्रियकर्ता, इस बात का कोई सबूत नहीं है कि SIRTl मनुष्यों में दीर्घायु के साथ जुड़ा हुआ है [329]।
रेड वाइन में पाया जाने वाला एक पॉलीफेनोल यौगिक रेस्वेराट्रोल, SIRT1 [330] का एक प्रबल उत्प्रेरक है। यह एएमपीके को सक्रिय करने के लिए भी दिखाया गया है, इसलिए एमटीओआर सिग्नलिंग को दबा रहा है [331]। इन विट्रो अध्ययन और रेस्वेराट्रॉल की एंटीऑक्सीडेंट और विरोधी भड़काऊ गतिविधि प्रदर्शित करने वाले सूजन रोग मॉडल के अलावा [332], कई चूहों के अध्ययन से इसकी एंटीवायरल क्षमता [333,334] का पता चलता है। दीर्घायु के संदर्भ में, अध्ययन में रेस्वेराट्रॉल द्वारा एक महत्वपूर्ण जीवनकाल विस्तार की रिपोर्ट करने में विफल रहे। स्वस्थ चूहे [327,335]। हालांकि, उच्च-कैलोरी आहार से खिलाए गए चूहों में, रेस्वेराट्रोल ने ट्रांसक्रिप्शनल प्रोफाइल को मानक-खिलाए गए चूहों [336] की ओर स्थानांतरित कर दिया। इसने इंसुलिन संवेदनशीलता में भी सुधार किया और उत्तरजीविता में वृद्धि की। इसी तरह के परिणाम रीसस बंदरों में उच्च वसा, उच्च शर्करा वाले आहार [337] पर देखे गए। एएमपीके-एसआईआरटी1 अक्ष और कम प्रणालीगत सूजन, ग्लूकोज और ट्राइग्लिसराइड के स्तर के माध्यम से रेस्वेराट्रोल प्रेरित चयापचय परिवर्तनों के साथ मोटापे से ग्रस्त पुरुषों के तीस दिन के पूरक। हालांकि, इसी तरह के एक अध्ययन ने रेस्वेराट्रोल [339] के किसी भी लाभकारी प्रभाव की सूचना नहीं दी।
कुल मिलाकर, प्रतिरक्षात्मकता और उम्र से जुड़े चयापचय रोगों के अंतर्निहित चयापचय मार्गों को लक्षित करने वाले अत्यधिक आशाजनक चिकित्सीय दृष्टिकोण हैं। हालांकि, मनुष्यों में बड़े पैमाने पर यादृच्छिक नियंत्रण परीक्षणों को यह देखने की आवश्यकता है कि क्या गैर-मानव प्राइमेट और छोटे मॉडल जीवों में ये रोमांचक अवलोकन मानव उपयोग के लिए अनुवाद योग्य हैं।
एपिजेनेटिक्स को संशोधित करने वाली रणनीतियाँ
कई उम्र से संबंधित बीमारियों, जैसे, कैंसर, मधुमेह और अल्जाइमर रोग के लिए एपिजेनेटिक हस्तक्षेपों को नियोजित किया गया है; हालांकि, केवल कुछ अध्ययन विशेष रूप से एपिजेनेटिक संरचना में आयु-निर्भर परिवर्तनों को लक्षित करते हैं [340]। इसके बजाय, इम्युनोजेन को रोकने के लिए नियोजित चयापचय हस्तक्षेप भी उम्र से जुड़े एपिजेनेटिक परिदृश्य को बदलकर काम करते हैं। रेस्वेराट्रोल, सीआर, और मेटफोर्मिन बुजुर्गों में उम्र से संबंधित डीएनए मेथिलिकरण और हिस्टोन संशोधनों को पुन: कॉन्फ़िगर करने के लिए तीन आशाजनक चिकित्सीय विकल्प हैं।
एक दिलचस्प अध्ययन से पता चला है कि थाइमस को पुन: उत्पन्न करने के परिणामस्वरूप 2.5-वर्ष की छोटी एपिजेनेटिक आयु [341] हुई। 51 से 65 वर्ष की आयु के प्रतिभागियों को पुनः संयोजक मानव विकास हार्मोन, डीहाइड्रोएपियनड्रोस्टेरोन (डीएचईए) के साथ एक 1-वर्ष का उपचार प्राप्त हुआ, जो एक स्टेरॉयड हार्मोन अग्रदूत और मेटफॉर्मिन है। उपचार ने कार्यात्मक थाइमिक द्रव्यमान को बहाल किया, प्रतिरक्षा सेल उप-सेटों में परिवर्तन, और साइटोकिन उत्पादन, साथ ही साथ परिवर्तित एपिजेनेटिक प्रोफाइल, जो कम उम्र से जुड़ा था।
रीसस बंदर, जो 40 प्रतिशत कैलोरी प्रतिबंध के संपर्क में थे, पुराने बंदरों में पाए जाने वाले मिथाइलेशन परिवर्तनों को प्रदर्शित करने में देर हो गई [342]। यद्यपि यह अध्ययन विलंबित मेथिलिकरण बहाव से जुड़े लंबे जीवनकाल का प्रत्यक्ष प्रमाण प्रदान नहीं करता है, लेकिन यह बताता है कि उम्र बढ़ने की प्रक्रिया को धीमा करने के लिए सीआर का उपयोग किया जा सकता है। इसके अनुरूप, रेस्वेराट्रोल या सीआर के साथ चूहों के जीवनकाल में सुधार के परिणामस्वरूप धीमी एपिजेनेटिक उम्र बढ़ने [343] हुई। आजीवन सीआर को मस्तिष्क में उम्र से संबंधित डीएनए मेथिलिकरण परिवर्तनों को रोकने के लिए भी दिखाया गया है, जो न्यूरोप्रोटेक्शन प्रदान करता है [344]।
कुछ अध्ययन बताते हैं कि सीआर एपिजेनेटिक्स को कैसे प्रभावित कर सकता है। इन तंत्रों में बढ़े हुए SIRTI अभिव्यक्ति, उच्च डीएनए मिथाइलट्रांसफेरेज़ (DNMT) गतिविधि और रास [340] जैसे विशिष्ट नियामक जीनों के हाइपरमेथिलेशन द्वारा मध्यस्थता में कमी हुई हिस्टोन एसिटिलेशन शामिल हैं। इसी तरह, मेटफॉर्मिन एसआईआरटी1 को सक्रिय करके और एचडीएसी को रोककर एपिजेनेटिक निशानों पर कार्य करता है।[345] हमारे ज्ञान के लिए, उम्र बढ़ने से संबंधित एपिजेनेटिक परिवर्तनों पर सीआर के प्रभावों की जांच करने वाला कोई शोध नहीं है, संभवतः मनुष्यों पर इस तरह के दीर्घकालिक हस्तक्षेपों को लागू करने की सीमाओं के कारण।
माइक्रोबायोटा को लक्षित करने वाले संभावित उपचार
चूंकि आंत माइक्रोबायोटा मेजबान चयापचय को नियंत्रित करता है, चयापचय को लक्षित करने वाले एंटी-एजिंग हस्तक्षेप अनिवार्य रूप से आंत माइक्रोबायोटा को प्रभावित करते हैं। एक उदाहरण के रूप में, चयापचय मार्गों पर कार्य करने के अलावा, मेटफॉर्मिन आंत माइक्रोबायोटा को नियंत्रित करता है। मोटे और वृद्ध चूहों में मेटफोर्मिन के प्रभावों की जांच करने वाले एक अध्ययन में एपिडीडिमल वसा में IL-1 और IL-6 में कमी पाई गई, जो आंत के रोगाणुओं में परिवर्तन से जुड़ा था [346]। इसके अलावा, टाइप 2 मधुमेह के रोगी जो मेटफोर्मिन लेते हैं, उनकी हिम्मत [347] में एक्करमेन्सिया की अधिकता थी, जो कि कम बैक्टीरियल ट्रांसलोकेशन और डिस्बिओसिस [348] के जोखिम से संबंधित थी। इनके अनुरूप, मेटफॉर्मिन ने उम्र से संबंधित लीकी आंत को कम किया और चूहों में सूजन [349]।
माइक्रोबायोटा को लक्षित करके इम्युनोजेन को रोकने के लिए एक अन्य उपचार रणनीति प्रो-और प्रीबायोटिक्स का उपयोग है। प्रोबायोटिक्स जीवित सूक्ष्मजीवों से युक्त पूरक हैं, जबकि प्रीबायोटिक्स ऐसे सब्सट्रेट हैं जिनका उपयोग सूक्ष्मजीव जीवित रहने के लिए कर सकते हैं [350]। हालांकि परस्पर विरोधी साक्ष्य हैं, अध्ययनों से पता चलता है कि नियमित प्रोबायोटिक का उपयोग आंतों के रोगाणुओं की विविधता और बहुतायत को नियंत्रित कर सकता है, जिससे डिस्बिओसिस [351,352] की घटनाओं में कमी आती है। प्रोबायोटिक्स बढ़े हुए बी और टी सेल की संख्या, बढ़ी हुई एनके सेल गतिविधि [353], और वृद्ध व्यक्तियों [354] में इन्फ्लूएंजा वायरस के खिलाफ उच्च आईजीए उत्पादन से स्पष्ट प्रतिरक्षा प्रतिक्रियाओं से जुड़े हैं। इसके अलावा, प्रोबायोटिक्स के साथ पूरक ने बुजुर्गों के बीच अवसरवादी बैक्टीरिया क्लोस्ट्रीडियम डिफ-फाइल के विकास को कम करने में मदद की [355]। इन निष्कर्षों के विपरीत, 10 यादृच्छिक नियंत्रित अध्ययनों के मेटा-विश्लेषण ने भड़काऊ साइटोकिन उत्पादन को कम करने पर प्रोबायोटिक्स का कोई लाभकारी प्रभाव नहीं दिखाया [356]।
प्रीबायोटिक्स, यानी सिनबायोटिक्स के साथ प्रोबायोटिक्स के संयोजन का भी लाभकारी प्रभाव पड़ता है, जैसे प्रोबायोटिक्स सप्लीमेंट। एक सिनबायोटिक फॉर्मूले के साथ बुजुर्ग व्यक्तियों में दो महीने के उपचार ने परिसंचरण में चयापचय सिंड्रोम मापदंडों में काफी सुधार किया और टीएनएफ और सी-रिएक्टिव प्रोटीन [357] जैसे भड़काऊ प्रोटीन में कमी आई। एक डबल-ब्लाइंड 4-सप्ताह के सहजीवी उपचार अध्ययन ने प्लेसीबो की तुलना में उपचार समूह में बिफीडोबैक्टीरिया, एक्टिनोबैक्टीरिया, फर्मिक्यूट्स और मेटाबोलाइट ब्यूटायरेट में वृद्धि की सूचना दी, जबकि प्रोटोबैक्टीरिया और प्रो-इंफ्लेमेटरी साइटोकिन्स कम थे [358]।
बुजुर्गों में संज्ञानात्मक कार्यों, चयापचय मापदंडों और आंत माइक्रोबायोटा में सुधार के लिए कैलोरी प्रतिबंध एक अन्य उपचार रणनीति हो सकती है। सीआर ने अल्जाइमर रोग के माउस मॉडल में संज्ञानात्मक गिरावट को धीमा कर दिया, जो हिम्मत में बढ़े हुए बैक्टेरॉइड्स से जुड़ा था। 2 महीने के लिए 30 प्रतिशत कम कैलोरी प्राप्त करने वाले वृद्ध चूहों ने अपने माइक्रोबायोटा में युवा चूहों के समान अधिक संतुलित संरचना की ओर महत्वपूर्ण बदलाव प्रदर्शित किए [359]। आजीवन सीआर ने माइक्रोबायोटा में अधिक व्यापक परिवर्तनों को प्रेरित किया, भड़काऊ पेप्टाइड्स की एकाग्रता को कम किया, और चूहों के जीवनकाल में वृद्धि की [360]। हालांकि, हाल के एक अध्ययन से पता चला है कि गंभीर सीआर, 50 प्रतिशत से अधिक, माइक्रोबायोटा की विविधता को बाधित करता है और रोगजनक बैक्टीरिया सी। डिफिसाइल [361] के विकास की ओर जाता है। इस प्रकार, सीआर की सीमा और अवधि को सावधानीपूर्वक निर्धारित करना महत्वपूर्ण है।
ब्रेन एजिंग के लिए हस्तक्षेप
शारीरिक व्यायाम मस्तिष्क स्वास्थ्य को बढ़ावा देने का एक उत्कृष्ट तरीका है। व्यायाम संज्ञानात्मक हानि का प्रतिकार करता है, मनोभ्रंश के जोखिम को कम करता है, स्थानिक स्मृति में सुधार करता है, और न्यूरोप्लास्टी को बढ़ाता है [362]। शारीरिक गतिविधि स्मृति हानि [363] के लिए जोखिम एलील्स के प्रभावों को कम कर सकती है और अल्जाइमर रोग [364,365] के विकास से बचा सकती है। कुल 163,797 प्रतिभागियों के साथ 16 अध्ययनों की एक व्यवस्थित समीक्षा ने बताया कि नियमित व्यायाम से मनोभ्रंश और अल्जाइमर में क्रमशः 28 प्रतिशत और 45 प्रतिशत जोखिम में कमी आई है [366]। ध्यान दें, व्यायाम की आवृत्ति और तीव्रता के बावजूद अधिकांश व्यक्तिगत अध्ययनों में व्यायाम से जुड़े जोखिम में कमी देखी गई थी।
अध्ययन न्यूरोप्रोटेक्शन [367,368] के पीछे संभावित तंत्र के रूप में व्यायाम के एंटीऑक्सिडेंट और विरोधी भड़काऊ प्रभावों का सुझाव देते हैं। व्यायाम के विरोधी भड़काऊ परिणामों में शामिल हैं कम परिसंचारी आईएल -6 लेकिन बढ़े हुए आईएल -10 और आईएल -1 आरए, कम संख्या में Treg, परिसंचरण में भड़काऊ मोनोसाइट्स की उच्च संख्या, और बाधित मोनोसाइट फ़ंक्शन [ 369]. इनके अलावा, शारीरिक व्यायाम कम सेन्सेंट टी कोशिकाओं, एनके सेल साइटोटोक्सिसिटी और न्यूट्रोफिल फागोसाइटोसिस में वृद्धि, और ल्यूकोसाइट्स [370] में लंबे समय तक टेलोमेरेस से जुड़ा हुआ है। इसके अतिरिक्त, मध्यम हृदय व्यायाम ने बुजुर्गों में इन्फ्लूएंजा टीकाकरण के बाद सेरोप्रोटेक्शन में सुधार किया [371]। इम्यूनोसेनेसेंस को धीमा करने से बेहतर प्रतिरक्षा निगरानी और सीएनएस की मरम्मत के माध्यम से मस्तिष्क की उम्र बढ़ने और संज्ञानात्मक गिरावट सीमित हो जाएगी।
इसके अलावा, यहां तक कि एक एकल व्यायाम सत्र भी BDNF के स्तर को बढ़ाता है जिसे नियमित व्यायाम [372] के साथ और बढ़ाया जाता है। दिलचस्प बात यह है कि बीडीएनएफ में व्यायाम से संबंधित वृद्धि महिलाओं की तुलना में पुरुषों में अधिक स्पष्ट है। केटोन निकायों को BDNF अभिव्यक्ति [373,374] को प्रेरित करने के लिए भी दिखाया गया है, संभवतः तंत्रिका संबंधी रोगों [375] में किटोजेनिक आहार के न्यूरोप्रोटेक्टिव प्रभाव में योगदान करते हैं।
सीआर न्यूरोनल क्षति को रोकने के लिए दिखाया गया एक और हस्तक्षेप है। यह बीडीएनएफ की अभिव्यक्ति में वृद्धि करता है और न्यूरोजेनेसिस को बढ़ाता है [376], ग्लाइकोलाइसिस से कीटोन निकायों के उपयोग के लिए एक ऊर्जावान बदलाव का कारण बनता है, सफेद पदार्थ की अखंडता की रक्षा करता है, और चूहों में दीर्घकालिक स्मृति में सुधार करता है [377]। चूहों में, एक वैकल्पिक दिन सीआर रेजिमेन रासायनिक रूप से प्रेरित क्षति [378] के लिए न्यूरोनल प्रतिरोध को बढ़ावा देता है। मस्तिष्क में ऑक्सीडेटिव तनाव के दमन के कारण सीआर-प्रेरित न्यूरोप्रोटेक्शन का एक तंत्र होने की संभावना है [379,380]। हालांकि, कैलोरी सेवन में 50 प्रतिशत की कमी के साथ गंभीर सीआर चूहों में अवसादग्रस्तता व्यवहार का कारण बताया गया था [381]। अल्जाइमर रोग के माउस मॉडल में, सीआर एमिलॉयड प्लेक जमाव को सीमित करने में सक्षम है [382,383], संभवतः एसआईआरटी 1 सक्रियण से जुड़े तंत्र के माध्यम से [384]।
कृन्तकों में सभी सकारात्मक परिणामों के बावजूद, गैर-मानव प्राइमेट में सीआर के न्यूरोप्रोटेक्टिव प्रभाव बहुत स्पष्ट नहीं हैं, जबकि बड़े मानव अध्ययनों की कमी है [385]। फिर भी, मनुष्यों के साथ एक छोटे से यादृच्छिक नियंत्रित परीक्षण के परिणामस्वरूप संज्ञानात्मक कार्य में कोई महत्वपूर्ण सुधार नहीं हुआ [386]। वृद्ध वयस्कों पर एक अन्य नैदानिक अध्ययन ने सीआर [387] के 3 महीनों के बाद बेहतर स्मृति स्कोर दिखाया। हिप्पोकैम्पस में उच्च कार्यात्मक कनेक्टिविटी के साथ बेहतर स्मृति, मोटापे से ग्रस्त महिलाओं में रिपोर्ट की गई थी, जो एक 3- महीने के सीआर आहार [388] से गुजरती थीं। न्यूरोप्रोटेक्टिव प्रभावों की सीमा को समझने के लिए सीआर के साथ अधिक व्यापक मानव अध्ययन आवश्यक हैं।
दिलचस्प बात यह है कि बीसीजी टीकाकरण हाल ही में गैर-इलाज वाले रोगियों [389, 390] की तुलना में बीसीजी इम्यूनोथेरेपी के साथ इलाज किए गए मूत्राशय के कैंसर रोगियों में अल्जाइमर और पार्किंसंस रोगों के जोखिम को कम करने के लिए दिखाया गया था। मूत्राशय के कैंसर के उपचार में, बीसीजी प्रशासन के सामान्य इंट्राडर्मल मार्ग के बजाय सीधे मूत्राशय में लगाया जाता है। रोमांचक भविष्य की शोध परियोजनाएं न्यूरोडीजेनेरेटिव रोगों पर इंट्राडर्मल बीसीजी के प्रभावों का आकलन करेंगी और यह पता लगाने के लिए अंतर्निहित तंत्र की जांच करेंगी कि क्या प्रशिक्षित प्रतिरक्षा न्यूरोप्रोटेक्टिव प्रभावों में भूमिका निभाती है। वर्तमान में, देर से शुरू होने वाले अल्जाइमर रोगियों (एनसीटी04449926) में इंट्रा-डर्मल बीसीजी इंजेक्शन का उपयोग करके नैदानिक परीक्षण चल रहा है।
समापन टिप्पणी
जैविक उम्र बढ़ना एक जटिल प्रक्रिया है जिसमें जीव की सभी प्रणालियाँ शामिल होती हैं। इसके केंद्र में प्रतिरक्षा प्रणाली है, जो अन्य सभी के साथ बातचीत करती है। उम्र बढ़ने की प्रतिरक्षा प्रणाली बुजुर्गों में संक्रमण और उम्र से संबंधित चयापचय और न्यूरोडीजेनेरेटिव रोगों के लिए उच्च संवेदनशीलता के लिए एक अपराधी है, दूसरों के बीच में। इसलिए, संक्रमण से संबंधित रुग्णता और मृत्यु दर को कम करने और वृद्ध व्यक्तियों में टीके की प्रतिक्रिया को बढ़ाने के लिए जन्मजात और अनुकूली प्रतिरक्षात्मक प्रतिक्रियाओं में सुधार करना बेहद महत्वपूर्ण है। यहां, हमने चयापचय नियमन में प्रतिरक्षा स्मृति की नई भूमिकाओं और एक स्वस्थ केंद्रीय तंत्रिका तंत्र को बनाए रखने की ओर इशारा करते हुए अनुसंधान का एक बड़ा निकाय भी प्रस्तुत किया। एक केंद्रीय नोड के रूप में प्रतिरक्षा के साथ, सभी कोणों से उम्र बढ़ने को स्वीकार करना, और उम्र बढ़ने से सर्वव्यापी रूप से प्रभावित सामान्य तंत्र को लक्षित करने वाले एंटी-एजिंग हस्तक्षेपों को डिजाइन करना आगे के शोध का एक समझदार तरीका है। व्यवहार संबंधी हस्तक्षेप जैसे कि कैलोरी प्रतिबंध और शारीरिक व्यायाम के साथ-साथ मेटफॉर्मिन और रेस्वेराट्रोल जैसे औषधीय एजेंट उम्र बढ़ने के कई पहलुओं को विनियमित करने में सक्षम हैं और पशु मॉडल और मनुष्यों में आशाजनक परिणाम मिले हैं। स्वस्थ हिम्मत, कार्यात्मक दिमाग और गंभीर संक्रमण से मुक्त लंबे जीवन जीने का प्रयास करने वाले मनुष्यों के लिए एक व्यापक रणनीति आवश्यक है।
घोषणाओं
हितों का टकराव लेखक कोई प्रतिस्पर्धी हितों की घोषणा नहीं करते हैं।
ओपन एक्सेस यह लेख क्रिएटिव कॉमन्स एट्रिब्यूशन 4 के तहत लाइसेंस प्राप्त है। 0 अंतर्राष्ट्रीय लाइसेंस, जो किसी भी माध्यम या प्रारूप में उपयोग, साझाकरण, अनुकूलन, वितरण और प्रजनन की अनुमति देता है, जब तक आप मूल लेखक को उचित श्रेय देते हैं। (एस) और स्रोत, क्रिएटिव कॉमन्स लाइसेंस के लिए एक लिंक प्रदान करें, और इंगित करें कि क्या परिवर्तन किए गए थे। इस आलेख में छवियों या अन्य तृतीय-पक्ष सामग्री को लेख के क्रिएटिव कॉमन्स लाइसेंस में शामिल किया गया है, जब तक कि सामग्री के लिए क्रेडिट लाइन में अन्यथा इंगित न किया गया हो। यदि सामग्री को लेख के क्रिएटिव कॉमन्स लाइसेंस में शामिल नहीं किया गया है और वैधानिक विनियमन द्वारा आपके इच्छित उपयोग की अनुमति नहीं है या अनुमत उपयोग से अधिक है, तो आपको सीधे कॉपीराइट धारक से अनुमति प्राप्त करने की आवश्यकता होगी। इस लाइसेंस की एक प्रति देखने के लिए, http://creativecommons.org/licenses/by/4 पर जाएं।0/।
यह लेख एलर्जी और इम्यूनोलॉजी में नैदानिक समीक्षाओं से निकाला गया है https://doi.org/10.1007/s12016-021-08905-x
