गुर्दे के विकास और रोग में हिस्टोन डीएसेटाइलिस की भूमिका
Feb 21, 2022
संपर्क करें:jerry.he@wecistanche.com
हांगबिंग लियू1
प्राप्त: 17 नवंबर 2019 / स्वीकृत: 10 नवंबर 2020 / ऑनलाइन प्रकाशित: 4 जनवरी 2021
©लेखक 2020

सिस्टैंच किडनी के कार्य में सुधार कर सकता है
सार
हिस्टोन डीएसेटाइलिस (एचडीएसी) महत्वपूर्ण एपिजेनेटिक नियामक हैं जो हिस्टोन और गैर-हिस्टोन प्रोटीन दोनों के डीसेटाइलेशन को मध्यस्थ करते हैं। एचडीएसी, विशेष रूप से कक्षा I एचडीएसी, विकास में अत्यधिक अभिव्यक्त होते हैंगुर्देऔर विकासात्मक नियंत्रण के अधीन है। HDACs एक महत्वपूर्ण भूमिका निभाते हैंगुर्दागठन, विशेष रूप से नेफ्रॉन पूर्वज रखरखाव और भेदभाव। साक्ष्य की कई पंक्तियाँ विभिन्न के विकास और प्रगति में एचडीएसी की महत्वपूर्ण भूमिका का समर्थन करती हैंगुर्दाबीमारी। HDAC अवरोधक (HDACis) गुर्दे की बीमारियों की रोकथाम और उपचार में बहुत प्रभावी हैं (सहित .)गुर्दाकैंसर)। रोगजनन और गुर्दे की बीमारी की प्रगति में एचडीएसी की भूमिका (ओं) में अंतर्निहित आणविक तंत्र की बेहतर समझ से अधिक प्रभावी और कम विषाक्त चयनात्मक एचडीएसी अवरोधक और कॉम्बीनेटरियल थैरेप्यूटिक्स विकसित करने में बहुत मदद मिलने की संभावना है।
कीवर्ड: हिस्टोन डीएसेटाइलेज़ · हिस्टोन डीएसेटाइलेज़ इनहिबिटर · किडनी रोग · किडनी कैंसर
परिचय
एपिजेनेटिक्स डीएनए अनुक्रम से स्वतंत्र रूप से जीन अभिव्यक्ति और विनियमन में आनुवंशिक परिवर्तनों के अध्ययन को संदर्भित करता है। हाल के वर्षों में स्वास्थ्य और रोग [1] में एपिजेनेटिक तंत्र की महत्वपूर्ण भूमिका के बारे में एक उभरती हुई जागरूकता देखी गई है। विकास के दौरान, एपिजेनेटिक संशोधन, जैसे डीएनए मिथाइलेशन, हिस्टोन एसिटिलिकेशन, और हिस्टोन मिथाइलेशन, क्रोमेटिन में क्रोमेटिन संरचना में परिवर्तन करके एक विशेष सेल में जीनोम प्रोग्रामिंग निर्धारित करने के लिए सेट किए जाते हैं और इस प्रकार ट्रांसक्रिप्शनल मशीनरी के लिए डीएनए पहुंच। पर्यावरणीय जोखिम (जैसे, आहार, विषाक्त पदार्थ, दवाएं, वायरल संक्रमण) के परिणामस्वरूप इन एपिजेनेटिक संशोधनों के विघटन से डीएनए अनुक्रम में बदलाव किए बिना, जीन फ़ंक्शन का अपचयन हो सकता है [1-3]। जैसा कि एपिजेनेटिक असामान्यताएं जीन और पर्यावरण के बीच परस्पर क्रिया पर निर्भर करती हैं, वे अक्सर फेनोटाइपिक रूप से परिवर्तनशील होते हैं, जो कि जन्मजात विसंगतियों के व्यापक फेनोटाइपिक स्पेक्ट्रम के साथ अच्छी तरह से फिट होते हैं।गुर्दाऔर मूत्र पथ (CAKUT) और एक अन्य गुर्दे की बीमारी [4–9]। इसलिए,
* होंगबिंग लियू
hliu8@tulane.edu
बाल रोग विभाग और तुलाने उच्च रक्तचाप और रेनल सेंटर ऑफ एक्सीलेंस, तुलाने यूनिवर्सिटी स्कूल ऑफ मेडिसिन, SL-37, 1430 तुलाने एवेन्यू, न्यू ऑरलियन्स,
एलए 70112, यूएसए
गुर्दे के विकास के एपिजेनेटिक आधार को समझने से किडनी के रोग तंत्र में नई अंतर्दृष्टि मिल सकती है और उम्मीद है कि एपिजेनेटिक संशोधक को लक्षित करने वाले फार्मास्युटिकल एजेंटों के माध्यम से CAKUT के उपचार या रोकथाम के लिए नए रास्ते खोल सकते हैं। ऐसी एपिजेनेटिक दवाएं पहले से ही नैदानिक उपयोग में हैं या कैंसर के साथ-साथ अन्य बीमारियों के इलाज के लिए जांच के अधीन हैं [10]।
हिस्टोन एसिटिलिकेशन एक एसिटाइल समूह के सहसंयोजक जोड़ को एक लाइसिन की ओर ले जाता है। हिस्टोन पूंछ के शुद्ध सकारात्मक चार्ज को बेअसर करके और नकारात्मक रूप से चार्ज किए गए डीएनए के बंधन को कम करके, इस तरह के अतिरिक्त परिणाम स्थानीय खुले क्रोमैटिन, सक्रिय प्रतिलेखन का एक निशान है। इसके विपरीत, निष्क्रिय किए गए हिस्टोन डीएनए के साथ दृढ़ता से बातचीत करते हैं और परिणामस्वरूप स्थानीय क्लोज क्रोमैटिन, निष्क्रिय प्रतिलेखन का एक निशान होता है। प्रमोटर और एन्हांसर हिस्टोन का डिफरेंशियल एसिटिलेशन विकासात्मक प्रक्रियाओं, सेलुलर प्रसार और विभेदन में एक बहुत ही महत्वपूर्ण नियामक भूमिका निभाता है। एबरैंट एसिटिलेशन या डीसेटाइलेशन से ल्यूकेमिया, एपिथेलियल कैंसर, नाजुक एक्स सिंड्रोम और रुबिनस्टीन-तैबी सिंड्रोम [11] जैसे विविध विकार होते हैं। हिस्टोन डीएसेटाइलिस (एचडीएसी) क्रमिक रूप से संरक्षित एंजाइमों का एक बड़ा परिवार है जो हिस्टोन पूंछ से एसिटाइल समूहों को हटाने के लिए उत्प्रेरित करता है। एचडीएसी की क्रिया हिस्टोन एसिटाइलट्रांसफेरेज़ (एचएटी) द्वारा प्रतिकारित की जाती है, जो एसिटाइल हिस्टोन पूंछ करती है। अब तक, 18 स्तनधारी एचडीएसी की पहचान की जा चुकी है। फाईलोजेनेटिक विश्लेषण और उनके कार्यों के अनुसार, एचडीएसी को चार वर्गों में बांटा गया है: कक्षा 1 (एचडीएसी 1-3, और 8), कक्षा II (एचडीएसी 4-7, 9-10), कक्षा III (सर 2/ Sirt 1-7), और चतुर्थ श्रेणी (Hdac11)। कक्षा I, II और IV को अपनी उत्प्रेरित गतिविधि के लिए जस्ता की आवश्यकता होती है, जबकि कक्षा III के सदस्य गतिविधि के लिए NAD पर निर्भर होते हैं। उनमें से, कक्षा I एचडीएसी का व्यापक अध्ययन किया गया है और उनकी विशेषता बताई गई है। यह देखते हुए कि हिस्टोन एसिटिलिकेशन आमतौर पर सक्रिय प्रतिलेखन से जुड़ा होता है, एचडीएसी को मूल रूप से सामान्य ट्रांसक्रिप्शनल सह-दमनकर्ता माना जाता था। हालांकि, बाद में, यह स्पष्ट हो गया कि एचडीएसी अत्यधिक चयनात्मक तरीके से जीन अभिव्यक्ति को विनियमित करते हैं और दमनकारी और सक्रिय दोनों प्रभाव प्रदर्शित करते हैं [12]। आंतरिक डीएनए बाध्यकारी गतिविधियों की कमी के कारण, एचडीएसी विभिन्न मौलिक जैविक प्रक्रियाओं [12] में अपने कार्यों के लिए अकेले काम नहीं कर सकता है।
यह स्पष्ट हो गया है कि एचडीएसी हिस्टोन के अलावा कई सबस्ट्रेट्स पर भी कार्य कर सकता है। विभिन्न HDACs के हिस्टोन सब्सट्रेट विशिष्टता को निर्धारित करना कठिन है। मुख्य कारण यह है कि कई शुद्ध HDACs में बहुत कम deacetylation गतिविधि और विभिन्न HDACs [13] के कार्यात्मक अतिरेक होते हैं। एचडीएसी के एक सदस्य का नुकसान या खराबी समग्र हिस्टोन एसिटिलेशन को बदलने के लिए पर्याप्त नहीं हो सकता है। इसके अलावा, एचडीएसी को ट्रांसक्रिप्शनल कॉम्प्लेक्स (जैसे सिन 3 कॉम्प्लेक्स, एनयूआरडी कॉम्प्लेक्स, और को-आरईएसटी कॉम्प्लेक्स) [14] के सहयोग से जीन को लक्षित करने के लिए भर्ती किया जाता है। इस प्रकार, जीन विनियमन में एचडीएसी की विशिष्टता अलग-अलग सेल प्रकारों के भीतर सहयोगी प्रोटीन पर निर्भर करती है। हालाँकि कक्षा I HDAC के तीन सदस्य (HDAC1, HDAC2 और HDAC3) आम तौर पर समान अनुक्रम सुविधाएँ साझा करते हैं, कुछ अध्ययनों से पता चला है कि HDAC3 (और शायद सभी वर्ग I HDACs) में अलग सब्सट्रेट विशिष्टता [15, 16] है। बहुत संभव है, प्रत्येक HDAC का कुछ सबस्ट्रेट्स में अपना विशिष्ट लक्ष्य होता है, जिसके लिए अधिक व्यापक जांच की आवश्यकता होती है। लगभग सभी एंजाइमों की तरह, एचडीएसी को उनकी गतिविधियों के लिए कार्यात्मक रूप से विनियमित किया जाता है। विभिन्न स्तरों पर कई विनियमन तंत्रों में, प्रोटीन-प्रोटीन इंटरैक्शन और पोस्ट-ट्रांसलेशन मॉडिफिकेशन (पीटीएम) दो अच्छी तरह से विकसित तंत्र हैं। कई एचडीएसी अकेले काम नहीं करते हैं बल्कि एक मल्टीप्रोटीन कॉम्प्लेक्स में एक घटक के रूप में कार्य करते हैं, जो व्यक्तिगत एचडीएसी को अपनी उत्प्रेरक गतिविधि को अधिक प्रभावी और विशिष्ट तरीके से करने में मदद करते हैं [17]। एचडीएसी के लिए बड़े प्रोटीन परिसरों के गठन के माध्यम से कार्य करना बहुत आम है। व्यापक जैव रासायनिक विश्लेषणों से पता चला है कि HDAC1 और HDAC2 तीन प्रमुख मल्टीप्रोटीन सह-दमनकर्ता परिसरों में सह-अस्तित्व में हैं: Sin3, NuRD (न्यूक्लियोसोम रीमॉडेलिंग और डीसेटाइलेशन) और CoREST (तत्व के लिए सह-दमनकर्ता -1- साइलेंसिंग ट्रांसक्रिप्शन कारक) [14 ]. एचडीएसी न केवल प्रोटीन संशोधक हैं, वे विभिन्न पीटीएम के अधीन भी हो सकते हैं। फास्फोराइलेशन सबसे व्यापक अध्ययन संशोधन है। HDAC1 को कैसिइन किनसे (CK2) और सीएमपी-आश्रित किनसे PKA [18] द्वारा फॉस्फोराइलेट किया जा सकता है। HDAC1 की एंजाइमिक गतिविधि के लिए Serine (S) 421 और S423 दोनों में फॉस्फोराइलेशन आवश्यक है, और इन दोनों साइटों के उत्परिवर्तन इसकी गतिविधि और जटिल गठन को महत्वपूर्ण रूप से कम करते हैं। CK2 422 और 424 (HDAC1 के S421 और S423 के समरूप) साइटों पर HDAC2 को फास्फोराइलेट कर सकता है, और S394 पर, HDAC2 [19] की मुख्य फास्फोराइलेशन साइट। लगातार, हमने विकासशील में S394 फॉस्फोराइलेटेड HDac2 की उपस्थिति भी पाई।गुर्देमास स्पेक्ट्रोमेट्री विश्लेषण के माध्यम से (लियू एट अल।, अप्रकाशित)। इसके अलावा, HDAC1 और HDAC2 के फॉस्फोराइलेशन को प्रोटीन फॉस्फेटस PP1 [20] द्वारा विपरीत रूप से नियंत्रित किया जाता है। अध्ययनों से यह भी पता चला है कि PP2A मानव हृदय में HDAC2 के S394 को डीफॉस्फोराइलेट करके हाइपरट्रॉफिक प्रतिक्रिया को नियंत्रित करता है [21]। सामूहिक रूप से, एचडीएसी महत्वपूर्ण एपिजेनेटिक न्यूनाधिक हैं और कई जैविक प्रक्रियाओं में भूमिका निभाते हैं। उनकी गतिविधियों को कई तंत्रों द्वारा कसकर नियंत्रित किया जाता है, जैसे प्रोटीन-प्रोटीन इंटरैक्शन, और पीटीएम। मल्टीप्रोटीन कॉम्प्लेक्स का निर्माण न केवल एचडीएसी की गतिविधि बल्कि उनकी सब्सट्रेट विशिष्टता को भी निर्धारित करता है। एचडीएसी द्वारा आणविक परिवर्तन मानव स्वास्थ्य और रोग पर एक महत्वपूर्ण प्रभाव डालने की संभावना है। इस समीक्षा में, हम एचडीएसी की भूमिकाओं का वर्णन करना चाहेंगेगुर्दाविकास और रोग।

गुर्दे के विकास में एचडीएसी की भूमिका
कक्षा I HDAC की सर्वव्यापी अभिव्यक्ति और उच्च डीएसेटाइलेज़ गतिविधि उनके कार्यात्मक महत्व के अनुरूप हैं। HDAC1 पारंपरिक नॉक-आउट चूहे भ्रूण के लिए घातक होते हैं, जिसके परिणामस्वरूप गंभीर प्रसार दोष और विकास मंदता [22] होती है। हैरानी की बात है कि HDAC1 की सशर्त दस्तक कई ऊतकों में अच्छी तरह से सहन की जाती है और चूहे व्यवहार्य होते हैं, बाद के विकास और प्रसवोत्तर जीवन में HDAC1 और HDAC2 के कार्यात्मक अतिरेक के कारण बहुत संभव है [22]। HDAC 1 और HDAC2 का सह-विलोपन जांचे गए सभी ऊतकों के लिए हानिकारक है [22]। इसके अलावा, HDAC 2-अशक्त चूहे जन्म के बाद 24 घंटे के भीतर हृदय की शिथिलता के कारण मर जाते हैं [22]। मेंगुर्दा, HDACs सर्वव्यापी और अत्यधिक अभिव्यक्त होते हैं। RT-PCR विश्लेषण इंगित करता है कि HDAC1, 2, 3, 4, 7, 9 विकासात्मक नियंत्रण के अधीन हैं और भ्रूण से नवजात और वयस्क जीवन में परिपक्वता के दौरान महत्वपूर्ण रूप से गिरावट [23] है। पश्चिमी धब्बा विश्लेषणगुर्दापरमाणु lysates आगे पुष्टि करते हैं कि HDac1–3 प्रोटीन भ्रूण में अत्यधिक प्रचुर मात्रा में होते हैंगुर्दाऔर प्रसवोत्तर [23] डाउन-रेगुलेटेड हैं। इम्यूनोस्टेनिंग से पता चलता है कि एचडीएसी 1 और 2 नवजात शिशु (पी 0) चूहों के गुर्दे में विकासशील गुर्दे की अलग-अलग आबादी में अत्यधिक व्यक्त किए जाते हैं, जिनमें अविभाजित मेटानेफ्रिक मेसेनचाइम, ब्रांचिंग यूरेरिक बड्स और स्ट्रोमा (चित्र। 1) शामिल हैं। ) Hdac1 और 2 अतिव्यापी और विशेष रूप से विकासशील और P21 किडनी (चित्र 1) में व्यक्त परमाणु में हैं। विकास में HDac3 की उच्च अभिव्यक्ति का भी पता चला थागुर्दापोडोसाइट्स सहित। इसके विपरीत, एचडीएसी 5, 6, और 8 संवैधानिक रूप से व्यक्त किए जाते हैं। रीनल माइक्रोवास्कुलचर एचडीएसी 7, 8 और 9 [24] को व्यक्त करता है। सामूहिक रूप से, कक्षा I और वर्ग II HDAC जीन को के दौरान अलग-अलग विनियमित किया जाता हैगुर्दाविकास। गुर्दे में सभी एचडीएसी की अभिव्यक्ति को हाल ही में एक समीक्षा [25] द्वारा अच्छी तरह से प्रलेखित किया गया था।

अंजीर। 1 नवजात (पी 0) (ए, बी) और पी 21 (सी, डी) चूहों के गुर्दे में क्रमशः एचडीएसी 1 और एचडीएसी 2 की उच्च अभिव्यक्ति और परमाणु स्थानीयकरण
हालांकि, HDACs का स्थानिक और अस्थायी रूप से प्रतिबंधित वितरण हिस्टोन H3 और H4 के वैश्विक एसिटिलीकरण स्तरों को नहीं बदलता है, जो सामान्य विकास के दौरान HAT और HDAC कार्यों के एक तंग युग्मन का सुझाव देता है [23]।
कक्षा I में HDAC, HDAC1 और HDAC2 क्रमिक रूप से एक-दूसरे से संबंधित हैं और दोनों बहुत प्रचुर मात्रा में कई ऊतकों में व्यक्त किए जाते हैं। HDAC1 और HDAC2 होमो- या हेटेरोडिमर्स बना सकते हैं और लगभग सभी परमाणु प्रोटीन परिसरों में एक साथ पाए जाते हैं, जिनमें तीन अच्छी तरह से विशेषता वाले सह-दमनकर्ता परिसर शामिल हैं: Sin3, NuRD और Co-REST [14, 26]। Hoxb7-Cre के साथ मूत्रवाहिनी कली (UB) वंश में Hdac1 और Hdac2 के सशर्त विलोपन से, अध्ययनों से पता चला है कि Hdac1 और Hdac2 के तीन से अधिक हटाए गए एलील वाले चूहों में गुर्दे के विकास में कोई महत्वपूर्ण असामान्यताएं नहीं दिखाई देती हैं [27] . ये चूहे वृद्धि या विकास में किसी भी असामान्यता के बिना वयस्कता तक जीवित रह सकते हैं। इसके विपरीत, Hdac1 और Hdac2 के सभी चार एलील के समवर्ती विलोपन के परिणामस्वरूप 2-4 सप्ताह की आयु [27] तक प्रसवोत्तर मृत्यु हो जाती है।गुर्दाP0 पर नॉकआउट चूहों के ऊतक नेफ्रोजेनिक ज़ोन की अनुपस्थिति, कॉर्टिकल-मेडुलरी पैटर्निंग की कमी, और कई उपकला सिस्ट के गठन को दिखाया, जो एक महत्वपूर्ण भूमिका और एचडीएसी 1 और एचडीएसी 2 की कार्यात्मक अतिरेक का सुझाव देते हैं।गुर्दागठन और कार्य [27]। अध्ययनों से यह भी पता चलता है कि UB एपिथेलियम में Hdac1 और Hdac2 के नुकसान से p53 स्थिरता और ट्रांसक्रिप्शनल गतिविधि [27] को बढ़ावा देने के लिए ट्यूमर शमन प्रोटीन p53 के चिह्नित हाइपरसेटिलेशन की ओर जाता है। जबकि p53 एक बहुत ही महत्वपूर्ण ट्यूमर शमन है, अप्रतिबंधित p53 गतिविधि गुर्दे के निर्माण के लिए हानिकारक है, सबसे अधिक संभावना अनुचित सेलुलर मृत्यु या प्रसार दोष [28] के कारण है।
गुर्दाजिले के शारीरिक कार्यों के साथ कई विशिष्ट प्रकार के सेल शामिल हैं।गुर्दास्तनधारियों में गठन दो प्रकार के ऊतकों, मूत्रवाहिनी कली और मेटानेफ्रिक मेसेनचाइम [5, 29-31] के बीच पारस्परिक बातचीत से शुरू होता है। सिक्स2 प्लस कैप मेसेनचाइम एक बहुशक्तिशाली स्व-नवीनीकरण नेफ्रॉन पूर्वज कोशिकाएं (एनपीसी) है जो कार्यात्मक नेफ्रॉन एपिथेलियम [3 0] को जन्म देती है। NPC रखरखाव और विभेदीकरण में HDAC1 / 2 की भूमिका में अंतर्दृष्टि प्राप्त करने के लिए, हमने सशर्त रूप से Hdac1 और Hdac2 को सिक्स2eGFPCre (Six2TGC) चूहों [30] के साथ हटा दिया। एनपीसी के साथ चूहे- एचडीएसी1 और एचडीएसी2 (सभी चार एलील) के दोहरे विलोपन के साथ चूहे सामान्य मेंडेलियन अनुपात में पैदा हुए थे, लेकिन जन्म के तुरंत बाद उनकी मृत्यु हो गई [4]। प्रसवोत्तर दिन (पी) 0 पर उत्परिवर्ती गुर्दे छोटे दिखाई दिएगुर्दाआकार, नेफ्रोजेनिक क्षेत्र की अनुपस्थिति, नवजात नेफ्रॉन और ग्लोमेरुली की कमी, और कई सिस्ट का गठन [4]। यूबी वंश में एचडीएसी1 और एचडीएसी2 विलोपन के समान, एचडीएसी1 या एचडीएसी2 में से एक एलील नेफ्रोजेनेसिस [4] सुनिश्चित करने के लिए पर्याप्त है। हमारे परिणामों से पता चला है कि नेफ्रॉन पूर्वजों और वृक्क पुटिकाओं [4] के ट्रांसक्रिप्शनल कार्यक्रमों को विनियमित करने के लिए हिस्टोन डीएसेटाइलिस 1 और 2 (एचडीएसी 1/2) आवश्यक हैं। HDAC1 / 2 नेफ्रोजेनेसिस के दौरान NPC के स्व-नवीकरण और विभेदन को संतुलित करने के लिए दोहरी भूमिका निभाते हैं (चित्र 2): एक ओर, HDAC1 / 2 सभी मार्कर जीन (जैसे सिक्स 2, Sall1) की अभिव्यक्ति के लिए आवश्यक हैं। और Osr1) एनपीसी में और इन कोशिकाओं का स्व-नवीकरण; दूसरी ओर, वे विहित Wnt लक्ष्य जीन की अभिव्यक्ति को दबाने और NPCs को पूर्व-परिपक्व अंतर से रोकने के लिए भी महत्वपूर्ण हैं। हमारे जैव रासायनिक और चिप विश्लेषणों से यह भी पता चला है कि HDAC1 और HDAC2, सिक्स2, Osr1 और Sall1 के साथ परस्पर क्रिया करते हैं, जो ट्रांसक्रिप्शनल रेगुलेटरों का एक नेटवर्क है जो NPC प्रसार और विभेदन के संतुलन को बनाए रखता है [4]। सिक्स2 विकासशील किडनी में एक मास्टर ट्रांसक्रिप्शन कारक है और एनपीसी के भेदभाव को दोहराकर और स्व-नवीकरण को चलाकर, स्व-नवीनीकरण के एक कार्यात्मक पूल को बनाए रखने में एक केंद्रीय भूमिका निभाता है। सिक्स2 और एचडीएसी1/2 को अविभाजित एनपीसी में सह-व्यक्त किया गया है और सभी नेफ्रॉन पूर्वज कोशिकाओं के रखरखाव और समय से पहले विभेदन की रोकथाम के लिए आवश्यक हैं [4]। हम तर्क देते हैं कि एनपीसी के स्व-नवीकरण और विभेदीकरण को ठीक से नियंत्रित करने के लिए सिक्स2 के दोहरे कार्य के लिए HDAC1 / 2 की आवश्यकता है। एचडीएसी न केवल हिस्टोन प्रोटीन बल्कि गैर-हिस्टोन प्रोटीन [12] को भी डीसेटाइलेट कर सकता है। एसिटिलीकरण सेट संवर्धन आधारित (एएसईबी) कंप्यूटर प्रोग्राम [32] द्वारा सिलिको भविष्यवाणी में पी300 द्वारा सिक्स2 एसिटिलीकरण और एचडीएसी1/2 (तालिका 1) द्वारा डीसेटाइलेशन के लिए जिम्मेदार कई संभावित साइटों को इंगित करता है। उनमें से, Lysine (K) 46, K52, और K71, सिक्स 2 के सिक्स डोमेन (1-124) डोमेन पर स्थित हैं, और K138 सिक्स2 [33] के होम्योडोमैन पर स्थित है। अध्ययनों से पता चला है कि सिक्स डोमेन में नाभिक की अधिक मजबूत प्रवृत्ति होती है
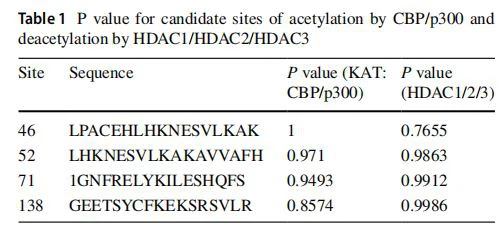
संचय और सिक्स डोमेन और होमोडोमैन से युक्त एक प्रोटीन विशेष रूप से नाभिक [33] पर पाया गया था। इसलिए, इन संभावित साइटों के एसिटिलीकरण की संभावना सिक्स2 प्रोटीन और / या ट्रांसक्रिप्शनल गतिविधि के नाभिक स्थानीयकरण से जुड़ी होगी। हाल ही में, हमारे जीनोम-वाइड विश्लेषण से पता चला है कि एचडीएसी 1 और सिक्स 2 एनपीसी नवीकरण जीन के बढ़ाने वाले क्षेत्रों पर कब्जा कर लेते हैं और एचडीएसी 1 का बंधन एनपीसी [34] में सक्रिय रूप से संचरित जीन के प्रमोटर क्षेत्र में खुले क्रोमैटिन को इंगित करता है। कैसे HDAC1/2 सिक्स2 फ़ंक्शन को नियंत्रित करता हैगुर्दाविकास निश्चित रूप से आगे की जांच का वारंट करता है।
स्तनधारीगुर्दामेटानेफ्रिक मेसेनचाइम और मूत्रवाहिनी कली के बीच पारस्परिक बातचीत से विकसित होता है। स्ट्रोमा, तीसरा वंश जो अंतरालीय स्थान को भरता है, अलग-अलग पूर्वजों से प्राप्त होता है जो प्रतिलेखन कारक फॉक्सड1 [35] को व्यक्त करते हैं। अध्ययनों से पता चलता है कि फॉक्सड1 कॉर्टिकल स्ट्रोमा को व्यक्त करने वाली एक बहुशक्तिशाली स्व-नवीनीकरण पूर्वज आबादी है, जो कॉर्टिकल और मेडुलरी इंटरस्टीशियल कोशिकाओं, मेसेंजियल कोशिकाओं और पेरिसाइट्स को जन्म देगी।गुर्दा[35]। HDAC1 और HDAC2 भी विकास के स्ट्रोमा में अधिक व्यक्त किए जाते हैंगुर्दे[4, 23, 27]। स्ट्रोमा वंश में दो HDAC की भूमिका की जांच करने के लिए, हम Foxd1-Cre [36] के साथ HDAC1 और HDAC2 को सशर्त रूप से हटाने के लिए एक माउस मॉडल का उपयोग कर रहे हैं। हमारी
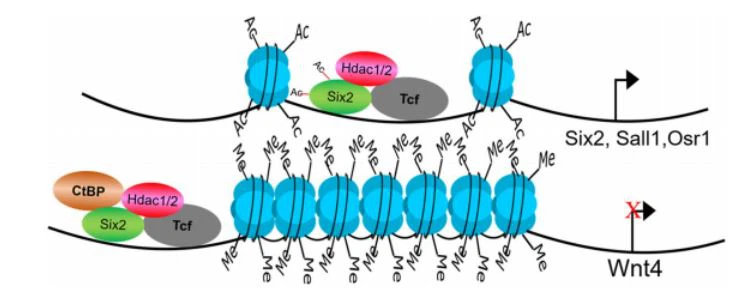
चित्र 2 HDAC1 / 2 नेफ्रोजेनेसिस के दौरान NPC के स्व-नवीकरण और विभेदीकरण को संतुलित करने के लिए दोहरी भूमिका निभाते हैं
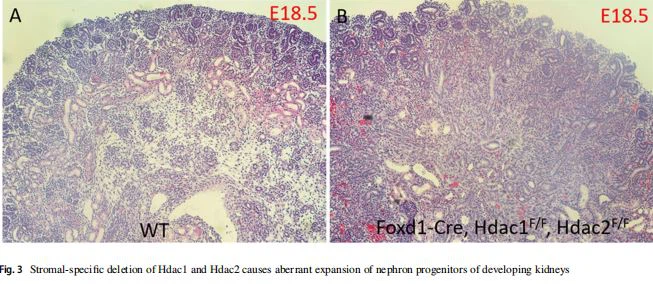
प्रारंभिक परिणामों से पता चला है कि स्ट्रोमल जनक में विशिष्ट HDAC1 / 2 विलोपन से नेफ्रॉन जनक (चित्र 3) का अचानक विस्तार होता है, इसी तरह का फेनोटाइप फॉक्सड में देखा गया है 1- Cre संचालित Sall1 विलोपन या वृक्क स्ट्रोमा का उन्मूलन [37 , 38]। अत्यधिक नेफ्रॉन विस्तार को प्रतिबंधित और विनियमित करने के लिए स्ट्रोमल एचडीएसी 1/2 कैसे आगे लक्षण वर्णन गुर्दे के गठन के एपिजेनेटिक विनियमन और स्ट्रोमल और नेफ्रॉन के बीच क्रॉस टॉक की दिशा में हमारी समझ को आगे बढ़ाने में मदद करेगा।
एचडीएसी और रीनल इंटरस्टिशियल फाइब्रोसिस
क्रोनिक किडनी रोग (सीकेडी) एक तेजी से पहचाना जाने वाला सार्वजनिक स्वास्थ्य मुद्दा है और गुर्दे के कार्य में क्रमिक और अपरिवर्तनीय गिरावट द्वारा चिह्नित किया गया है। रीनल इंटरस्टीशियल फ़्रब्रोसिस सीकेडी की पहचान है। रेनल इंटरस्टीशियल fbro- वृक्क ट्यूबलर शोष, बाह्य मैट्रिक्स (ECM) के असामान्य जमाव और fbroblasts के प्रगतिशील विस्तार की विशेषता है। अंतर्निहित रोगजनक तंत्र जटिल और विविध हैं। संचित साक्ष्यों से पता चला है कि HDACs रीनल इंटरस्टिशियल फ़ब्रोसिस के रोगों में भाग लेते हैं और HDAC निषेध मुख्य रूप से निम्नलिखित तंत्रों के माध्यम से एंटी-फ़्रब्रोटिक प्रभाव डालता है: (1) प्रो-फ़ब्रोटिक टीजीएफ-सिग्नलिंग को दबाने, (2) ट्यूबलर को रोकने एपिथेलिया सेल एपोप्टोसिस, और (3) बोन मॉर्फोजेनेसिस प्रोटीन 7 (बीएमपी7) [39] की अभिव्यक्ति में वृद्धि। ट्रांसफ़ॉर्मिंग ग्रोथ फ़ैक्टर बीटा (TGF-) ट्रांसफ़ॉर्मिंग ग्रोथ फ़ैक्टर का एक सदस्य है, जो विभिन्न जैविक प्रक्रियाओं के नियमन में आवश्यक है। स्तनधारियों में, टीजीएफ के तीन समस्थानिकों की पहचान की गई हैगुर्दा: टीजीएफ- 1, टीजीएफ- 2, और टीजीएफ- 3। उनमें से, टीजीएफ - 1 स्मॉड और गैर-स्मैड मार्गों के माध्यम से अपनी जैविक गतिविधि को बढ़ाता है और गुर्दे की फब्रोसिस में इसकी भूमिका सबसे अच्छी विशेषता है (यू एट अल। 2003; मेंग एट अल। 2016)। में टीजीएफ- 1 का अबाध सक्रियणगुर्दाfbroblast प्रसार को बढ़ावा देने और असामान्य बाह्य मैट्रिक्स [40] के जमाव को बढ़ावा देकर बीचवाला fbrosis का कारण बनता है। पहले के अध्ययनों से पता चला है कि ट्राइकोस्टैटिन ए (टीएसए), एक पैन एचडीएसी इनहिबिटर (एचडीएसी) दोनों वर्ग I और वर्ग II एचडीएसी के साथ उपचार, एकतरफा मूत्रवाहिनी बाधा (यूयूओ) माउस मॉडल [41] में गुर्दे की फ़्रब्रोसिस को कम करता है। टीएसए उपचार भी महत्वपूर्ण रूप से निष्क्रिय fbroblasts। इसके अलावा, HDAC1 या HDAC2 की साइलेंसिंग ने STAT3 (सिग्नल ट्रांसड्यूसर और ट्रांसक्रिप्शन 3 के एक्टिवेटर) के फॉस्फोराइलेशन को कम करके रीनल फ़ब्रोब्लास्ट प्रसार को अवरुद्ध कर दिया, जो एक सिग्नलिंग अणु है जो रीनल फ़ब्रो-ब्लास्ट के प्रसार और रीनल फ़ब्रोसिस [42] के विकास से जुड़ा है। आगे के अध्ययनों से पता चला है कि टीएसए उपचार बीएमपी -7 की अभिव्यक्ति को भी बढ़ाता है और गुर्दे की चोट [43, 44] के रोगजनन को कम करता है। चूंकि बीएमपी -7 टीजीएफ के खिलाफ सुरक्षा को प्रेरित करता है - - मध्यस्थता वाले गुर्दे की फाइब्रोसिस, बीएमपी की बहाली -7 अभिव्यक्ति एक अन्य प्रमुख तंत्र का प्रतिनिधित्व करती है जिसके द्वारा एचडीएसी निषेध प्रगतिशील सीकेडी को रोकता है [44]। इसके अलावा, MS-275 या Fk228 (कक्षा I HDACs के चयनात्मक अवरोधक) का प्रशासन वृक्क fbroblast सक्रियण और प्रसार को रोककर किडनी फ़्रब्रोसिस की प्रगति को महत्वपूर्ण रूप से कम करता है, यह सुझाव देता है कि कक्षा I HDACs वृक्क फेब्रोसिस में प्रमुख भूमिका निभाते हैं [45, 46]।
सामूहिक रूप से, HDACs वृक्क fbro-blast सक्रियण और वृक्क अंतरालीय fbrosis में महत्वपूर्ण भूमिका निभाते हैं, और HDACs (विशेष रूप से कक्षा I HDACs) के अवरोधकों का उपयोग इसलिए वृक्क फ़्रब्रोसिस को कम करने और उपचार करने के लिए प्रभावी चिकित्सा प्रदान कर सकता है।
एचडीएसी और मधुमेहगुर्दाबीमारी
मधुमेह दुनिया में 451 मिलियन से अधिक लोगों को प्रभावित करता है और मधुमेह अपवृक्कता (डीएन,गुर्दामधुमेह में रोग) सीकेडी का सबसे आम कारण है। अंतिम चरणगुर्दाडिस-ईज (ESKD) CKD का अंतिम चरण है। यह तब होता है जब दोनों गुर्दे शरीर की दैनिक जीवन की जरूरतों को पूरा नहीं कर पाते हैं। संयुक्त राज्य अमेरिका में ESRD के सबसे आम कारण मधुमेह और उच्च रक्तचाप [47] हैं। ग्लोमेरुलर मेसेंजियम और ट्यूबलोइंटरस्टिटियम में ईसीएम का प्रगतिशील संचय डीएन की पहचान है। कई प्रीक्लिनिकल अध्ययनों ने मधुमेह के गुर्दे की बीमारी [48, 49] के प्रायोगिक मॉडल में एचडीएसी निषेध की प्रभावशीलता का प्रदर्शन किया है। प्रारंभिक अध्ययनों ने स्ट्रेप्टोजोटोकिन (एसटीजेड) से प्रेरित मधुमेह में एचडीएसी2 गतिविधि में वृद्धि की सूचना दी।गुर्देऔर चूहे की किडनी समीपस्थ ट्यूबलर उपकला कोशिकाएं (NRK-52E) TGF के संपर्क में आती हैं- 1 [50]। HDAC2 के siRNA नॉक-डाउन ने NRK-52E कोशिकाओं में फ़ाइब्रोनेक्टिन और -SMA की अभिव्यक्ति को कम कर दिया। टीएसए उपचार ने ईसीएम घटकों की अभिव्यक्ति को कम कर दिया और उपकला-मेसेनकाइमल-संक्रमण (ईएमटी) को रोका। वैल्प्रोइक एसिड (VPA) (एक अन्य HDACI/II अवरोधक) या SK704 (चयनात्मक वर्ग I HDAC अवरोधक) का NRK -52E कोशिकाओं पर समान प्रभाव देखा गया, जो विकास में वर्ग I HDAC की आवश्यक भूमिका का समर्थन करता है। मधुमेह गुर्दे की बीमारी [50]।
प्रतिक्रियाशील ऑक्सीजन प्रजातियों (आरओएस) के कारण एंडोप्लाज्मिक रेटिकुलम (ईआर) तनाव डीएन विकास [51] से जुड़ा है। एपिडर्मल ग्रोथ फैक्टर रिसेप्टर (ईजीएफआर) ऑक्सीडेटिव तनाव की मध्यस्थता करता है और ईजीएफआर सक्रियण को डायबिटिक चूहों में फंसाया गया था। ईजीएफआर/एकेटी/आरओएस/ईआर तनाव संकेतन डीएन प्रगति में एक आवश्यक भूमिका निभाता है और ईजीएफआर को रोकना डीएन [51] में संभावित चिकित्सीय रणनीति के रूप में काम कर सकता है। अध्ययनों से पता चला है कि 4 सप्ताह के लिए डायबिटिक चूहों के वोरीनोस्टैट के उपचार से ईजीएफआर स्तर में काफी कमी आई और दमित हो गयागुर्दाविकास और ग्लोमेरुलर हाइपरट्रॉफी, यह दर्शाता है कि एचडीएसी ईजीएफआर सक्रियण [48] के माध्यम से प्रारंभिक डीएन में भूमिका निभा सकते हैं।
पोडोसाइट्स अंतत: विभेदित उपकला कोशिकाएं हैं और इसका एक महत्वपूर्ण घटक प्रस्तुत करते हैंगुर्दाफ़्लर्टेशन बैरियर [52]। पोडोसाइट क्षति गुर्दे की फ़्लर्टेशन बाधा अखंडता के नुकसान के माध्यम से डीएन की प्रगति को तेज करती है, जिसके परिणामस्वरूप प्रोटीन मूत्र (प्रोटीनुरिया) से बच जाता है [52]। डेटाबेस विश्लेषण के साथ, प्रोटीन्यूरिक चूहों के ग्लोमेरुली से माइक्रोएरे में उच्च HDAC1 और HDAC2 गतिविधि का पता चला था (इनौ एट अल। 2019)। हाल के अध्ययनों ने murine और मानव ग्लोमेरुलर रोग के नियमन में पॉडोसाइट HDAC गतिविधि की महत्वपूर्ण भूमिका का प्रदर्शन किया, और दृढ़ता से सुझाव दिया कि HDAC1 और HDAC2 गतिविधियों का निषेध मानव प्रोटीनयुक्त गुर्दे की बीमारी की प्रगति को दबा सकता है। VPA (एक वर्ग I HDAC अवरोधक, FDA-अनुमोदित दवा) और सुबेरानिलोहाइड्रॉक्सैमिक एसिड (SAHA) के प्रशासन ने प्रोटीनुरिया को कम किया और कई कृंतक ग्लोमेरुलर चोट मॉडल में ग्लोमेरुलोस्केलेरोसिस के विकास को कम किया। Podocye- विशिष्ट HDAC1 और HDAC2 पृथक चूहों प्रगतिशील ग्लोमेरुलोस्केलेरोसिस के प्रतिरोधी थे। इसके अलावा, वयोवृद्ध उम्र बढ़ने कोहोर्ट अध्ययन में 120, 000 प्रतिभागियों के अनुदैर्ध्य विश्लेषण ने अनुमानित ग्लोमेरुलर फ़्लोट्रेशन दर [52] की गिरावट पर वीपीए उपचार के एक मजबूत सुरक्षात्मक प्रभाव का प्रदर्शन किया।
संक्षेप में, मधुमेह के कारण गुर्दे की बीमारी क्रोनिक किडनी की विफलता का सबसे आम कारण बनी हुई है, और एचडीएसीआई मधुमेह के गुर्दे की बीमारी के इलाज के लिए नैदानिक लाभ प्रदान करता है।
एचडीएसी और रीनल कार्सिनोमा
विभिन्न प्रकार के कैंसर में HDAC अवरोधकों का बड़े पैमाने पर अध्ययन किया गया है। रेनल सेल कार्सिनोमा (आरसीसी) सबसे आम हैगुर्दाकैंसर और संयुक्त राज्य अमेरिका में वयस्क कैंसर का 2-3 प्रतिशत हिस्सा [53]। कक्षा I HDACs, विशेष रूप से HDAC1, 2, और 3 को RCC में अत्यधिक अभिव्यक्त किया जाता है, जिससे वे चिकित्सा के लिए दिलचस्प लक्ष्य बन जाते हैं [54]। हाल के अध्ययनों से पता चला है कि वृक्क कार्सिनोमा कोशिकाओं [55] के विकास और अस्तित्व के लिए HDAC1 और HDAC2 आवश्यक हैं। HDACis ई-कैडरिन (कोशिका आसंजन अणु) और प्लेटलेट-व्युत्पन्न वृद्धि कारक रिसेप्टर (PDGFR, RCC मेटास्टेसिस गठन का एक प्रमुख चालक) की कमी का कारण बनता है [55]। क्लियर सेल रीनल सेल कार्सिनोमा (ccRCC) रीनल सेल कार्सिनोमा का सबसे आम रूप है। ccRCC को ट्यूमर सप्रेसर जीन वॉन हिप्पेल लिंडौ (VHL) [56] की निष्क्रियता की विशेषता है। अध्ययनों से पता चला है कि HDAC1 और 6 अत्यधिक व्यक्त हैं और ccRCC [56] में सेल आक्रमण और प्रवासन को नियंत्रित करते हैं। हाल ही में, हमने विल्म्स ट्यूमर में HDAC1 और HDAC2 की उच्च गतिविधि का भी पता लगाया, जो कि गुर्दे का एक ठोस कैंसरयुक्त ट्यूमर है जो अपरिपक्व बच्चे से उत्पन्न होता है।nआई सेल (लियू एट अल।, अप्रकाशित)। हिस्टोन और गैर-हिस्टोन प्रोटीन दोनों को लक्षित करके, एचडीएसी ठोस ट्यूमर [57] के विकास और प्रगति में महत्वपूर्ण भूमिका निभाते हैं। HDACi को कैंसर कोशिकाओं के विकास की गिरफ्तारी, एपोप्टोसिस और विभेदन को प्रभावी ढंग से प्रेरित करने और ट्यूमर एंजियोजेनेसिस के निषेध [57, 58] के लिए प्रदर्शित किया गया है।
संचित साक्ष्य से पता चला है कि HDACi कैंसर कोशिका प्रसार को रोकता है और कोशिका चक्र गिरफ्तारी को प्रेरित करता है [57, 58]। RCC कोशिकाओं के VPA उपचार से G1 को p21 [59] के अपग्रेडेशन द्वारा गिरफ्तार किया गया। इसके अलावा, LBH589 (panobinostat; Farydak®, Novartis Pharms Corp.) ने औरोरा A और B के ह्रास और सर्वाइविन [60] के डाउनरेगुलेशन द्वारा RCC कोशिकाओं की G2/M गिरफ्तारी को प्रेरित किया, जिसकी विशेष रूप से HDAC3 और 6 [60] के माध्यम से मध्यस्थता की गई थी। . ऑरोरा ए और बी अत्यधिक संरक्षित सेरीन / थ्रेओनीन किनेसेस हैं जो समसूत्रण और अर्धसूत्रीविभाजन के दौरान महत्वपूर्ण भूमिका निभाते हैं, विशेष रूप से जी 2-एम सेल चक्र प्रगति में। उत्तरजीवी एपोप्टोसिस (आईएपी) परिवार के अवरोधक का सदस्य है, जो एपोप्टोसिस या क्रमादेशित कोशिका मृत्यु को रोकने का कार्य करता है। G2/M गिरफ्तारी भी KBH-A145, एक-लैक्टम-आधारित हाइड्रोक्सैमिक एसिड डेरिवेटिव से प्रेरित है जो HDAC [61] को रोकता है। मानव वृक्क कैंसर कोशिकाओं में, KBH-A145 HDAC1 की p21 प्रमोटर [61] की भर्ती को रोककर p21 को अपग्रेड करता है। सामूहिक रूप से, इन निष्कर्षों से संकेत मिलता है कि HDAC अवरोधक कोशिका चक्र नियामकों, जैसे कि p21, औरोरा A, और औरोरा B को प्रभावित करके RCC में चक्र गिरफ्तारी का कारण बनते हैं।
कई कैंसर के इलाज के लिए एफडीए की मंजूरी के बावजूद, एचडीएसी इनहिबिटर (एचडीएसीसीआई) के एकल चिकित्सीय उपयोग में ठोस ट्यूमर [62] के खिलाफ सीमित चिकित्सीय प्रभाव है। कई अध्ययनों ने आरसीसी [58] के इलाज के लिए अन्य कैंसर एजेंटों के साथ एचडीएसी के संयुक्त उपयोग के लाभों का प्रदर्शन किया है। उदाहरण के लिए, कम खुराक वाले इंटरफेरॉन, या AEE788 (एक रिसेप्टर टाइरोसिन किनसे अवरोधक), या RAD001 (mTOR का एक अवरोधक) के संयोजन में VPA, RCC सेल [63] में HDAC गतिविधि और सेल प्रसार को रोकने में बहुत अधिक प्रभावी है। एकल-हाथ चरण I / II अध्ययन के परिणाम बताते हैं कि मेटास्टेटिक सीसीआरसीसी वाले रोगियों में उच्च खुराक आईएल -2 के लिए कक्षा 1 एचडीएसी अवरोधक एंटिनोस्टैट के अलावा उपचार फायदेमंद हो सकता है [64]। इसी समूह ने यह भी बताया कि द्वितीय श्रेणी के एचडीएसी अवरोधक वोरिनोस्टैट और वीईजीएफ़ अवरोधक बेवाकिज़ुमैब का पुनर्संयोजन एकल-हाथ चरण I / II नैदानिक परीक्षण [65] में अपेक्षाकृत अच्छी तरह से सहन किया जाता है।
सामूहिक रूप से, ये अध्ययन दृढ़ता से सुझाव देते हैं कि एचएडीसी निषेध, खासकर जब अतिरिक्त चिकित्सा एजेंटों के साथ मिलकर, आरसीसी के इलाज के लिए एक प्रभावी तरीका प्रदान कर सकता है।

निष्कर्ष और दृष्टिकोण
एचडीएसी, विशेष रूप से कक्षा I एचडीएसी, को इसमें महत्वपूर्ण भूमिका निभाने के लिए प्रदर्शित किया गया हैगुर्दाविकास [4, 23, 27, 9]। एचडीएसी की असामान्य अभिव्यक्ति स्तर और गतिविधि विभिन्न किडनी रोगों के रोगजनन और प्रगति के साथ निकटता से जुड़ी हुई है। कई HDACi को इलाज में बहुत प्रभावी दिखाया गया हैगुर्दाबीमारी। गुर्दे की बीमारी पर हिस्टोन डीएसेटाइलेज़ इनहिबिटर के चिकित्सीय प्रभाव पर व्यापक जानकारी एक समीक्षा पत्र (चुन, 2018) में प्रदान की गई थी। सामान्य रूप से HDACs के आणविक तंत्र को बेहतर ढंग से समझने के लिए और अधिक अध्ययन आवश्यक हैंगुर्दागठन और गुर्दे की बीमारियां। HDACs और HDACi प्रोटीन एसिटिलीकरण को बदलकर जीन अभिव्यक्ति को विनियमित (या परिवर्तित) करते हैं। वर्तमान में, एचडीएसी-मॉड्यूलेटेड या एचडीसीएआई-मध्यस्थता प्रोटीन एसिटिलेशन की प्रोफाइलगुर्दे(शारीरिक या रोग स्थितियों में) अच्छी तरह से ज्ञात नहीं है। एचडीएसी नॉकआउट या प्रोटिओमिक दृष्टिकोण का उपयोग करते हुए एचडीएसी निषेध के जवाब में वैश्विक प्रोटीन लाइसिन एसिटिलेशन का व्यापक विश्लेषण गुर्दे के विकास में एचडीएसी के विनियमन तंत्र में उपन्यास अंतर्दृष्टि प्रदान करेगा और गुर्दे की बीमारियों और संबंधित गुर्दे-हृदय की रोकथाम और उपचार के लिए नए चिकित्सीय रास्ते खोलेगा। बीमारी। कई अध्ययनों ने एचडीएसी इनहिबिटर के रीनोप्रोटेक्टिव प्रभाव को सफलतापूर्वक प्रदर्शित किया है, हालांकि, उनमें से ज्यादातर पैन-एचडीएसी इनहिबिटर हैं। ब्रॉड-स्पेक्ट्रम एचडीएसी निषेध से नेफ्रोटॉक्सिसिटी होने की अधिक संभावना है, और नैदानिक परिणामों में सुधार और विषाक्तता को कम करने के लिए विशिष्ट एचडीएसी अवरोधकों के विकास की आवश्यकता है। अतिरिक्त एजेंटों के साथ एचडीएसी इनहिबिटर को जोड़कर कॉम्बीनेटरियल थेरेपी भी उपचार के लिए लाभकारी होगी। इसके अलावा, एचडीएसी और एचडीएसी इनहिबिटर की भूमिकाओं की व्यापक समझ भी पुनर्योजी चिकित्सा में नेफ्रोजेनेसिस को पुनर्पूंजीकृत करने के लिए नए उपकरणों के विकास के लिए बहुत मददगार होगी।
पावती इस पांडुलिपि को गंभीर रूप से पढ़ने और संपादित करने के लिए डॉ एल-दहर को बहुत धन्यवाद। इस प्रकाशन में रिपोर्ट किए गए शोध को अमेरिकन हार्ट एसोसिएशन (17एसडीजी33660072), नेशनल इंस्टीट्यूट ऑफ हेल्थ ग्रांट्स पी50 डीके096373-03 और पी30जीएम103337 द्वारा समर्थित किया गया था।
ओपन एक्सेस यह लेख क्रिएटिव कॉमन्स एट्रिब्यूशन 4 के तहत लाइसेंस प्राप्त है। 0 अंतर्राष्ट्रीय लाइसेंस, जो किसी भी माध्यम या प्रारूप में उपयोग, साझाकरण, अनुकूलन, वितरण और पुनरुत्पादन की अनुमति देता है, जब तक आप मूल लेखक को उचित श्रेय देते हैं ( s) और स्रोत, Creative Commons लाइसेंस के लिए एक लिंक प्रदान करें, और इंगित करें कि क्या परिवर्तन किए गए थे। इस लेख की छवियां या अन्य तृतीय-पक्ष सामग्री लेख के क्रिएटिव कॉमन्स लाइसेंस में शामिल हैं, जब तक कि सामग्री के लिए क्रेडिट लाइन में अन्यथा इंगित न किया गया हो। यदि सामग्री को लेख के क्रिएटिव कॉमन्स लाइसेंस में शामिल नहीं किया गया है और वैधानिक विनियमन द्वारा आपके इच्छित उपयोग की अनुमति नहीं है या अनुमत उपयोग से अधिक है, तो आपको सीधे कॉपीराइट धारक से अनुमति प्राप्त करने की आवश्यकता होगी। इस लाइसेंस की एक प्रति देखने के लिए, http://creativecommons.org/licenses/by/4 पर जाएं।0/।
