गुर्दे की बीमारियों का उपचार: मेसेनकाइमल स्टेम सेल और एक्स्ट्रासेलुलर वेसिकल्स
Mar 23, 2022
संपर्क करना:joanna.jia@wecistanche.com/ व्हाट्सएप: 008618081934791
भाग : गुर्दे की बीमारियों के खिलाफ चिकित्सा में मेसेनकाइमल स्टेम सेल और बाह्य कोशिकीय पुटिका
यूलिंग हुआंग और लीना यांगो
सार
गुर्दे के रोगउनकी बढ़ती घटनाओं और मृत्यु दर के कारण मानव स्वास्थ्य के लिए खतरा पैदा करते हैं। प्रीक्लिनिकल और क्लिनिकल अध्ययनों में यह स्वीकार किया गया है किमेसेनचिमल स्टेम सेल(MSCs) गुर्दे की बीमारियों के इलाज के लिए प्रभावी और सुरक्षित हैं। एमएससी (मेसेनचिमल स्टेम सेल) मुख्य रूप से पोषी कारकों को स्रावित करके और वितरित करके अपनी भूमिका निभाते हैंबाह्य पुटिका(ईवीएस)। MSC-व्युत्पन्न EVs में निहित आनुवंशिक सामग्री और प्रोटीन (बाह्य पुटिका) (एमएससी-ईवी), सेलुलर संचार के एक महत्वपूर्ण साधन के रूप में, गुर्दे की बीमारियों के लक्षित उपचार के लिए एक शोध केंद्र बन गया है। वर्तमान में, MSC-EVs(बाह्य पुटिका)तीव्र गुर्दे की चोट (AKI), क्रोनिक किडनी रोग (CKD), मधुमेह अपवृक्कता (DN), और एथेरोस्क्लोरोटिक नवीकरणीय रोग (ARVD) पर स्पष्ट चिकित्सीय प्रभाव दिखाया है; हालांकि, प्रतिरोपित किडनी में उनकी भूमिका विवादास्पद बनी हुई है। यह समीक्षा उन तंत्रों को सारांशित करती है जिनके द्वारा MSC-EVs(बाह्य पुटिका)जानवरों के मॉडल में इन बीमारियों का इलाज करें और कुछ समस्याओं का प्रस्ताव करें, जिससे भविष्य के नैदानिक अभ्यास की सुविधा की उम्मीद की जा सके।
कीवर्ड: किडनी रोग, मेसेनकाइमल स्टेम सेल, एक्स्ट्रासेलुलर वेसिकल्स

भाग के लिए यहां क्लिक करें
एमएससी-ईवी और किडनी रोग
एमएससी-ईवीएस(बाह्य पुटिका)और एक्ली
गंभीर रूप से बीमार रोगियों में एकेआई प्रचलित है, यहां तक कि उन एकेआई रोगियों की मृत्यु भी जो गहन देखभाल इकाइयों में नहीं हैं, 10-20 प्रतिशत [45] जितनी अधिक हैं। AKI के लिए अभी भी विशिष्ट और प्रभावी उपचारों की कमी है, जबकि स्टेम सेल प्रत्यारोपण आशाजनक है। कई प्रयोगों ने MSCs के लाभों की पुष्टि की है(मेसेनचिमल स्टेम सेल)AKI के उपचार में, और MSCs के प्रभाव को बढ़ाने के कई तरीके(मेसेनचिमल स्टेम सेल)हाल के वर्षों में सामने आए हैं। उदाहरण के लिए, I-17A को COX के माध्यम से Treg का प्रतिशत बढ़ाने में सक्षम पाया गया है-2/PGE2 पथ-मार्ग और MSCs के इम्युनोसुप्रेशन फ़ंक्शन का अनुकरण करता है(मेसेनचिमल स्टेम सेल)[46]; MSCs कोटिंग करके(मेसेनचिमल स्टेम सेल)गुर्दे की चोट के अणु के खिलाफ निर्देशित एंटीबॉडी के साथ-1, MSCs की अवधारण(मेसेनचिमल स्टेम सेल)इस्केमिक गुर्दे में लंबे समय तक [47]; सिस्प्लैटिन-प्रेरित AKI, MSCs के माउस मॉडल में(मेसेनचिमल स्टेम सेल)एक न्यूनतम इनवेसिव तकनीक का उपयोग करके सीधे महाधमनी में इंजेक्ट किया जाता है, जो MSCs के उपयोग की प्रभावी दर में सुधार करता है(मेसेनचिमल स्टेम सेल) [48].
जैसे-जैसे शोध आगे बढ़ता है, सबूत बताते हैं कि MSC-EVs(बाह्य पुटिका)AKI के इलाज में एक प्रमुख भूमिका निभाते हैं। एमएससी-ईवीएस(बाह्य पुटिका)ऑक्सीकरण, एपोप्टोसिस, और सूजन को रोककर और एंजियोजेनेसिस, सेल चक्र, पुनर्जनन, ऑटोफैगी और प्रसार [49-54](छवि 2) को विनियमित करके AKI को राहत दे सकता है। हालांकि, विभिन्न रोगजनकों वाले AK के लिए, MSC.EVs से स्थानांतरित सिग्नल पदार्थ(बाह्य पुटिका)लक्ष्य कोशिकाओं के लिए अपनी अनूठी विशेषताओं का प्रदर्शन करते हैं। AKI के मुख्य रोगजनकों में दवाओं की गुर्दे की विषाक्तता, प्रत्यारोपण के कारण होने वाली इस्केमिक-रीपरफ्यूजन चोट (IRI) और सेप्सिस शामिल हैं। इसके अनुरूप, प्रायोगिक AKI मॉडल मुख्य रूप से सिस्प्लैटिन, जेंटामाइसिन, पैराक्वाट, इस्किमिया-रीपरफ्यूजन (I/R) द्वारा एकतरफा या द्विपक्षीय वृक्क धमनियों को रोके जाने और कोकल लिगेशन और पंचर (CLP) के कारण होने वाले सेप्सिस से प्रेरित होते हैं। इस समीक्षा में विभिन्न AKI मॉडल में MSC-EVs के तंत्र को तालिका 1 में संक्षेपित किया गया है।

अमेज़नमेंगुर्दा
आई/आर-प्रेरित गुर्दे की चोट
I/R AK का सामान्य रोगजनन है। पशु परीक्षणों में, I/R मॉडल आम तौर पर एकतरफा या द्विपक्षीय गुर्दे की धमनियों और नसों को बंद करके और फिर ऑक्सीजन की आपूर्ति प्रदान करके स्थापित किए जाते हैं। पिछले शोध ने संकेत दिया कि huMSC-EVs(बाह्य पुटिका)हाइपोक्सिया-इंड्यूसीबल कारक -1 [49] से प्रेरित एंजियोजेनेसिस को बढ़ावा देने के प्रभाव से स्वतंत्र चूहों में गुर्दे की आईआरआई को कम कर सकता है। एमएससी-ईवीएस(बाह्य पुटिका)AKI को राहत देने के लिए विभिन्न मार्गों के माध्यम से I/R मॉडल में मैक्रोफेज को भी रोक सकता है। Zou et al द्वारा किए गए प्रयोगों में, मानव व्हार्टन की जेली MSCs से प्राप्त MVs(मेसेनचिमल स्टेम सेल)(hWJMSCs) miR-15a/15b/16 द्वारा रीनल केमोकाइन CX3CL1 की अभिव्यक्ति को दबाते हैं और CD68 प्लस मैक्रोफेज की संख्या को कम करते हैं [55]। शेन एट अल। पाया गया कि BMMSC-Exos पर व्यक्त CC केमोकाइन रिसेप्टर -2 मैक्रोफेज के लिए CCL2 की भर्ती और सक्रियण को रोकता है, जो lig-और CL2 [56] को बांधने के लिए एक प्रलोभन के रूप में कार्य करता है।
एपोप्टोसिस आईआरआई से निकटता से संबंधित है। गु एट अल। सत्यापित, विवो और इन विट्रो प्रयोगों के माध्यम से, कि ईवीएस(बाह्य पुटिका)hWJMSCs . से व्युत्पन्न(मेसेनचिमल स्टेम सेल)(एचडब्ल्यूजेएमएससी-ईवीएस(बाह्य पुटिका)) miR-30 [57] का उपयोग करके माइटोकॉन्ड्रिया विखंडन को रोककर रीनल ट्यूबलर एपिथेलियल कोशिकाओं (TECs) के एपोप्टोसिस को कम करता है। इसके अलावा, ली एट अल। ने कहा कि MSC-Exo ने भड़काऊ कारकों (IL -6, TNF-, NF-kappa B, और IFN-y) और एपोप्टोसिस-संबंधित कारकों (caspase -9) की अभिव्यक्तियों को रोककर IRI की प्रगति को धीमा कर दिया। cleaved caspase-3, Bax, और Bcl-2)[50]।
आई/आर को कम करने के लिए एंटीऑक्सीडेशन एक प्रभावी उपाय है। झांग एट अल। पता चला कि hWJMSC-EVs(बाह्य पुटिका)परमाणु कारक-एरिथ्रोइड 2-संबंधित कारक Nrf2/ARE [57] को सक्रिय करके उनके एंटी-ऑक्सीडेटिव प्रभाव को निभाते हैं। इसके बाद, काओ एट अल द्वारा प्रयोग। प्रदर्शित किया कि BMMSC-EVs(बाह्य पुटिका)टीईसी में miRNA-200a-3p स्थानांतरित करके Keapl-Nrf2 सिग्नलिंग मार्ग को सक्रिय करें, इस प्रकार माइटोकॉन्ड्रिया को एक एंटीऑक्सीडेंट भूमिका निभाने के लिए संशोधित करें [51]।
दवाओं से प्रेरित AKI के मॉडल आमतौर पर सिस्प्लैटिन को शामिल करके स्थापित किए जाते हैं। सिस्प्लैटिन-प्रेरित एकेआई मॉडल, ब्रूनो एट अल का उपयोग करना। पाया गया कि बीएमएमएससी-एमवी टीईसी में एपोप्टोटिक रोधी जीन (बीसीएल-एक्सएल, बीसीएल2 और बीआईआरसी8) की अभिव्यक्तियों को प्रेरित करके और प्रो-एपोप्टोटिक जीन (कैस्पल, कैस्प8, और एलटीए) की अभिव्यक्ति को रोककर गुर्दे की रक्षा करते हैं।[58] झोउ एट अल। ने निष्कर्ष निकाला कि huMSC-Exos विवो और इन विट्रो में नेफ्रोसाइट्स के प्रसार को प्रोत्साहित कर सकता है और फॉस्फोराइलेशन और एक्स्ट्रासेलुलर रेगुलेटेड किनसे (ERK) 1/2 पाथवे [52] के सक्रियण को प्रेरित कर सकता है। डी अल्मेडा एट अल। घायल कोशिकाओं और विशिष्ट miRNA-mRNA नेटवर्क को विनियमित करने में ADMSC-MVs के कार्य पर प्रकाश डाला। उदाहरण के लिए, miR-141 ऑटोफैगी को विनियमित करने के लिए Uk2 को लक्षित करता है, और miR-377 सेल चक्र को संशोधित करने के लिए Cull को लक्षित करता है [53]। वांग एट अल। ने पाया कि एचयूएमएससी-एक्सो प्री-प्रोसेसिंग ऑटोफैगी [59] को सक्रिय करके विवो और इन विट्रो में सिस्प्लैटिन-प्रेरित गुर्दे की विषाक्तता को रोक सकता है। जिया एट अल। दो अध्ययन किए और 14-3-3 को huMSC-Exos द्वारा सक्रिय ऑटोफैगी के एक नए तंत्र के रूप में पहचाना: 14-3-3 ATG16L पर कार्य करता है, जो ऑटोफैगी को सक्रिय करता है और इसलिए सिस्प्लैटिन-प्रेरित AKI [60, 61] को रोकता है। उल्लाह एट अल। हाल ही में प्रस्तावित है कि BMMSC-EVs(बाह्य पुटिका)और स्पंदित केंद्रित अल्ट्रासाउंड दोनों hsp को रोककर सिस्प्लैटिन-प्रेरित कोशिका की चोट को कम करते हैं 70- मध्यस्थता NLRP3 इन्फ्लामासोम [62]।
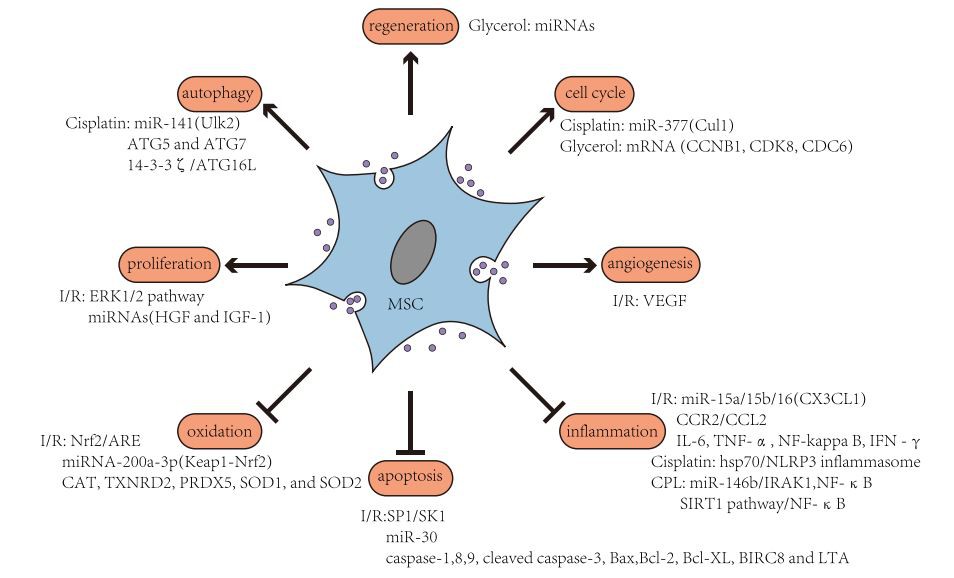
अंजीर। 2 MSC-EVs के कार्यात्मक मार्ग(बाह्य पुटिका)विभिन्न AKI मॉडल में।एमएससी-ईवीएस(बाह्य पुटिका)ऑक्सीकरण, एपोप्टोसिस, और सूजन को रोककर और एंजियोजेनेसिस, सेल चक्र, पुनर्जनन, ऑटोफैगी और प्रसार को विनियमित करके AKI को राहत दे सकता है। प्रोग्राम(मेसेनचिमल स्टेम सेल), मेसेनचिमल स्टेम सेल; ईवीएस, बाह्य पुटिका; एकेआई, तीव्र गुर्दे की चोट; आई/आर, इस्किमिया-रीपरफ्यूजन; सीएलपी, दुम बंधाव, और पंचर सिस्प्लैटिन-प्रेरित एकेआई मॉडल
ग्लिसरीनम द्वारा प्रेरित मायोलिसिस के कारण एकेआई मॉडल
हाल के वर्षों में, ग्लिसरीनम द्वारा प्रेरित मायोलिसिस के कारण एकेआई मॉडल पर भी बहुत ध्यान दिया गया है। ऐसे मॉडल में, ब्रूनो एट अल। पाया कि बीएमएमएससी-ईवीएस(बाह्य पुटिका)(मुख्य रूप से एक्सोस) विशिष्ट mRNA (CCNB1, CDK8, और CDC6) में समृद्ध होते हैं, जो सेल चक्रों की शुरुआत और प्रगति को प्रभावित करते हैं। समृद्ध miRNAs वृद्धि कारकों (HGF और IGF -1) द्वारा प्रसार को बढ़ावा देते हैं और इसलिए AKI [63] को राहत देते हैं। बायोइंजीनियरिंग के माध्यम से, टप्पारो एट अल। इन-क्रीस्ड विशिष्ट miRNAs(hsa-miR-10a-5p, hsa-miR-29a-3p, hsa-miR-127-3p, और hsa -एमआईआर-486-5पी)बीएमएमएससी-ईवीएस में(बाह्य पुटिका)इसके पुनर्योजी प्रभाव का अनुकरण करने और ग्लिसरीनम द्वारा प्रेरित गुर्दे की चोट को कम करने के लिए [54]।
सीएलपी
सीएलपी द्वारा तैयार किया गया एकेआई मॉडल गंभीर रूप से बीमार रोगियों के सेप्सिस से संबंधित एके का अनुकरण करता है। सेप्सिस के साथ चूहों में, झांग एट अल। पता चला कि huMSC-Exos इंटरल्यूकिन -1 रिसेप्टर से जुड़े किनसे अभिव्यक्ति [64] को डाउनग्रेड करते हुए miR -146 b स्तर को बढ़ाकर NF-KkB गतिविधि को रोकता है। इसी तरह, गाओ एट अल। ने कहा कि ADMSC-Exo SIRT1 सिग्नलिंग मार्ग के माध्यम से NF-KB को विनियमित कर सकता है, इस प्रकार सेप्सिस से संबंधित AKI [65] की सूजन को रोकता है।
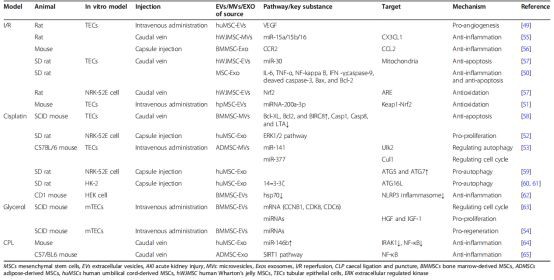
तालिका 1 एमएससी-ईवीएस के कार्यात्मक मार्ग(बाह्य पुटिका)विभिन्न एकेआई मॉडल में
एमएससी-ईवीएस(बाह्य पुटिका)और सीकेडी
यह साबित करने वाले नए सबूत हैं कि, कई मामलों में, एकेआई सीकेडी में विकसित हो सकता है [66]। एकेआई विकसित करने के बाद, अंतिम चरण के गुर्दे की बीमारियों और सीकेडी के अनुबंध के अतिरिक्त जोखिमों का अनुमान लगाया गया था कि क्रमशः प्रत्येक 100 एकेआई रोगियों में 0.4 और 10 मामलों में सालाना वृद्धि हुई है, [67]। सीकेडी को वृक्क पैरेन्काइमा के प्रगतिशील अपरिवर्तनीय फाइब्रोसिस की विशेषता है। कई बीमारियां सीकेडी में विकसित हो सकती हैं, जिनमें एकेआई, मधुमेह, एथेरोस्क्लेरोसिस और नेफ्रोटिक सिंड्रोम शामिल हैं। MSCs के साथ CKD के उपचार के संबंध में कई साक्ष्य प्राप्त हुए हैं(मेसेनचिमल स्टेम सेल)पूर्व और बाद के नैदानिक परीक्षणों में। हाल के शोध में यह पाया गया है कि मेलाटोनिन प्रीकंडीशनिंग MSCs की उपचार क्षमता को बढ़ाता है(मेसेनचिमल स्टेम सेल)ऑटोलॉगस और एलोजेनिक प्रत्यारोपण [68,69] में। एक नैदानिक परीक्षण में जिसमें सीकेडी के सात पात्र रोगियों का 18-महीना अनुवर्ती कार्रवाई शामिल है, एकल-खुराक ऑटोलॉगस एमएससी(मेसेनचिमल स्टेम सेल)सीकेडी रोगियों [70] में सुरक्षित और सहनीय साबित हुए हैं। फिर से खोजकर्ताओं ने पाया कि huMSCs का वातानुकूलित माध्यम प्रोलिफरेशन और एंटी-एपोप्टोसिस [71] द्वारा एकतरफा मूत्रवाहिनी रुकावट (UUO) से प्रेरित फाइब्रोसिस से राहत देता है। आज तक, कई प्रीक्लिनिकल अध्ययनों ने साबित किया है कि MSC-EVs(बाह्य पुटिका)सीकेडी के इलाज में प्रभावी हैं।
साइक्लोस्पोरिन के कारण क्रोनिक रीनल टॉक्सिसिटी के माउस मॉडल में, ईवीएस का वातानुकूलित माध्यम समाप्त हो गया(बाह्य पुटिका), एमएससी-ईवीएस(बाह्य पुटिका), और ईवीएस(बाह्य पुटिका)गुर्दे की बीमारियों के पूर्वानुमान में सुधार कर सकता है [72]। एरिस्टोलोचिक एसिड नेफ्रोपैथी मॉडल में, MSC-EVs(बाह्य पुटिका)-SMA, TGF 1, और कॉलर [73] जैसे प्रो-फाइब्रोजेनिक जीन की अभिव्यक्तियों को काफी कम करते हैं। UUO मॉडल में, वांग एट अल। ने पाया कि BMMSC-Exos miRNA के साथ TGF - 1 को रोककर रीनल इंटरस्टिशियल फाइब्रोसिस को कम करता है। -लेट7सी [74]। हाल ही में, कुछ शोधकर्ताओं ने पाया (माउस मॉडल में) कि huMSC-Exos ROS-मध्यस्थता P38MAPK/ERK मार्ग [75] को दबाकर गुर्दे के बीचवाला फाइब्रोसिस से राहत देता है। चेन एट अल। ने प्रस्तावित किया कि ग्लियाल-व्युत्पन्न न्यूरोट्रॉफिक कारक-संशोधित ADMSC-Exos SIRT1 / eNOS मार्ग [76] को सक्रिय करके ट्यूबलोइंटरस्टिशियल फाइब्रोसिस में पेरिवास्कुलर केशिकाओं को उत्तेजित करता है। इसके अलावा, पिछले शोध ने यह भी सुझाव दिया कि ADMSC-Exos TECs के प्रतिलेखन कारक Sox9 की अभिव्यक्ति को बढ़ाता है, और Sox9 प्लस कोशिकाओं की संतान फाइब्रोटिक परिवर्तन के बजाय वृक्क नलिकाओं के पुनर्जनन की सुविधा प्रदान करती है, इस प्रकार AKI-CKD संक्रमण को धीमा कर देती है [17,77 ].

Maca ginseng cistanche गुर्दे में
एमएससी-ईवीएस(बाह्य पुटिका)और डीएन
डीएन ईएसआरडी के लिए मुख्य रोगजनन है। ऐसी कई जाँचें हैं जिनसे पता चलता है कि MSC प्रत्यारोपण DN की प्रगति को धीमा कर सकता है। एक यादृच्छिक नियंत्रित परीक्षण ने बताया कि टाइप 2 मधुमेह [78] के विषयों में मेसेनकाइमल अग्रदूत कोशिकाओं का उपयोग करना सुरक्षित और व्यवहार्य है; हालांकि, एलोजेनिक प्रत्यारोपण में प्रतिरक्षा अस्वीकृति समस्याएं हैं और हाइपरग्लाइकेमिया से ऑटोलॉगस एमएससी को प्रेरित क्षति है।(मेसेनचिमल स्टेम सेल). इन समस्याओं को हल करने के लिए, नागिशी एट अल। मधुमेह से व्युत्पन्न BMMSCs की आकारिकी, प्रसार क्षमता और सेलुलर जुटाने की क्षमता में सुधार के लिए व्हार्टन के जेली एक्सट्रैक्ट सुपरनैटेंट का अभिनव रूप से उपयोग किया जाता है, जो प्रभावी ऑटोलॉगस प्रत्यारोपण [79] को सक्षम बनाता है। हाल ही में, कुछ शोधकर्ताओं ने MSCs को सह-संस्कृति करने का भी प्रयास किया(मेसेनचिमल स्टेम सेल)पेरिटोनियल मैक्रोफेज के साथ [80] और MSCs को संशोधित करने के लिए(मेसेनचिमल स्टेम सेल)MSCs की उपचार क्षमता में सुधार करने के लिए एंजियोटेंसिन-परिवर्तित एंजाइम 2 [81] के साथ(मेसेनचिमल स्टेम सेल)डीएन के लिए
एमएससी-ईवीएस का तंत्र(बाह्य पुटिका), डीएन के उपचार के लिए एक नए साधन के रूप में, निरंतर अन्वेषण के अधीन है। गैलो एट अल। पाया गया कि MSC/ह्यूमन लीवर स्टेम सेल (HLSC)-EVs(बाह्य पुटिका)miR-222 [82] के हस्तांतरण के माध्यम से मेसेंजियल कोशिकाओं को हाइपरग्लेसेमिया से होने वाले नुकसान से बचा सकता है। इसके अलावा, हाइपरग्लेसेमिया सीधे पॉडोसाइट्स की चोट को प्रेरित कर सकता है। पॉडोसाइट्स के पैथोलॉजिकल परिवर्तन डीएन की प्रगति से निकटता से संबंधित हैं। एमएससी-ईवीएस(बाह्य पुटिका)एंटी-एपोप्टोसिस, एंटी-फाइब्रोसिस और प्रो-ऑटोफैजिक प्रभावों सहित विभिन्न तरीकों से पोडोसाइट्स और अन्य गुर्दे की कोशिकाओं की रक्षा करने में सक्षम हैं, इस प्रकार डीएन (छवि 3) का इलाज करते हैं। डुआन एट अल। पता चला है कि मानव मूत्र-व्युत्पन्न स्टेम कोशिकाओं के वातानुकूलित माध्यम से पृथक एक्सो वीईजीए की अभिव्यक्ति और एमआईआरएनए -16-5 पी द्वारा पॉडोसाइट्स के एपोप्टोसिस को रोकता है, जिससे डीएन [83] से राहत मिलती है। यह डुआन एट अल द्वारा सिद्ध किया गया है। ADSC-EV miRNA-26a-5p TLR4 और NF-KB/VEGFA सिग्नलिंग मार्ग को डाउनरेगुलेट करके चूहों में पॉडोसाइट्स के हाइपरग्लेसेमिया-प्रेरित एपोप्टोसिस को दबा देता है [84] . एंटी-फाइब्रोसिस भी MSC-EVs के साथ DN उपचार में लागू किया जाने वाला एक प्रमुख तंत्र है(बाह्य पुटिका). झोंग एट अल। ने बताया कि MSC-MVs विवो में और इन विट्रो में miRNA-45la के माध्यम से सेल चक्र अवरोधकों P15 और P19 को दबाने में सक्षम हैं, सेल चक्र को फिर से शुरू करते हैं और इस प्रकार EMT और इंटरस्टीशियल फाइब्रोसिस [85] को उलटते हैं। ग्रेंज एट अल। माना कि ईवीएस(बाह्य पुटिका)HLSCs और MSCs . की(मेसेनचिमल स्टेम सेल)डीएन माउस मॉडल में ग्लोमेरुलर और ट्यूबल-इंटरस्टिशियल फाइब्रोसिस की प्रगति को रोक और उलट सकता है, फाइब्रोसिस से संबंधित जीन सर्पियाला, एफएएस लिगैंड, सीसीएल 3, टीआईएमपी 1, एमएमपी 3, टाइप I कोलेजन और स्नेल [86] को डाउनग्रेड कर सकता है। जिन एट अल। सत्यापित किया गया कि ADMS C-Exo, miRNA-215-5p [87] द्वारा ZEB2 के आनुवंशिक प्रतिलेखन को दबाकर पोडोसाइट्स के EMT को कमजोर करता है। ऑटोफैगी को हाल ही में डीएन में देरी के लिए एक तंत्र के रूप में भी माना गया है। इब्राहिम एट अल ने पुष्टि की कि एमएससी-एक्सोस ऑटोफैगी को बढ़ाता है और फिर एमटीओआर सिग्नलिंग मार्ग [88] के माध्यम से डीएन की प्रगति को धीमा कर देता है। जिन एट अल। आगे दिखाया कि ADMSC-Exo miRNA -486 द्वारा Smadl/mTOR सिग्नलिंग मार्ग को बाधित कर सकता है, जो ऑटोफैगी को बढ़ावा देता है और पॉडोसाइट्स में एपोप्टोसिस को रोकता है, इस प्रकार DN [89] के लक्षणों को कम करता है। उपरोक्त परीक्षणों का विवरण तालिका 2 में संक्षेपित किया गया है।
एमएससी-ईवीएस(बाह्य पुटिका)और एथेरोस्क्लोरोटिक नवीकरणीय रोग
एथेरोस्क्लेरोसिस गुर्दे की धमनी स्टेनोसिस का प्राथमिक कारण है। एथेरोस्क्लोरोटिक रेनोवैस्कुलर डिजीज (एआरवीडी) क्रोनिक रीनल इस्किमिया को प्रेरित कर सकता है और आगे फाइब्रोसिस को जन्म दे सकता है, जो ईएसआरडी विकसित करता है। एआरवीडी के इलाज के लिए पर्क्यूटेनियस ट्रांसल्यूमिनल रीनल एंजियोप्लास्टी एक सामान्य सर्जरी है; हालांकि, एट्रोफिक किडनी के कार्यों को बहाल करना मुश्किल है। पशु प्रयोगों ने पुष्टि की है कि MSCs . का संयोजन(मेसेनचिमल स्टेम सेल)एथेरोस्क्लोरोटिक रीनल आर्टरी स्टेनोसिस के इलाज के लिए एआरवीडी के साथ गुर्दे के कार्यों को बहाल करने में मदद करता है [90]। इसके बाद, कई नैदानिक परीक्षणों ने ऑटोलॉगस ADMSCs को संक्रमित करने की सुरक्षा को प्रदर्शित किया है(मेसेनचिमल स्टेम सेल)एआरवीडी के उपचार में [91-93]। इसके बाद, एडीएमएससी-ईवीएस(बाह्य पुटिका)हाल के शोध का केंद्र भी बन गया है। एकतरफा नवीकरणीय रोग जटिल चयापचय सिंड्रोम (मेट्स) के मॉडल में, एरिन एट अल। साबित कर दिया कि ऑटोलॉगस ADMSC-EVs(बाह्य पुटिका)चयापचय वृक्क संवहनी रोगों के साथ सूअरों में वृक्क सूक्ष्म संवहनी प्रणाली में सुधार [94]। इसके अलावा, शिमोनी एट अल। आगे MSC-EVs . में miRNA की पहचान की(बाह्य पुटिका)एआरवीडी के लिए एक महत्वपूर्ण लक्ष्य के रूप में [95]। इसके अलावा, एमएससी-ईवीएस(बाह्य पुटिका)टीजीएफ द्वारा टीजीएफ के लाभों को बढ़ाने के लिए भी पाए गए थे और इसलिए मेट्स प्लस आरएएस मॉडल [96] में गुर्दे की धमनी स्टेनोसिस के साथ गुर्दे के कार्यों में सुधार करते हैं। ऑटोलॉगस ADMSC-EVs(बाह्य पुटिका)आईएल-10 के माध्यम से मैक्रोफेज के फेनोटाइप को एम1 से एम2 में बदलने को भी प्रेरित कर सकता है, ताकि रीनल आर्टरी स्टेनोसिस [97] से राहत मिल सके।
उसी समय, कुछ शोधकर्ताओं ने प्रस्तावित किया कि MSC-Exos केवल गुर्दे की धमनी स्टेनोसिस [98] से प्रेरित उम्र बढ़ने वाले गुर्दे को आंशिक रूप से राहत दे सकता है। मेट्स ईवीएस पर miRNA की लोडिंग की मात्रा को बदलने में सक्षम हैं(बाह्य पुटिका), ईवीएस में उम्र बढ़ने से संबंधित miRNA को अपग्रेड करें(बाह्य पुटिका), और यहां तक कि ईवीएस के उपयोग को सीमित करें(बाह्य पुटिका)असामान्य प्रतिलेखन [99-101] के माध्यम से बहिर्जात पुनर्योजी चिकित्सा में। झाओ एट अल। पाया कि ऑटोलॉगस ADMSCs(मेसेनचिमल स्टेम सेल)तुलनात्मक अध्ययन के माध्यम से सूक्ष्म परिसंचरण को बेहतर ढंग से संरक्षित कर सकते हैं, जबकि ADMSC-EVs(बाह्य पुटिका)नेफ्रोसाइट्स की अक्षुण्णता बनाए रखने और नेक्रोसिस को कम करने में बेहतर प्रदर्शन करते हैं [102]। संक्षेप में, MSC-EVs का अनुप्रयोग मूल्य(बाह्य पुटिका)एआरवीडी के उपचार में विवाद बना हुआ है, और उनकी प्रभावकारिता को प्रकट करने के लिए आगे के शोध की आवश्यकता है।
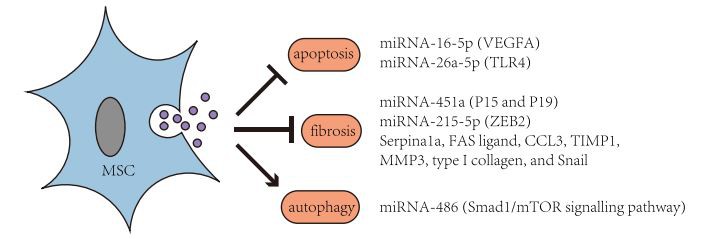
अंजीर। 3 MSC-EVs के कार्यात्मक मार्ग(बाह्य पुटिका)डीएन में।एमएससी-ईवीएस(बाह्य पुटिका)पोडोसाइट्स और अन्य कोशिकाओं को विभिन्न तरीकों से बचाने में सक्षम हैं, जिसमें एंटी-एपोप्टोसिस, एंटी-फाइब्रोसिस और प्रो-ऑटोफैजिक प्रभाव शामिल हैं, इस प्रकार डीएन का इलाज करते हैं। प्रोग्राम(मेसेनचिमल स्टेम सेल), मेसेनचिमल स्टेम सेल; ईवीएस(बाह्य पुटिका), बाह्य कोशिकीय पुटिका; डीएन, मधुमेह अपवृक्कता
एमएससी-ईवीएस(बाह्य पुटिका)और गुर्दा प्रत्यारोपण
अंतिम चरण के गुर्दे की विफलता के रोगियों के लिए गुर्दा प्रत्यारोपण पसंदीदा उपचार पद्धति है। दाता अंगों की कमी और प्रत्यारोपण का आधा जीवन चिकित्सा को सीमित करता है [4]। इसके अलावा, इस्किमिया-प्रेरित एकेआई को किडनी प्रत्यारोपण में व्यापक रूप से देखा जाता है, क्योंकि इस्किमिया के विकास के लिए उपलब्ध समय के कारण दाता से किडनी के रीनल इस्किमिया-रीपरफ्यूजन में रिसेप्टर्स में देरी के बीच देरी होती है [103]।
यह भी प्रत्यारोपण के विलंबित कार्यों का एक प्रमुख कारण है। इन समस्याओं को हल करने के लिए, स्थिर कोल्ड स्टोरेज, हाइपोथर्मिक मशीन परफ्यूज़न (HMP), और इस्किमिया और रीपरफ्यूज़न को लक्षित करने वाले कई नए ड्रग उम्मीदवारों का अध्ययन किया जा रहा है [104]। डेल रियो एट अल का काम। सत्यापित किया गया है कि स्थिर कोल्ड स्टोरेज [105] के लिए एचएमपी और नॉर्मोथर्मिक क्षेत्रीय छिड़काव बेहतर हैं। इसके अलावा, शोधकर्ता वर्तमान तकनीकों के पूरक के लिए अन्य प्रभावी तरीके खोजने के लिए समर्पित हैं।
ऑटोलॉगस MSCs प्राप्त करने वाले 105 चीनी गुर्दा प्रत्यारोपण विषयों को शामिल करने वाला एक परीक्षण(मेसेनचिमल स्टेम सेल)प्रतिरोपित गुर्दे के पुनर्संयोजन से पता चलता है कि MSCs का उपयोग करना संभव और सुरक्षित है(मेसेनचिमल स्टेम सेल)गुर्दा प्रत्यारोपण में [106]; हालांकि, हाल ही में एक अन्य शोध दल द्वारा किए गए एक समान परीक्षण में पाया गया कि गुर्दे के प्रत्यारोपण, संक्रामक जटिलताओं, गुर्दा कार्यों, अस्वीकृति आवृत्ति, और जीवित रहने के समय की पोस्ट-ऑपरेटिव जटिलताओं में नियंत्रण के साथ सांख्यिकीय अंतर नहीं दिखता है 1- वर्ष अनुवर्ती [107]। इसलिए, MSC-EVs का सुरक्षात्मक प्रभाव(बाह्य पुटिका)प्रतिरोपित किडनी में विवाद का विषय बना हुआ है। ग्रेगोरिनी और अन्य ने साबित किया कि MSCs जोड़ना(मेसेनचिमल स्टेम सेल)/ईवीएस(बाह्य पुटिका)एचएमपी अवधि में बेल्ज़र समाधान सेल व्यवहार्यता के लिए आवश्यक एंजाइमी तंत्र को संरक्षित करके गुर्दे को इस्केमिक चोट से बचा सकता है [108]। कोच एट अल द्वारा किए गए प्रयोगों से संकेत मिलता है कि एमएससी-ईवीएस(बाह्य पुटिका)कुछ हद तक एलोजेनिक गुर्दा प्रत्यारोपण के प्रतिरक्षण को नियंत्रित करता है [109]। इससे महत्वपूर्ण रूप से अलग, हेटेरोटोपिक किडनी ट्रांस-प्लांटेशन के एक चूहे के मॉडल की स्थापना करके, जोस रामिरेज़-बाजो एट अल। पाया कि ऑटोलॉगस MSCs(मेसेनचिमल स्टेम सेल)गुर्दे की अस्वीकृति के चूहे के मॉडल में प्रत्यारोपण और विषयों के जीवित रहने के समय को लम्बा खींचना, जबकि ईवीएस(बाह्य पुटिका)नहीं [110]। इस विषय का शायद ही कभी अध्ययन किया जाता है, और निष्कर्ष निकालने से पहले और अधिक शोध की आवश्यकता होती है।
तालिका 2 एमएससी-ईवीएस के कार्यात्मक मार्ग(बाह्य पुटिका)डीएन मॉडल में

समस्याएं और संभावनाएं
पिछले शोध में, MSCs(मेसेनचिमल स्टेम सेल)गुर्दे की विभिन्न बीमारियों के इलाज में सकारात्मक भूमिका निभाते पाए गए हैं। उदाहरण के लिए, MSC-CM M2 मैक्रोफेज-मध्यस्थता विरोधी भड़काऊ कार्रवाई [111] के आधार पर प्रायोगिक एंटी-ग्लोमेरुलर बेसमेंट मेम्ब्रेन ग्लोमेरुलोनेफ्राइटिस से राहत देता है। प्रणालीगत ल्यूपस एरिथेमेटोसस (एसएलई) में, एलोजेनिक एमएससी प्रत्यारोपण गुर्दे की चोट को कम करता है [112]। नैदानिक परीक्षणों से यह भी पता चलता है कि एलोजेनिक MSCs के साथ SLE रोगियों का इलाज करना सुरक्षित और व्यवहार्य दोनों है(मेसेनचिमल स्टेम सेल)स्वस्थ दाताओं से [113]। एड्रियामाइसिन द्वारा प्रेरित नेफ्रोटिक सिंड्रोम के मॉडल में, MSCs(मेसेनचिमल स्टेम सेल)मुख्य रूप से सूजन को नियंत्रित करके गुर्दे की मरम्मत में अपनी भूमिका निभाते हैं [114]। इसके अलावा, स्वस्थ दाताओं और अज्ञातहेतुक नेफ्रोटिक सिंड्रोम (INS) के रोगी MSCs के कार्यों और आकारिकी में स्पष्ट अंतर प्रदर्शित नहीं करते हैं(मेसेनचिमल स्टेम सेल), जो इंगित करता है कि MSCs(मेसेनचिमल स्टेम सेल)आईएनएस को ऑटोलॉगस कोशिकाओं के साथ इलाज के लिए इस्तेमाल किया जा सकता है [115]। MSC उपचार पेराक्रिन के तंत्र द्वारा GAN पर लाभकारी प्रभाव डालता है जो Th1/Th2 साइटोकाइन [116] के संतुलन को नियंत्रित करता है। एंटी-थिल के चूहे के मॉडल में।1-प्रेरित ग्लोमेरुलोनेफ्राइटिस, हाइपोक्सिक-पूर्व शर्त MSCs(मेसेनचिमल स्टेम सेल)HIFla/VEGF/Nrf2 [117] के सिग्नल ट्रांसडक्शन के माध्यम से ग्लोमेरुलर एपोप्टोसिस, ऑटोफैगी और सूजन को कम करें। प्रोग्राम(मेसेनचिमल स्टेम सेल)2-गुर्दे,1-क्लिप मॉडल [118] में गुर्दा उच्च रक्तचाप से राहत और गुर्दा समारोह में सुधार। ऑटोलॉगस मेसेनकाइमल स्ट्रोमल कोशिकाओं के साथ एंटीन्यूट्रोफिल साइटोप्लाज्मिक एंटीबॉडी-संबंधित वास्कुलिटिस [119] और ऑटोसोमल प्रमुख पॉलीसिस्टिक किडनी रोग [120] के खिलाफ शरीर का इलाज करते समय कोई प्रतिकूल घटना और गंभीर प्रतिकूल घटनाएं नहीं देखी गईं। मौजूदा शोध यह भी प्रस्तावित करते हैं कि MSCs(मेसेनचिमल स्टेम सेल)संभवतः IL-22 [121] के माध्यम से फोकल सेग्मल ग्लोमेरुलोस्केलेरोसिस से राहत दिलाता है।
अंत में, पशु मॉडल और नैदानिक परीक्षणों दोनों ने MSCs की क्षमता के बहुत सारे प्रमाण प्रदान किए(मेसेनचिमल स्टेम सेल)गुर्दे की बीमारियों के उपचार में; हालांकि, MSC-EVs के साथ उपरोक्त बीमारियों के उपचार में बहुत कम शोध हुआ है(बाह्य पुटिका), जिसका पता लगाया जाना बाकी है। यह संभव है क्योंकि ईवीएस का पृथक्करण, शुद्धिकरण और बड़े पैमाने पर उत्पादन(बाह्य पुटिका)एक चुनौती बने रहें; इसके अलावा, वह तंत्र जिसके द्वारा MSC-EVs गुर्दे की बीमारियों का इलाज करते हैं, स्पष्ट नहीं किया गया है। इसके अलावा, इष्टतम स्रोत, उचित खुराक, और ईवीएस के प्रशासन के उचित मार्ग को ध्यान में रखते हुए(बाह्य पुटिका), गुर्दे की बीमारियों के नैदानिक उपचार के लिए MSC-EVs के अनुप्रयोग की प्रभावकारिता का आकलन करने के लिए और अधिक शोध किए जाने की आवश्यकता है।

सिस्टैंच विर्कुंगमेंगुर्दा
निष्कर्ष
इस समीक्षा में, हमने MSC . के जटिल और महत्वपूर्ण प्रभावों की हालिया प्रगति को संक्षेप में प्रस्तुत किया है(मेसेनचिमल स्टेम सेल)-ईवीएस(बाह्य पुटिका)गुर्दे की बीमारियों में, जिसमें AKI, CKD, DN, ARVD, और गुर्दा प्रत्यारोपण शामिल हैं। बड़ी संख्या में लेख इस बात का समर्थन करते हैं कि अधिकांश किडनी रोग MSC से लाभान्वित हो सकते हैं(मेसेनचिमल स्टेम सेल)-ईवीएस(बाह्य पुटिका); हालांकि, गुर्दा प्रत्यारोपण के प्रभाव अभी भी विवादास्पद हैं। हालांकि एमएससी(मेसेनचिमल स्टेम सेल)-ईवीएस(बाह्य पुटिका)विभिन्न स्रोतों से पृथक पशु अध्ययनों और प्रीक्लिनिकल परीक्षणों में गुर्दे की बीमारियों के लिए चिकित्सीय एजेंटों के रूप में महान वादा दिखाते हैं, आगे के अध्ययन आवश्यक हैं क्योंकि इस समय केवल कुछ नैदानिक कार्यों का वर्णन किया गया है।
संदर्भ
फ्रेजर एसडीएस, रोडरिक पीजे। किडनी डिजीज इन द ग्लोबल बर्डन ऑफ डिजीज स्टडी 2017.Nat Rev Nephrol.2019;15(4):193-4.https://doi.org/10.1038/s41 581-019-0120-0।
चाड एआर। छोटी वाहिकाएँ, बड़ी भूमिका: वृक्क माइक्रोकिरकुलेशन और गुर्दे की चोट की प्रगति। उच्च रक्तचाप.2017;69(4):551-63.https://doi.org/10.1161/HYPERTENSIONAHA.116.08319।
क्रेमर ए, पिपियास एम, नूर्डज़िज एम, स्टेल वीएस, एफ़ेंटाकिस एन, अंबुहल पीएम, एट अल। यूरोपीय रेनल एसोसिएशन-यूरोपीय डायलिसिस एंड ट्रांसप्लांट एसोसिएशन (ईआरए-ईडीटीए) रजिस्ट्री वार्षिक रिपोर्ट 2015: एक सारांश। क्लिन किडनी जे.2018;11(1):108-22।
बस्तानी बी। प्रत्यारोपण अंग की कमी का वर्तमान और भविष्य: कुछ संभावित उपचार। जेनेफ्रोल.2020;33(2):277-88.https//doi.org/10.1007/s4 0620-019-00634-x।
स्क्वीलारो टी, पेलुसो जी, गाल्डेरिसी यू.क्लिनिकल परीक्षण के साथमेसेनचिमल स्टेम सेल: ताज़ा जानकारी। सेल प्रत्यारोपण। 2016;25(5):829-48.https://doiorg/10.3727/0963 68915SX689622.
अब्बासज़ादेह एच, घोरबानी एफ, डेराखशानी एम, मूवसघपुर ए, यूसेफी एम। मानव गर्भनाल मेसेनकाइमल स्टेम सेल-व्युत्पन्न बाह्य कोशिकीय पुटिका: एक उपन्यास चिकित्सीय प्रतिमान। जे सेल फिजियोल। 2020;235(2):706-17.https://doi. संगठन/10.1002/आईसीपी.29004
सिल्वा एमएल, चागास्टेल्स पीसी, नारडी एनबी।मेसेनचिमल स्टेम सेललगभग सभी प्रसवोत्तर अंगों और ऊतकों में 7d में रहते हैं। जे सेल साइंस.2006;119(11):2204-13।
ज़ुक पीए, झू एम, मिज़ुनो एच, हुआंग जे, फ़ुट्रेल डब्ल्यू, काट्ज़ एजे, बेनहैम पी, लोरेंज एचपी, हेड्रिक एमएच। मानव वसा ऊतक से बहुसंख्यक कोशिकाएं: सेल-आधारित उपचारों के लिए निहितार्थ। ऊतक इंजी. 2001;7(2):211-28.https://doi.org/10.1 089/107632701300062859।
मानव गर्भनाल रक्त में एरिसेस ए, कोंगेट पी, मिंगुएल जे। मेसेनकाइमल पूर्वज कोशिकाएं। बीआर जे हेमेटोल.2000;109(1):235-42.https://doi.org/10.1 046 /i.1365-2141.2000.01986.x,
एंकर पीएस, शेरजोन एसए, क्लेजबर्ग-वैन डेर केयूर सी, डी ग्रोट-स्विंग्स जी, क्लास एफएचजे, फिबे वी, एट अल। का अलगावमेसेनचिमल स्टेम सेलमानव अपरा से भ्रूण या मातृ उत्पत्ति का। स्टेम सेल। 2004;22(7):1338-45।
भारद्वाज एस, लियू जी, शिवाई, वू आर, यांग बी, हे टी, फैन वाई, लू एक्स, झोउ एक्स, लियू एच, अटाला ए, रोहोजिंस्की, झांग वाई। मानव मूत्र-व्युत्पन्न स्टेम कोशिकाओं के बहुसंख्यक भेदभाव: चिकित्सीय के लिए संभावित मूत्रविज्ञान में आवेदन। स्टेम सेल.2013;31(9):1840-56.
कैपलन एच, ओल्सन एसडी, कुमार ए, जॉर्ज एम, प्रभाकर केएस, वेन्ज़ेल पी, बेदी एस, टोलेडानो-फुरमैन एनई, ट्रायोलो एफ, काम्हिह-मिल्ज़ जे, मोल जी। कॉक्स सीएसजेआर। मेसेनकाइमल स्ट्रोमल सेल चिकित्सीय वितरण: नैदानिक अनुप्रयोग के लिए अनुवाद संबंधी चुनौतियां। फ्रंट इम्यूनोल.2019;10 https//doiorg/10.3389/immu.2 01901645।
